magnezyum
| özellikler | |||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Genel olarak | |||||||||||||||||||||||||||||||||||||||||||
| İsim , sembol , atom numarası | Magnezyum, Mg, 12 | ||||||||||||||||||||||||||||||||||||||||||
| Öğe kategorisi | alkali toprak metaller | ||||||||||||||||||||||||||||||||||||||||||
| Grup , nokta , blok | 2 , 3 , s | ||||||||||||||||||||||||||||||||||||||||||
| Dış görünüş | gümüş beyazı | ||||||||||||||||||||||||||||||||||||||||||
| CAS numarası | |||||||||||||||||||||||||||||||||||||||||||
| EC numarası | 231-104-6 | ||||||||||||||||||||||||||||||||||||||||||
| ECHA Bilgi Kartı | 100.028.276 | ||||||||||||||||||||||||||||||||||||||||||
| ATC kodu | |||||||||||||||||||||||||||||||||||||||||||
| Dünya kabuğunun kütle kesri | %1,94 | ||||||||||||||||||||||||||||||||||||||||||
| atomik | |||||||||||||||||||||||||||||||||||||||||||
| atom kütlesi | 24.305 (24.304-24.307) ve | ||||||||||||||||||||||||||||||||||||||||||
| Atom yarıçapı (hesaplanmış) | 150 (145) öğleden sonra | ||||||||||||||||||||||||||||||||||||||||||
| kovalent yarıçap | 141 öğleden sonra | ||||||||||||||||||||||||||||||||||||||||||
| Van der Waals yarıçapı | 173 pm | ||||||||||||||||||||||||||||||||||||||||||
| Elektron konfigürasyonu | [ Ne ] 3 sn 2 | ||||||||||||||||||||||||||||||||||||||||||
| 1. İyonlaşma enerjisi | 7..646 236 (4) eV ≈ 737.75 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||
| 2. İyonlaşma enerjisi | 15..035 271 (6) eV ≈ 1 450.68 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||
| 3. İyonlaşma enerjisi | 80.1436 (6) eV ≈ 7 732.68 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||
| 4. İyonlaşma enerjisi | 109.2654 (12) eV ≈ 10 542.51 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||
| 5. İyonlaşma enerjisi | 141.33 (3) eV ≈ 13 636 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||
| fiziksel olarak | |||||||||||||||||||||||||||||||||||||||||||
| Fiziksel durum | sabit | ||||||||||||||||||||||||||||||||||||||||||
| Kristal yapı | altıgen | ||||||||||||||||||||||||||||||||||||||||||
| yoğunluk | 1.738 g / cc 3 (20 ° C ) | ||||||||||||||||||||||||||||||||||||||||||
| Mohs sertliği | 2.5 | ||||||||||||||||||||||||||||||||||||||||||
| manyetizma | paramanyetik ( Χ m = 1.2 · 10 -5 ) | ||||||||||||||||||||||||||||||||||||||||||
| Erime noktası | 923 K (650 °C) | ||||||||||||||||||||||||||||||||||||||||||
| kaynama noktası | 1383K (1110°C) | ||||||||||||||||||||||||||||||||||||||||||
| molar hacim | 14.00 10 -6 m 3 mol -1 | ||||||||||||||||||||||||||||||||||||||||||
| Buharlaşma ısısı | 132 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||
| Füzyon ısısı | 8,7 kJ mol -1 | ||||||||||||||||||||||||||||||||||||||||||
| ses hızı | 4602 m s -1 293,15 K'da. | ||||||||||||||||||||||||||||||||||||||||||
| Özgül ısı kapasitesi | 1023 J kg -1 K -1 | ||||||||||||||||||||||||||||||||||||||||||
| iş fonksiyonu | 3.66 eV | ||||||||||||||||||||||||||||||||||||||||||
| Elektrik iletkenliği | 22,7 · 10 6 A · V -1 · m -1 | ||||||||||||||||||||||||||||||||||||||||||
| Termal iletkenlik | 160 W m -1 K -1 | ||||||||||||||||||||||||||||||||||||||||||
| kimyasal olarak | |||||||||||||||||||||||||||||||||||||||||||
| oksidasyon durumları | 1, 2 | ||||||||||||||||||||||||||||||||||||||||||
| Normal potansiyel | −2.372 V (Mg 2+ + 2 e - → Mg) | ||||||||||||||||||||||||||||||||||||||||||
| elektronegatiflik | 1.31 ( Pauling ölçeği ) | ||||||||||||||||||||||||||||||||||||||||||
| izotoplar | |||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||
| Diğer izotoplar için izotopların listesine bakın. | |||||||||||||||||||||||||||||||||||||||||||
| NMR özellikleri | |||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||
| güvenlik talimatları | |||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||
|
Olabildiğince ve alışılageldiği kadarıyla SI birimleri kullanılır. Aksi belirtilmedikçe, verilen veriler standart koşullar için geçerlidir . | |||||||||||||||||||||||||||||||||||||||||||
Magnezyum a, kimyasal element ile eleman sembolü Mg ( simya : ⚩) ve atom numarası 12. periyodik tablonun ikinci olduğu elemanlarının ana grup veya 2. IUPAC grubuna ve böylece ait alkalin toprak metalleri .
Magnezyum on biri en yaygın elementlerin yerkabuğu . Bitkilerin yaprak yeşilinde olduğu gibi çok sayıda mineralde de bulunur .
Öykü

Eleman atamasının kökeni literatürde farklı şekilde sunulmaktadır:
- "manyetik taş" anlamına gelen eski Yunanca μαγνησία λίθος'dan ,
- arasında Magnisia , doğu bir alandır Yunanistan ,
- dan Magnesia , Türkiye şimdi ne de Anadolu'daki bir şehirde.
Bununla birlikte, verilen tüm türevler etimolojik olarak mıknatıslardan veya onların isimsiz kahramanı Magnes'den geliyor gibi görünüyor .
Magnezyum bileşikleri, elemental magnezyumun üretilmesinden yüzyıllar önce biliniyordu ve kullanılıyordu. Magnesia alba , magnezyum karbonata atıfta bulunurken, magnezya, magnezyum oksitin ortak adıydı .
İskoç fizikçi ve kimyager Joseph Black , 18. yüzyılda magnezyum bileşiklerini sistematik olarak inceleyen ilk kişiydi. 1755'te De hume acido a cibis orto et Magnesia alba adlı çalışmasında , o zamanlar sıklıkla karıştırılan kireç ( kalsiyum karbonat ) ve magnesia alba (magnezyum karbonat) arasındaki farkı tanıdı . O anlaşılacaktır Magnesia alba olarak karbonatın yeni bir öğe. Bu nedenle Black, elemental magnezyumu hiçbir zaman temsil etmemesine rağmen, genellikle magnezyumun kaşifi olarak anılır.
1808'de Sir Humphry Davy kazanan bir yardımıyla nemlendirilmiş magnezyum hidroksit elektrolizi ile magnezyum volta sütun olmayan saf biçimde, ancak olarak - amalgam o birlikte çalıştığı, katot yapılmış cıva . O gösterdi magnezyum olduğu , ilk başta bir yeni metal oksit olarak adlandırılan magnium .
1828'de Fransız kimyager Antoine Bussy , kuru magnezyum klorürü indirgeyici madde olarak potasyum ile ısıtarak az miktarda saf magnezyum üretmeyi başardı . 1833'te Michael Faraday , erimiş magnezyum klorürün elektrolizi yoluyla magnezyum üreten ilk kişi oldu. Bu deneylere dayanarak, Alman kimyager Robert Wilhelm Bunsen , 1840'larda ve 1850'lerde, geliştirdiği Bunsen elementi yardımıyla erimiş tuzların elektrolizi yoluyla magnezyum üretimine yönelik işlemler üzerinde çalıştı . 1852'de erimiş, susuz magnezyum klorürden büyük miktarlarda magnezyum üretimi için bir elektroliz hücresi geliştirdi. Magnezyum üretimi için bu işlem günümüze kadar tercih edilmiştir.
Magnezyumun teknik üretimi, 1857'de Henri Etienne Sainte-Claire Deville ve H. Caron tarafından bir süreç kullanılarak Fransa'da başladı . Sözde Deville-Caron işleminde, susuz magnezyum klorür ve kalsiyum florür karışımı sodyum ile indirgenir. In İngiltere , Johnson Matthey 1860 etrafında benzer bir işlem kullanılarak magnezyum üretmeye başladı. Ancak, üretim zorlukları nedeniyle bu erken girişimler ekonomik olmadı.
oluşum

Magnezyum, tepki verme özelliğinden dolayı doğada elementel halde bulunmaz. Bir şekilde mineral , bunun şeklinde ağırlıklı olarak oluşur karbonatlar , silikatlar , klorürler ve sülfatlar . Dolomit formundaki bir magnezyum minerali bile dağ oluşturur, örn. B. Dolomitler'de .
En önemli mineraller dolomit CaMg (CO 3 ) 2 , manyezit (acı spar) MgCO 3 , olivin (Mg, Fe) 2 [SiO 4 ], enstatite MgSiO 3 ve kieserite MgSO 4 · H 2 O'dur .
Diğer mineraller şunlardır:
- Serpantin Mg 3 [Si 2 O 5 ] (OH) 4
- Talk Mg 3 [Si 4 O 10 ] (OH) 2
- Sepiyolit Mg 4 [Si 6 O 15 ] (OH) 2
- Schönite K 2 Mg (SO 4 ) 2 · 6 H 2 O
- Carnallite KMgCl 3 · 6H 2 O
- Spinel MgAl 2 O 4
Suda çözündüğünde kalsiyum ile birlikte su sertliğine neden olur . Gelen deniz suyu , bu fazla 1 kg / m³ dahil olduğunu.
Çıkarma ve sunum
Magnezyum esas olarak iki şekilde çıkarılır:
- Tarafından fused- tuzu elektroliz erimiş magnezyum klorür içinde Downs hücreleri : Downs hücreleri aşağıdaki ısıtılır büyük demir olukları oluşmaktadır. Yukarıdan gömülü grafit çubuklar, uçlarında halka şeklinde bir katot ile çevrelenen anot görevi görür . Metalik magnezyum üzerinde toplar eriyik tuz ve sıyrılabilir edilir. Oluşan klor gazı hücrenin üst kısmında toplanır ve magnezyum oksitten magnezyum klorür üretmek için yeniden kullanılır . Magnezyum klorürün erime noktasını düşürmek için erimiş tuza kalsiyum ve sodyum klorür eklenir.
- Magnezyum oksitin termal indirgenmesiyle (Pidgeon prosesi): Yanmış dolomit , barit ve ferrosilikon gibi bir indirgeyici ajan , krom-nikel çelikten yapılmış bir kaba dökülür . Daha sonra boşaltılır ( gaz pompalanır ) ve 1160 °C'ye ısıtılır. Buhar halindeki magnezyum yoğunlaşır üzerinde su soğutmalı dış kafa parçasının fırın . Partiler halinde elde edilen magnezyum, vakum damıtma ile daha da saflaştırılır.
Pidgeon süreci günümüzde en önemli üretim sürecidir ve çoğunlukla Çin'de kullanılmaktadır.
Küresel magnezyum üretiminin %88'i, 2015 yılında yaklaşık 800.000 ton magnezyum metalinin üretildiği Çin'de gerçekleşmektedir. Bunu , her biri yüzde birkaç pazar payına sahip olan Rusya , İsrail ve Kazakistan izlemektedir .
Üretim magnezyum 1 kg kullanılarak Pidgeon işlemini üreten sera gazlarının bir CO ile 2 (karşılaştırma için: 1 kg yaklaşık 31 kg eşdeğer çelik CO 0.5 ila 2 kg üreten 2 eşdeğer).
Magnezyum 60'dan mineraller de bulunmasına rağmen, sadece dolomit , magnezit , brusit , Carnallite , talk ve olivin olan ticari önem.
Mg + 2 - katyon olduğu deniz suyu , ikinci deniz suyu ve en bol katyon, deniz tuzu olanağına magnezyum çekici bir ticari kaynakları yapar. Çıkarmak için, bir magnezyum hidroksit çökeltisi oluşturmak üzere deniz suyuna kalsiyum hidroksit eklenir .
Magnezyum hidroksit (brusit) suda çözünmez ve süzülerek çıkarılabilir ve konsantre magnezyum klorür oluşturmak üzere hidroklorik asit ile reaksiyona sokulabilir.
Magnezyum , elektroliz yoluyla magnezyum klorürden üretilir .
özellikler
Katı, gümüşi, parlak hafif metal magnezyum, alüminyumdan yaklaşık üçte bir oranında daha hafiftir . Saf magnezyum, güç ve sertlik açısından zayıftır. Onun elastikiyet modülü yaklaşık 45 GPa. Havada magnezyum, alüminyumdan farklı olarak tamamen opak olmayan bir oksit tabakası ile kaplanmıştır. Bunun nedeni, magnezyum oksit, magnezyum kendisinden daha düşük bir mol hacme sahip olmasıdır (MgO: 10.96 cm 3 / mol Mg: 13.96 cm 3 / mol); bkz. Pilling-Bedworth oranı .
İnce şeritler veya folyoların tutuşması kolaydır. Bu oluşturulması için bir parlak beyaz alevle hava içerisinde yanan magnezyum oksit MgO ve biraz magnezyum nitrür Mg 3 K 2 . Taze yapılmış magnezyum tozu, kendiliğinden tutuşana kadar havada ısınabilir. Daha yüksek sıcaklıklarda, yani özellikle erimiş sıvılarda tehlikeli reaksiyonlar beklenebilir. Magnezyum ayrıca karbon monoksit , nitrojen oksit ve kükürt dioksit gibi birçok oksitte de yanar.
Magnezyum , hidrojen oluşturmak için su ile reaksiyona girer:
- Magnezyumun su ile reaksiyonu
Reaksiyonu büyük ölçüde durduran ( pasivasyon ) az çözünür bir magnezyum hidroksit kaplaması oluşur . Amonyum tuzları gibi zayıf asitler bile hidroksit iyonlarını suya dönüştürdükleri ve çözünür tuzlar oluşturdukları için hidroksit tabakasını çözmek için yeterlidir. Pasivasyon olmadan, ekzotermik reaksiyon şiddetlidir; magnezyum tozu ne kadar inceyse, o kadar şiddetlidir. Hava ile açığa çıkan hidrojen kolayca patlayıcı bir karışım ( oksihidrojen ) oluşturur.
Magnezyum, magnezyum oksit ve karbon oluşturmak için ekzotermik olarak karbondioksit ile reaksiyona girer :
Magnezyumun karbondioksit ile reaksiyonu
Bu nedenle, karbondioksit magnezyum yangınlarını söndürmez, aksine onları besler.
İçinde alüminyum aksine, bu göreceli olarak dirençli olan , hidroflorik asit ve bazlar . Bunun nedeni, düşük çözünürlüğü olan magnezyum flüorür (mgf 2 ) bir kaplama olarak oluşturulabilir önler Mg (OH) daha da oluşumunu 3 - iyonları.
izotoplar
19 mg ile 40 mg magnezyum arasında toplam 21 izotop bilinmektedir. Bu üçünden 24 mg, 25 mg ve 26 mg izotopları stabildir ve doğada bulunur. Doğal izotopik bileşimin daha büyük oranda olduğu izotop %78,99 ile 24 mg, 25 mg %10,0 ve 26 mg %11,01 oranındadır. En uzun ömürlü kararsız izotopları olan 28 Mg, dönüştürür için 28 Al bir ile yarılanma ömrü ile 20,915 saatlik beta çürüme ve 27 da Mg, çürükleri için 27 Al 9,435 dakikalık bir yarılanma ömrü ile . Diğer tüm izotopların yalnızca saniye veya milisaniyelik kısa yarı ömürleri vardır.
kullanmak
metalik magnezyum
Magnezyum tozu ve teli yanıcı cihazlarda , bombalarda ve parlama mühimmatında kullanılmakta olup, eski zamanlarda el feneri tozu olarak da kullanılmaktadır . Magnezyum çubuklar genellikle , soy metallerden yapılmış parçaları korozyondan koruyan kurban anotlar olarak hizmet eder .
Gelen metalürji magnezyum, çok yönlü olarak kullanılan
- z. B. titanyum ekstraksiyonu için Kroll işleminde indirgeyici ajan olarak ,
- uranyum , bakır , nikel , krom ve zirkonyum ekstraksiyonu için indirgeyici madde olarak ,
- AlSiMg ve AlMg gruplarının alüminyum alaşımlarının bir bileşeni olarak ,
- demir ve çeliğin kükürtten arındırılması için magnezyum granül olarak ,
- sfero dökme demir için katkı maddesi olarak
Magnezyum, uçak ve motorlu taşıtların yapımı için bir grup standartlaştırılmış hafif alaşıma dayanmaktadır ( erime , havaya ve oksidasyona maruz kalmaya karşı koruma sağlamak için bir erimiş magnezyum klorür kaplama tabakası gerektirir , s. Eritme işlemi ), ayrıca elektrona bakınız (Malzeme)
Diğer bir uygulama ise su altında yanan meşalelerdir .
Olarak organik kimya , üretilmesi için kullanılan Grignard bileşikleri .
Magnezyum çok kolay tutuştuğu için olumsuz koşullarda bile çalışan çakmak olarak da kullanılır . Yangın Başlatma Kitleri olarak satılan magnezyum bloklar , aşınması havada kendiliğinden tutuşan bir çakmaktaşı ile birlikte verilir. Prosedür, çakmaktaşı ve çıra ile bir ateş yakmanın Taş Devri yöntemine benzer , magnezyum çıra rolünü üstlenir. İlk olarak, talaşlar magnezyum bloğundan bir bıçakla kazınır ve gerçek yakıtın üzerine veya altına yerleştirilir. Ardından, çakmaktaşı kazıyarak (örneğin bıçağın arkası ile), onları tutuşturmak için magnezyum yongalarına mümkün olduğunca yakın kıvılcımlar üretilir.
Magnezyum alaşımları
Magnezyum alaşımlarını, alüminyum ve alaşımlarına göre önemli kılan en önemli özelliği, sağladıkları hafif yapıdır. Yaklaşık 1,75 g/cm³ yoğunluğuyla, yaklaşık 2,75 g/cm³ yoğunluğuyla hafif alüminyumdan farkı açıktır. Ayrıca erime aralığı 430 ile 630 °C arasındadır, bu da enerji tasarrufu için daha düşüktür. Ancak çekme mukavemeti ve sertlik gibi mekanik özellikler, alüminyum alaşımlarına göre önemli ölçüde daha düşüktür . Düşük yoğunluk, magnezyumu erken bir aşamada mobil uygulamalar için ilgi çekici hale getirdi. İlk büyük ölçekli uygulama , sert Zeppelin hava gemileri için iskele yapımında Birinci Dünya Savaşı'ndan önce gerçekleşti . Magnezyum alaşım kullanılmıştır olarak motorlu araçların yuva parçalarının üretimi için ve cep her türlü jantları üretimi için. 1930'dan sonra, magnezyum alaşımları giderek uçak yapımında kullanılan yaptıkları ağırlık tasarrufu olarak daha fazla enerji tasarrufu uçuşlar izin verdiği yanı sıra daha yüksek yükler. Hızlı (Almanya'da magnezyum üretiminin genişlemesine yol açtı Tüm bu elektron gelen Griesheim kimyasal fabrikada da ABD'de 1940 sonrası) ve,. Üretimin başlamasından hemen sonra "Elektron" ilk magnezyum alaşımlarının ticari markası oldu .
Magnezyum dökümleri için diğer olası kullanımlar, kısmen savaş nedeniyle, kısmen yapıcı olarak öngörülü ve aynı zamanda alaşımları optimize ederek, teknik gelişmeler sırasında kendilerini sundular. Mg-Al, Mg-Mn, Mg-Si, Mg-Zn ve son olarak Mg-Al-Zn alaşımları magnezyum bazlı malzemeler olarak geliştirildi.
İletim gövdesi VW böceği , bir Mg-Si alaşımından milyonlarca dökülmüştür. Günümüzde magnezyum alaşımları sadece ağırlıktan tasarruf etmek için kullanılmamakta, aynı zamanda yüksek sönümleme ile de karakterize edilmektedir. Titreşimlere maruz kaldığında bu, titreşim ve gürültü emisyonlarında bir azalmaya yol açar. Bu nedenle de magnezyum alaşımları, genel olarak otomobil yapımında olduğu gibi motor yapımında da ilgi çekici malzemeler haline gelmiştir. Bu nedenle parçalar yalnızca magnezyum alaşımlı motor değil, aynı zamanda Alfa Romeo 156'da ve daha sonra BMW'de seri üretimde ilk kez uygulanan hibrit proses / hibrit döküm motor bloklarının dökümü için de giderek artmaktadır (ayrıca bkz . BMW N52 ).

Olarak döküm işlemi (ayrıca bkz döküm , pek çok, daha büyük, ince duvarlı bileşenler nihai boyutlarına ve pahalı son işlem olmadan yakın üretilebilir). B. jantlar, profiller, muhafazalar, kapılar, kaputlar, bagaj kapakları, el freni kolları ve diğerleri. Mg-Al-Zn alaşımlarından yapılan parçalar sadece otomotiv mühendisliğinde değil, makine mühendisliğinde de kullanılmaktadır.
Hafif yapıya yönelik çabalar, 20. yüzyılın sonunda zaten magnezyum-lityum alaşımlarına , hatta lityum ilavesiyle magnezyumdan daha hafif alaşımlara yol açtı .
Tıpta magnezyum malzemeleri
En son araştırmalar , insan vücudu için emilebilir implant malzemesi (örneğin stent olarak ) olarak magnezyum malzemelerinin yüksek gelişme potansiyeli vaat ediyor . Magnezyum malzemeleri kullanım sırasında temas korozyonundan korunmalıdır. Korozyon direnci normal atmosferik etkilere Ancak iyidir. Temas korozyon davranışı, belirli bir süre sonra güvenli bir şekilde çözüleceğinden, sınırlı bir süre kullanılacak bir implant malzemesi olarak kullanıldığında belirleyici bir avantaj olacaktır. Bu, implantları çıkarma operasyonunun risklerini ve maliyetlerini ortadan kaldırır.
fizyoloji
Magnezyum temel maddelerden biridir ve bu nedenle tüm organizmalar için vazgeçilmezdir. Bitkilerin yeşil yaprakları olan klorofil , yaklaşık %2 magnezyum içerir. Orada klorofilin merkez atomunu oluşturur. Olarak magnezyum eksikliği soldurmak bitkiler hem de hafif eksikliği. Magnezyum eksikliğini önlemek için insan vücuduna ayrıca günlük olarak yeterli miktarda magnezyum sağlanmalıdır.
Bir yetişkinin vücudu yaklaşık 20 g magnezyum içerir (karşılaştırma için: 1000 g kalsiyum ). Kan plazmasında magnezyumun %40'ı proteinlere bağlıdır; normal serum seviyesi 0.8–1.1 mmol / l'dir. Magnezyum, bir enzim bileşeni veya koenzim olarak yaklaşık 300 enzim reaksiyonunda yer alır. Ek olarak, serbest Mg iyonları hücre zarı üzerindeki potansiyeli etkiler ve bağışıklık sisteminde ikinci bir haberci görevi görür . Bu stabilize dinlenme potansiyelini ve uyarılabilir kas ve sinir hücrelerinin ve hücreler otonom sinir sistemi . Magnezyum eksikliği huzursuzluğu, sinirliliği, sinirliliği, konsantrasyon eksikliğini, yorgunluğu, genel halsizliği, baş ağrılarını , kardiyak aritmileri ve kas kramplarını tetikler . Kalp krizleri de meydana gelebilir. Metabolizma ve ruh alanında, magnezyum eksikliğinin depresyon ve şizofrenik psikozları şiddetlendirdiği varsayılmaktadır . Bir kan magnezyumun fazla sinir sistemi ve kalp bozukluğu aşırı alımı ve böbrek fonksiyon bozukluğu ve potansiyel nedeniyle oluşabilir.
Magnesiumresorption ilk olarak üst bulundu ince bağırsak yerine, ancak sindirim sistemi geri kalanında. Böbrekler yoluyla atılır ve tüm gıdalarda ve içme suyunda farklı miktarlarda bulunur. Gerekli günlük yaklaşık 300 mg doz, genellikle dengeli bir diyetle elde edilir. Artan bir ihtiyaç, diyet takviyeleri veya ilaçlarla karşılanabilir . Ciddi hastalık, hamilelik veya rekabetçi sporlar nedeniyle hafif bir magnezyum eksikliği mümkündür. Böbrek fonksiyon bozukluğu, uzun süreli ishal, kronik bağırsak iltihabı, kötü kontrol edilen diyabetes mellitus, kortikoidler , belirli diüretikler veya yetersiz beslenme ile birlikte alkolizm ile ciddi eksiklikler ortaya çıkar .
Sitrat , glukonat , aspartat ve aspartat hidroklorür gibi magnezyum tuzları , kas krampları, migren veya hamilelik komplikasyonları gibi eksiklikler ve nöromüsküler rahatsızlıklara karşı Almanya'da günlük 100 ila 400 mg dozlarda tıbbi ürünler olarak onaylanmıştır . Yan etkileri gastrointestinal şikayetler ve ishaldir, aşırı doz durumunda ayrıca yorgunluk ve yavaş nabız. Böbrek fonksiyon bozukluğu ve bazı kardiyak aritmiler kontrendikasyondur .
Magnezyum takviyelerini ağızdan alırken (tabletler, çiğnenebilir veya pastiller, sıvı içinde çözülecek granüller), dozaj önemlidir. Çeşitli çalışmalar, 120 mg alındığında yaklaşık %35'inin , ancak 360 mg'lık tam günlük doz alındığında yalnızca yaklaşık %18'inin emildiği sonucuna varmıştır . Vücutta emilim için bugün ilaçlarda kullanılan bileşiklerin formu önemsizdir, çünkü bunlar farmakolojik, biyolojik ve klinik olarak eşdeğerdir; Magnezyum aspartat veya magnezyum sitrat gibi organik tuzlar, vücut tarafından inorganik bileşiklerden daha hızlı emilir. Öte yandan, ek magnezyum, vücutta yeterli miktarda bağlayıcı molekül varsa, vücutta yararlı bir şekilde kalır; Bu, ancak en az dört hafta boyunca magnezyum arzında veya tüketiminde daha uzun bir artıştan sonra biyokimyasal ayarlamalar yoluyla gerçekleşir.
Magnezyum sülfat ("Epsom tuzu") daha önce müshil olarak kullanılıyordu ve kardiyak aritmileri tedavi etmek için kullanılıyordu.
Magnezyum tuzları alternatif tıpta kullanılmaktadır .
Gıda
Magnezyum , özellikle ATP ve nükleik asit bağlayıcı enzimlerde olmak üzere yaklaşık 300 farklı protein için bir kofaktör görevi görür . İnsanlar için önerilen günlük magnezyum alımı, yaşa ve cinsiyete bağlı olarak günde 24 ila 400 mg arasındadır.
Magnezyum, özellikle de çok sayıda gıdalarda bir bileşik olarak ortaya bütün tahıl ürünleri , (örneğin bütün tahıl ekmeği , bütün tahıl makarna , bütün tahıl , pirinç , yulaf gevreği , mısır gevreği ,) maden suyu , özellikle tıbbi su , musluk suyu , yeterli su sertliği , ciğer , kümes hayvanları , sofra balıkları , kabak çekirdeği , ay çekirdeği , çikolata , kaju fıstığı , yer fıstığı , patates , ıspanak , alabaşlar , çilek , portakal , muz , susam , pancar şurubu , süt ve süt ürünleri .
Tehlikeler ve koruyucu önlemler
Elementel magnezyumun tehlikeliliği, sıcaklığa ve parçacık boyutuna büyük ölçüde bağlıdır: kompakt magnezyum, erime noktasının altındaki sıcaklıklarda zararsızdır, magnezyum talaşı ve tozu ise oldukça yanıcıdır . Geniş yüzey alanı nedeniyle, ikincisi havadaki oksijenle kolayca reaksiyona girebilir. Çok ince magnezyum tozu ile kendi kendine tutuşma riski vardır ; Hava-toz karışımları bile patlayıcıdır . Flegmatizasyon , genel olarak magnezyum ve metal tozları işlenirken riski azaltan bir tedavidir. Erimiş magnezyum ayrıca havada kendiliğinden tutuşur. İnce taneli veya ısıtılmış magnezyum, su ve diğer oksijen içeren bileşikler gibi birçok başka maddeyle de reaksiyona girer. Magnezyum eriyikleri bu nedenle atmosferik oksijen girişine karşı kalıcı koruma gerektirir. Pratikte bu, eriyiğin magnezyum klorür açısından zengin maddelerle kaplanmasıyla yapılır. Oksidasyona karşı koruma olarak kükürt heksaflorür de uygundur. Geçmişte alışılmış olan elementel kükürt ile kaplama, üretilen kükürt dioksitin neden olduğu ciddi rahatsızlık nedeniyle artık uygulanmamaktadır.
Magnezyum yangınlarında 3000 °C civarında sıcaklıklar oluşur. Magnezyum bunlarla şiddetli reaksiyona girdiğinden , su , karbon dioksit , köpük veya nitrojen gibi yaygın söndürücü maddeler hiçbir koşulda kullanılmamalıdır. Su bir magnezyum ateşiyle temas ederse, akut bir oksihidrojen reaksiyonu riski vardır .
Bir eriyiğin ateşi ( metal yangını ) için, oksijenin hızlı yer değiştirmesi gibi boğulma söndürme ilkesi geçerlidir. En basit durumda, kuru kumla kaplayarak, aksi takdirde magnezyum eriyikleri için bir kaplama tuzu uygulayarak. D sınıfı yangın söndürme tozları , magnezyum oksit tozu ( Magnesia usta / yanmış magnesia ) ve gerekirse kuru, paslanmayan gri dökme demir talaşları da uygundur .
Magnezyum kullanırken, verilen tüm güvenlik talimatlarına tam olarak uyulmalıdır. Hiçbir koşulda patlayıcı bir ortam (magnezyum tozu, hidrojen, aerosoller ve yanıcı soğutma yağlarının buharları) ortaya çıkmamalıdır. Tutuşturma kaynaklarından kaçınmak gibi normal iş güvenliği önlemleri de dikkate alınmalıdır.
kanıt
En iyi yolu saptamak magnezyum vasıtasıyladır Magneson II , san bir titanyum veya quinalizarin .
Magneson II (4- (4-nitrofenilazo) -1-naftol) ile tespit için orijinal madde suda çözülür ve alkali hale getirilir. Daha sonra birkaç damla azo boya Magneson II çözeltisi eklenir. Magnezyum iyonları varsa koyu mavi renkli bir vernik oluşur. Diğer alkali toprak metaller önce çökeltme ile karbonatlar olarak uzaklaştırılmalıdır.
Titan sarısı ( tiyazol sarı G) ile tespit için orijinal madde suda çözülür ve asitleştirilir. Daha sonra bir damla titanyum sarısı çözeltisi ile karıştırılır ve seyreltik sodyum hidroksit çözeltisi ile alkali hale getirilir. Magnezyum varsa, açık kırmızı bir çökelti oluşur. Nikel, çinko, manganez ve kobalt iyonları bu algılamaya müdahale eder ve önceden sülfit olarak çökeltilmelidir.
Kinalizarin ile tespit için, asidik numune çözeltisine iki damla boya çözeltisi eklenir. Daha sonra reaksiyon bazik olana kadar seyreltik sodyum hidroksit çözeltisi ilave edilir. Mavi renk veya yağış magnezyumu gösterir.
Fosfat tuzu çözeltileri ile çökelti oluşumu, magnezyum tuzları için bir tespit reaksiyonu olarak da kullanılabilir. Amonyak ve amonyum klorür ile pH 8 ila 9'a tamponlanan ağır metal içermeyen numune çözeltisi, disodyum hidrojen fosfat çözeltisi ile karıştırılır. Magnezyum amonyum fosfat MgNH 4 PO 4'ün neden olduğu beyaz, asitte çözünür bir bulanıklık magnezyum iyonlarını gösterir:
Amonyak çözeltisinden Mg2 +, zayıf çözünür sarı-yeşilimsi bir bileşik olarak oksin ile de tespit edilebilir. Bu ispat katyon ayırma işlemi için uygundur .
bağlantılar
Olarak bileşikler , magnezyum, bir iki değerli olarak hemen hemen istisnasız meydana katyon ile oksidasyon halinde 2.
Oksitler ve hidroksitler
Magnezyum oksit (magnezyum) renksiz sodyum klorür kristalleri oluşturur - yapı . Doğada volkanik mineral periklaz olarak bulunur . Bunlar ayrıca koyu yeşil, cam gibi parlayan düzenli kristaller içeren kapanımlar nedeniyle beyazdan griye kadardır.
Magnezya tozu, gıdalara asitlik düzenleyici veya ayırıcı madde olarak eklenir . Laboratuvarlar ve endüstri için çeşitli ısıya dayanıklı nesneler magnezyum oksit seramiklerinden yapılmıştır .
Magnezyum hidroksit renksiz, kuvvetli bazik bir tuzdur ve doğal olarak mineral brusit olarak bulunur . Bu sahip üç köşeli bir kristal yapıya içinde boşluk grubu P 3 m 1 (boşluk grubu no. 164), ve bir olarak kullanılan pişirme yağı katkı maddesi (bağlanma için sülfür dioksit bir şekilde,) topaklaştırıcı için atık su olarak, alev geciktiriciler olarak termoplastik plastik ( poliolefinler , polivinil klorür ) ve elastomerler gibi, katkı maddesi kullanılır olarak deterjanlar . Olarak ilaç bu olarak kullanılan bir antasit için nötralize mide asidi ve hafif bir şekilde laksatif kullanılır.
Magnezyum peroksit bir olan bir ince toz haline getirilmiş, renksiz bir bileşik olup, pirit kristal yapısı boşluk grubuna Pa 3 (boşluk grubu no. 205) . Bu benzer kalsiyum peroksit ve serbest bırakır oksijen kontrollü ile reaksiyona ile sulu çözeltiler . Tarım , ilaç ve kozmetikte çeşitli kullanımları vardır .
gübre
Tüm kireçleme ekin ve çayır alanlar, magnezyum şeklinde kullanılan magnezyum oksit ya da magnezyum karbonat için telafi magnezyum mahrum toprak ile bitki . Ayrıca, toprak pH değeri arttırılır ve diğer besin maddelerinin mevcudiyeti iyileştirilir. Magnezyum bileşiği genellikle kireçle birlikte magnezyum ve kalsiyum içeren kompleks bir gübre olarak kullanılır . Doğal olarak Bobierrit olarak bulunan magnezyum fosfat Mg 3 (PO 4 ) 2 ( trimagnezyum fosfat ) ve magnezyum nitrat da kompleks gübreler olarak kullanılır.
Halideler

Magnezyum klorür oldukça higroskopiktir ve mineral bishopitte (MgCl 2 · 6 H 2 O), çift tuzlu karnalit (KMgCl 3 · 6 H 2 O), deniz suyunda ve tuz göllerinde doğal olarak oluşur . Bu kristalize olur köşeli bir kristal sistemi içinde boşluk grubu R, 3 m (boşluk grubu no. 166) . Gıda teknolojisinde asit düzenleyici , sıkılaştırıcı , aroma arttırıcı , taşıyıcı veya ayırıcı olarak kullanılır . Bir termal pil olarak, magnezyum klorür heksahidrat , ısı enerjisini depolayabilir ve serbest bırakabilir.
Magnezyum florür formları renksiz kristaller kristalize tetragonally içinde rutil yapısı içinde boşluk grubu P 4 2 / mnm (boşluk grubu no. 136) boşluk grubu . Bu , optik özellikler, birlikte sahip kimyasal stabilite, bunu yapmak önemli bir malzeme, optik uygulamalarda.
Magnezyum bromür ve magnezyum iyodür da bir üç köşeli bir kristal yapıya sahip higroskopik tuzlar boşluk grubu P 3 m 1 (boşluk grubu no. 164) .
Diğer inorganik bileşikler
Magnezyum karbonat doğal olarak manyezit (acı spar) olarak büyük miktarlarda bulunur . Bu kristalize trigonally içinde boşluk grubu R, 3 , c (boşluk grubu no. 167) . Olarak gıda endüstrisinde bu şekilde ilave edilir , bir asit düzenleyici , taşıyıcı madde ya da serbest bırakma ajanı. Tırmanma ve jimnastikte kullanılır ve ayrıca magnezya ve tebeşir isimleriyle bilinir . Sporcular onu böylece daha sonra egzersiz başlangıcından önce o avuç kuru cilt barları kapsayan süre külçe veya demir çubuklar germe uzun veya halter çok sorumlu değildir. Ayrıca tıbbi ve endüstriyel kullanımları vardır.
Magnezyum nitrat , renksiz bir higroskopik tuz kolayca olan çözünür olarak su . Heksahidrat (Mg (NO 3 ) 2 · 6H 2 O) sahip monoklinik kristal yapıya sahip boşluk grubu P 2 1 / c (boşluk grubu no. 14) . Bu şekilde kullanılan gübre , latent ısı depolama (heksahidrat gibi) ya da seramik endüstrisi.
Magnezyum sülfat heptahidrat (Mg (SO 4 ) 7H 2 O), mineral epsomit (Epsom tuzu) olarak bilinir . Eşkenar dörtgen bir psödotetragonal kristal kafes oluşturan renksiz kristaller oluşturur . Kristaller, genellikle lifli çiçek açar agrega ve form dikit . Bu kullanılan gübre bir şekilde, kurutucu ve şifalı uygulamalar için.
Magnezyum fosfatlar (magnezyum dihidrojen fosfat (Mg (H 2 PO 4 ) 2 ), magnezyum hidrojen fosfat (MgHPO 4 ) ve magnezyum fosfat (Mg 3 (PO 4 ) 2 )) 'de kullanılan sanayi olarak seramik hammadde ve benzeri gibi alev geciktirici . Gıda endüstrisinde yem katkı maddesi , müshil ve gıda katkı maddesi olarak kullanılırlar . Asitlik düzenleyiciler veya salma ajanları olarak gıdalara eklenirler.
Spinel sık ortaya çıkan bir olan , mineral ile ilgili mineral sınıfı arasında oksitler ve hidroksitler idealize ile kimyasal bileşimi mgAl 2 O 4 ve bu nedenle bir magnezyum alüminat , bir gelen kimyasal noktası görüntüsü . Bu kristalize isotypically ile manyetit olarak kübik kristal sistemi içinde boşluk grubu Fd 3 m (boşluk grubu no. 227) .
Dolomit , CaMg [CO 3 ] 2 kimyasal bileşimine sahip karbonatlar ve nitratların mineral sınıfından çok yaygın bir mineraldir ve bu nedenle kimyasal olarak bir kalsiyum- magnezyum karbonattır. Bu kristalize olur köşeli bir kristal sistemi içinde boşluk grubu R ' 3 (boşluk grubu no. 148) .
Magnezyum hidrit , hidrojen ve enerji depolamak için kullanılabilir. Tarafından , hidrojen , magnezyum hidrid, bir salınır, metal köpüğün daha hafif ilginç özellikleri olan su oluşturulur.
Diğer ilginç kristalli magnezyum bileşikleri, örneğin, magnezyum diborid , magnezyum karbür , magnezyum nitrür , magnezyum sülfür , magnezyum silisit , magnezyum germanid , magnezyum metasilikat , magnezyum titanyum oksit ve magnezyum poloniddir .
Magnezyum organilleri
Magnezyum organilleri, magnezyum ve karbon arasında bir bağ bulunan organometalik bileşiklerdir . Magnezyum organilleri arasında Grignard bileşikleri ( R -Mg- X ) açık ara en önemlileridir. Magnezyum ve alkenil magnezyum halojenürlerin ikili organilleri açıkça ikincil bir rol oynamaktadır.
Organil magnezyum halojenürler
Organil magnezyum halojenürler (genellikle Grignard bileşikleri olarak adlandırılır ), organil halojenürlerin magnezyum talaşları ile reaksiyonu yoluyla doğrudan bir işlemde elde edilir . Grignard reaktifleri , Schlenk dengesinde çözelti halindedir . Element organillerine halojen - organil - ikame ile reaksiyona girerler:
Genel olarak:
z. B.:
veya çoklu bağ sistemlerine sahip organillerin eklenmesiyle :
Genel olarak:
z. B .:
Magnezyum ikili organilleri
İkili magnezyum organiller (R 2 Mg, ayrıca magnezyum diorganiller olarak da adlandırılır) farklı şekillerde üretilebilir:
- transmetalasyon yoluyla , örneğin cıva diorganilleri:
- nedeniyle dismutasyon zaman Schlenk denge kaydırılır yardımıyla , 1,4-dioksan :
- Magnesasikller ( halkasında magnezyum bulunan siklik alkanlar ) 1,4-dioksan yardımıyla da hazırlanabilir .
- tarafından metatez ait Grignard bileşikleri ile lityum organiller
- hidromagnezasyon ile (MgH 2'nin 1-alkenlere eklenmesi ):
- nedeniyle ilave bir element , C = C magnezyum çift bağı , bazı doymamış hidrokarbonlar gibi 1,3-bütadien veya antrasen (metal ekleme). Örneğin, 1,3-bütadien'in tetrahidrofuran içinde oda sıcaklığında reaksiyonu mümkündür :
- (2-büten-1,4-diil) magnezyum olarak da adlandırılan üretilen magnezyum bütadien, daha sonraki sentezlerde bütadien anyonları kaynağı olarak kullanılabilir . Turuncu-sarı magnezyum antrasen benzer şekilde görüntülenir. Magnezyum antrasen daha sonra magnezyumun hidrojenasyonu için bir katalizör olarak kullanılabilir .
alkenil magnezyum halojenürler
Karbomagnezasyon olarak bilinen olayda, alkinler alkinlerle reaksiyona girerek alkenil magnezyum halojenürler oluşturur:
Diğer organik bileşikler
Magnezyum hidrojen sitrat ve trimagnezyum disitrat , sitrik asidin magnezyum tuzlarıdır . Magnezyum sitrat ilaç olarak kullanılır .
Magnezyum monoperoksiftalat a, dezenfektan için yüzey dezenfeksiyonu .
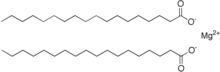
Magnezyum stearat , stearik asidin magnezyum tuzudur ve kireç sabunlarından biridir . Bir magnezyum iyonu ve iki uzun zincirli stearat iyonundan oluşur.
İnternet linkleri
Bireysel kanıt
- ↑ a b Harry H. Binder: Kimyasal elementler sözlüğü. S. Hirzel Verlag, Stuttgart 1999, ISBN 3-7776-0736-3 .
- ↑ Özellikler (bilgi kutusu) değerleri aksi belirtilmedikçe www.webelements.com (magnezyum) adresinden alınmıştır.
- ↑ Verilen IUPAC, IUPAC tarafından önerilen standart değerdir, çünkü bu elementin izotopik bileşimi yerel olarak değişebildiğinden, parantez içinde verilen kütle aralığı, ortalama atom ağırlığını gösterir. Standart Atom Ağırlıkları Revize 2013 .
- ↑ a b c d e Kramida, A., Ralchenko, Yu., Reader, J. ve NIST ASD Ekibinde magnezyum üzerine giriş (2019): NIST Atomic Spectra Database (ver. 5.7.1) . Ed.: NIST , Gaithersburg, MD. doi : 10.18434 / T4W30F ( https://physics.nist.gov/asd ). 11 Haziran 2020'de alındı.
- ↑ a b c d e Magnezyum ile ilgili giriş WebElements, https://www.webelements.com , 11 Haziran 2020'de erişildi.
- ^ NN Greenwood, A. Earnshaw: Elementlerin Kimyası. 1. baskı. VCH, Weinheim 1988, ISBN 3-527-26169-9 , sayfa 136.
- ↑ David R. Lide (Ed.): CRC Kimya ve Fizik El Kitabı . 90. baskı. (İnternet versiyonu: 2010), CRC Press / Taylor ve Francis, Boca Raton, FL, Magnetic Suceptibility of the Elements and Inorganik Compounds, s. 4-144. Oradaki değerler g/mol bazında olup cgs biriminde verilmiştir. Burada verilen değer, ölçü birimi olmaksızın ondan hesaplanan SI değeridir.
- ↑ a b Yiming Zhang, Julian RG Evans, Shoufeng Yang: El Kitaplarında Elemanların Kaynama Noktaları ve Buharlaşma Entalpileri için Düzeltilmiş Değerler. İçinde: Kimya ve Mühendislik Verileri Dergisi. Cilt 56, 2011, sayfa 328-337, doi: 10.1021 / je1011086 .
- ↑ Ludwig Bergmann, Clemens Schaefer, Rainer Kassing: Deneysel Fizik Ders Kitabı. Cilt 6: Katılar. 2. Baskı. Walter de Gruyter, 2005, ISBN 3-11-017485-5 , s. 361.
- ↑ A. Stasch, C. Jones: Kararlı dimerik magnezyum (I) bileşikleri: kimyasal işaretlerden çok yönlü reaktiflere kadar. İçinde: Dalton İşlemleri . Cilt 40, 2011, sayfa 5659-5672, doi: 10.1039 / C0DT01831G .
- ↑ David R. Lide (Ed.): CRC Kimya ve Fizik El Kitabı . 90. baskı. (İnternet versiyonu: 2010), CRC Press / Taylor ve Francis, Boca Raton, FL, Electrochemical Series, s. 8-22.
- ↑ bir B ile ilgili kayıt magnezyum, toz, stabilize içinde bir GESTIS madde veritabanı İFA 9 Ağustos 2016'da erişilebilir. (JavaScript gerekli)
- ↑ üzerinde giriş magnezyum içinde sınıflandırılması ve Etiketleme Envanteri Avrupa Kimyasallar Ajansı (AKA), 1 Ağustos'ta erişilen, 2016 Üreticileri veya distribütörler olabilir genişletmek uyumlaştırılmış sınıflandırma ve etiketleme .
- ↑ 26A9 (Hex) karakterlerinin Unicode Standardı, Sürüm 5.2'de (PDF; 291 kB) magnezyum olarak tanımı .
- ^ ABD Jeolojik Araştırması, Mineral Emtia Özetleri, Ocak 2016
- ↑ Volker Hasenberg: Magnezyum üretiminin yaşam döngüsü analizi ve ekolojik değerlendirmesi. PE INTERNATIONAL, Akıllı Hafif Ağaçlar için Malzeme Forumu 24 Nisan 2012, Hannover Fuarı.
- ↑ Magnezyum ve CO 2 Arasındaki Reaksiyon . Purdue Üniversitesi, 15 Haziran 2016'da erişildi .
- ↑ G. Audi, FG Kondev, Meng Wang, WJ Huang, S. Naimi: Nükleer özelliklerin NUBASE2016 değerlendirmesi. In: Chinese Physics C. 41, 2017, S. 030001, doi: 10.1088 / 1674-1137 / 41/3/030001 (tam metin)
- ↑ FY Li, B. Chaigne-Delalande ve diğerleri: Mg 2+ için insan T-hücresi immün yetmezliği tarafından ortaya konan ikinci haberci rolü . İçinde: Doğa. Cilt 475, Sayı 7357, Temmuz 2011, sayfa 471-476; doi: 10.1038 / doğa10246 . PMID 21796205 ; PMC 3159560 (ücretsiz tam metin).
- ↑ a b c Sighart Golf: Organik ve inorganik bileşiklerin biyoyararlanımı. İçinde: İlaç gazetesi . Temmuz 2009, erişildi 4 Mart 2015 .
- ^ R. Swaminathan: Magnezyum metabolizması ve bozuklukları. In: Clin Biochem Rev. 24 (2), Mayıs 2003, s. 47-66. PMID 18568054 .
- ↑ z. B. Kenneth D Fine, Carol A Santa Ana, Jack L Porter, John S Fordtran: Magnezyumun gıdalardan ve takviyelerden bağırsak emilimi. İçinde: J Clin Invest . Cilt 88 (2), Ağustos 1991, s. 396-402, PMC 295344 (serbest tam metin, PDF), doi: 10.1172 / JCI115317 .
- ↑ Örneğin bkz. K. Knudsen, J. Abrahamson: Magnezyum sülfatın antiaritmik etkileri. Üç vaka raporu. İçinde: Acta Anesthesiologica Scandinavica. Cilt 39, No. 6, (Kopenhag) 1995, s. 850.
- ↑ Alman Beslenme Derneği : Besin alımı için referans değerler: Magnezyum . 20 Ekim 2013'te erişildi.
- ↑ Magnezyum hidroksit girişi . İçinde: Römpp Çevrimiçi . Georg Thieme Verlag, 13 Haziran 2014'te erişildi.
- ↑ Georg Brauer (Ed.), Marianne Baudler ve diğerlerinin işbirliğiyle : Handbook of Preparative Inorganic Chemistry. 3., gözden geçirilmiş baskı. Cilt II, Ferdinand Enke, Stuttgart 1978, ISBN 3-432-87813-3 , s. 907.
- ↑ Ekilebilir arazilerin ve otlakların kireçlenmesi. (PDF; 43 kB) (Artık mevcut çevrimiçi.) DLR Rheinhessen-Nahe-Hunsrück, arşivlenmiş orijinal üzerinde 14 Şubat 2016 ; 14 Şubat 2016 tarihinde erişildi .
- ↑ Science-Online-Lexica: Magnezyumfosfat. İçinde: Kimya Sözlüğü. 26 Mayıs 2011 alındı.
- ↑ Magnezyum nitrat girişi . İçinde: Römpp Çevrimiçi . Georg Thieme Verlag, 26 Mayıs 2011'de erişildi.
- ↑ Tuzdan yapılan ısı depolama . 2012'den makale.
- ↑ için Giriş hiçbir CAS. 7783-40-6 içinde bir GESTIS madde veritabanı IFA , 17 Ekim 2012 tarihinde erişti. (JavaScript gerekli)
- ^ MA Brogan, AJ Blake, C. Wilson, DH Gregory: Magnezyum diiyodür, MgI 2 . İçinde: Açta Crystallographica , C59, 2003, s. I136-i138, doi: 10.1107 / S0108270103025769 .
- ^ Hans Lohninger: Sporcular için Magnesia. Erişim tarihi: 6 Temmuz 2019 .
- ↑ ilgili kayıt magnezyum nitrat içinde arasında GESTIS madde veritabanı İFA 23 Temmuz 2016'da erişilebilir. (JavaScript gerekli)
- ↑ Spinel. İçinde: mindat.org. Hudson Mineraloji Enstitüsü, 15 Mayıs 2019'da erişildi .
- ^ Hugo Strunz , Ernest H. Nikel : Strunz Mineralojik Tabloları. Kimyasal-yapısal Mineral Sınıflandırma Sistemi . 9. baskı. E. Schweizerbart'sche Verlagbuchhandlung (Nägele ve Obermiller), Stuttgart 2001, ISBN 3-510-65188-X , s. 188 .
- ^ Hugo Strunz, Ernest H. Nikel: Strunz Mineralojik Tabloları. Kimyasal-yapısal Mineral Sınıflandırma Sistemi . 9. baskı. E. Schweizerbart'sche Verlagbuchhandlung (Nägele ve Obermiller), Stuttgart 2001, ISBN 3-510-65188-X , s. 287 .
- ↑ Reuben D. Rieke: Yüksek düzeyde reaktif metal tozlarının hazırlanması ve bunların organik ve organometalik sentezde kullanımı. İçinde: Kimyasal Araştırma Hesapları. Cilt 10, Sayı 8, Ağustos 1977, sayfa 301-306, doi: 10.1021 / ar50116a005 .
- ^ AF Holleman , E. Wiberg , N. Wiberg : İnorganik Kimya Ders Kitabı . 102. baskı. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1 , s. 1233.
- ↑ Christoph Elschenbroich : Organometallchemie . 6., gözden geçirilmiş baskı. Vieweg + Teubner, 2008, ISBN 978-3-519-53501-0 ( Google kitap aramada kitap önizlemesi ).
- ↑ Yukitami Saheki, Katsuhiko Sasada, Nobumasa Satoh, Noriyuki Kawaichi, Kenji Negoro: Bir Grignard Reaktifinden Saf Dialkilmagnezyumun Uygun Hazırlanması. İçinde: Kimya Mektupları. Cilt 16, 1987, sayfa 2299-2300, doi: 10.1246 / cl.1987.2299
- ↑ Borislav Bogdanovic: Magnezyum antrasen sistemleri ve sentez ve katalizdeki uygulamaları. İçinde: Kimyasal araştırma hesapları. Cilt 21, Sayı 7, Temmuz 1988, sayfa 261-267 , doi: 10.1021 / ar00151a002 .
- ↑ K. Fujita, Y. Ohnuma, H. Yasuda, H. Tani: Magnezyum-bütadien ilave bileşikler: İzolasyon, yapısal analiz ve kimyasal reaktivite. İçinde: Organometalik Kimya Dergisi. Cilt 113, Sayı 3, Haziran 1976, s. 201-213, doi: 10.1016 / S0022-328X (00) 87329-5 .
- ↑ Ramsden, HE 63: ABD Patenti 1967, 3,354,190.
- ↑ ilgili kayıt organik magnezyum bileşiklerinin. İçinde: Römpp Çevrimiçi . Georg Thieme Verlag, 26 Mayıs 2014'te erişildi.
- ↑ Franz v. Bruchhausen, Siegfried Ebel, Eberhard Hackenthal, Ulrike Holzgrabe: Hager's Handbook of Pharmaceutical Practice, Cilt 5: Maddeler LZ . Springer-Verlag, 2013, ISBN 978-3-642-58388-9 , s. 86 ( Google Kitap aramasında sınırlı önizleme ).