bakır
| özellikleri | ||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Genel olarak | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| İsim , sembol , atom numarası | Bakır, Cu, 29 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Öğe kategorisi | Geçiş metalleri | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Grup , nokta , blok | 11 , 4 , gün | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Bak | kırmızı-kahverengi, metalik, bakır renkli | |||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS numarası | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| EC numarası | 231-159-6 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| ECHA Bilgi Kartı | 100.028.326 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Dünya kabuğunun kütle kesri | %0.01 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| atomik | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| atom kütlesi | 63.546 (3) u | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Atom yarıçapı (hesaplanmış) | 135 (145) öğleden sonra | |||||||||||||||||||||||||||||||||||||||||||||||||||
| kovalent yarıçap | 132 öğleden sonra | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Van der Waals yarıçapı | öğleden sonra 140 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektron düzenlenişi | [ Ar ] 3 gün 10 4 sn 1 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| 1. İyonlaşma enerjisi | 7..726 380 (4) eV ≈ 745.48 kJ / mol | |||||||||||||||||||||||||||||||||||||||||||||||||||
| 2. İyonlaşma enerjisi | 20..29239 (6) eV ≈ 1 957.92 kJ / mol | |||||||||||||||||||||||||||||||||||||||||||||||||||
| 3. İyonlaşma enerjisi | 36.841 (12) eV ≈ 3 554.6 kJ / mol | |||||||||||||||||||||||||||||||||||||||||||||||||||
| 4. İyonlaşma enerjisi | 57.38 (5) eV ≈ 5 536 kJ / mol | |||||||||||||||||||||||||||||||||||||||||||||||||||
| 5. İyonlaşma enerjisi | 79.8 (7) eV ≈ 7 700 kJ / mol | |||||||||||||||||||||||||||||||||||||||||||||||||||
| fiziksel olarak | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fiziksel durum | sıkıca | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Kristal yapı | Kübik alan merkezli | |||||||||||||||||||||||||||||||||||||||||||||||||||
| yoğunluk | 8.92 g / cm³ (20 ° C ) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Mohs sertliği | 3.0 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| manyetizma | diamanyetik ( Χ m = -9.6 10 -6 ) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Erime noktası | 1357,77 K (1084,62 ° C) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| kaynama noktası | 2868K (2595°C) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| molar hacim | 7.11 · 10 -6 m 3 · mol -1 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Buharlaşma ısısı | 305 kJ / mol | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Füzyon ısısı | 13,3 kJ mol -1 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| ses hızı | 3570 m s -1 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Özgül ısı kapasitesi | 385 J kg -1 K -1 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| iş fonksiyonu | 4.65 eV | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektrik iletkenliği | 58.1 · 10 6 A · V -1 · m -1 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Termal iletkenlik | 400 W m -1 K -1 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| mekanik olarak | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| elastikiyet modülü | 100… 130 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Poisson'ın numarası | 0.34 ... 0.35 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| kimyasal olarak | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| oksidasyon durumları | 1, 2 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Normal potansiyel | 0,340 V (Cu 2+ + 2 e - → Cu) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| elektronegatiflik | 1.9 ( Pauling ölçeği ) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| izotoplar | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Diğer izotoplar için izotopların listesine bakınız . | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| NMR özellikleri | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||
| güvenlik talimatları | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||
| MAK |
İsviçre: 0.1 mg m -3 ( solunabilir toz olarak ölçülmüştür ) |
|||||||||||||||||||||||||||||||||||||||||||||||||||
|
Olabildiğince ve alışılageldiği kadarıyla SI birimleri kullanılır. Aksi belirtilmedikçe, verilen veriler standart koşullar için geçerlidir . | ||||||||||||||||||||||||||||||||||||||||||||||||||||
Bakır ( Latince Cuprum ) a, kimyasal element ile eleman sembolü , Cu ve atom numarası bir olan 29 geçiş metali üzere periyodik tablonun o 4 süresi ve 1 olan bir alt-grubu ya da (yeni sayma grubu 11 sonra) bakır grup . Latince adı cuprum türetilmiştir (aes) Cyprium " cevher Yunan adası Kıbrıs'ta bakır eski zamanlarda mayınlı edildi".
Nispeten yumuşak bir metal olarak bakırın şekillendirilmesi kolay ve serttir. Birçok yönden mükemmel bir ısı ve elektrik iletkeni olarak kullanılır. Ayrıca madeni paralar grubuna da aittir .
Önemli bir teknoloji veya işlevsel metal olarak bakır, yarı değerli bir metaldir .
Tarih

Bakır, altın , gümüş ve kalay , insanlığın gelişimleri sırasında tanıdığı ilk metallerdi . Bakırın işlenmesi kolay olduğu için, yaklaşık 10.000 yıl önce bilinen en eski kültürler tarafından kullanılmıştır . MÖ 5. binyıldan itibaren yaygın kullanımının zamanı. MÖ 3. binyıla kadar M.Ö. bölgeye bağlı olarak Bakır Çağı olarak da adlandırılır . In Hujayrat el-Ghuzlan Ürdün zaten yaklaşık 4.000 M.Ö. yoktu. Bakırın seri üretim yeri. Olarak simya , bakır Venüs ve kadınlık ile ilişkili ♀ ( planet metaller ) ve sülfür ve cıva bir bileşik olarak inceledi. İlk aynalar bu metalden yapılmıştır. Geç Doğu Akdeniz Tunç Çağı boyunca , bakır esas olarak Kıbrıs'ta çıkarıldı ve oradan sığır postu şeklinde çoğunlukla yaklaşık 30 kg ağır bakır çubuklar ( öküz derisi çubuklar olarak adlandırılır ) olarak ihraç edildi . MÖ 16. yüzyıldan 11. yüzyıla kadar Kıbrıs öküz derisi çubuklarının parçaları Akdeniz bölgesinin büyük bir bölümünde, Sardinya'ya kadar, Balkanlar'da ve hatta Alplerin kuzeyinde bulunabilir (Oberwilflingen'de bulunan tortu ). Sanayi öncesi en büyük bakır üreticisi, tahmini yıllık 15.000 ton üretimle Roma İmparatorluğu idi .
Daha sonra bakır, kalay ile alaşımlandı ve bronz oluşturmak için kurşun oldu . Bu daha sert ve teknik olarak daha dayanıklı alaşım Tunç Çağı'na adını vermiştir . Kurşun ve kalay arasındaki ayrım , ancak artan metal bilgisi ile ortaya çıktı, bu nedenle günümüz bakış açısına göre bronz terimi, yalnızca yüksek bakır içeriğine sahip kalay-bakır alaşımlarına doğru bir şekilde uygulandı.
Altın sarısı bakır-çinko alaşımı " pirinç " antik Yunanistan'da zaten biliniyordu . İlgili cevherlerin birlikte işlenmesiyle eritildi, ancak Romalılara kadar bu işlemin giderek daha fazla kullanılması değildi. Alaşım altın-bakır Tumbaga edildi yaygın olarak kullanılan yılında antik Kolombiya .
Mineral olarak bakır
Doğal bakırın doğal oluşumları, yani elemental haliyle, Uluslararası Mineraloji Birliği (IMA) kurulmadan çok önce biliniyordu . Bu nedenle bakır, bağımsız bir mineral türü olarak büyükbaba olarak adlandırılan bir mineral olarak kabul edilir .
Göre Strunz (9. basım) 'e göre mineral sistematiği , bakır bir sistem olarak sınıflandırılmıştır. "1.AA.05" (elementler - metaller ve intermetalik bileşikler - bakır cupalit ailesi - bakır grubu) veya I / A.01 altında sınıflandırılan eski 8. baskıda ( bakır serisi ). Ağırlıklı olarak İngilizce konuşulan ülkelerde kullanılan Dana'ya göre minerallerin sistematiği, mineral elementini sistem no. 01/01/01/03 ( altın grubu ).
Doğada bakır genellikle bazaltik lavlarda ya “bakır kırmızısı”, parlak metalik külçeler (eriyikten katılaşmış) ya da dendritler olarak adlandırılan dallı yapılar şeklinde oluşur . Bazen kristal eğitim de bulunabilir. Bakır meydana parajenezinde çeşitli, çoğu ile ikincil gibi bakır mineralleri bornitte , kalkozin , Kornvalit , Kuprit , azurite ve malakit sıra sıra tenorite değil, aynı zamanda bu gibi pek çok diğer mineraller ile ilişkili olabilir , kalsit , Klinoklaz , prehnit , mineraller içerir , kuvars ve gümüş .
Pseudomorphism bakır ila aragonit
Bakır cevherleri yaygındır. Örneğin, bakır yapılır kalkopirit ( bakır pirit , CuFeS 2 ), kalkozin ( bakır parlaklık , Cu 2 S), daha nadiren de gelen bornitten ( renkli bakır çakıl , Cu 5 FeS 4 ), atacamite (CuCl 2 , Cu (OH) 2 ), malakit (Cu 2 [(OH) 2 | CO 3 ]) ve diğer cevherler. 2019 yılında 636 bakır minerali biliniyordu. Bileşikte en yüksek bakır konsantrasyonuna sahip mineraller kuprit ( % 88.8'e kadar ) ve algodonit ( % 83.6'ya kadar) ile paramelakonit , tenorit ve kalkozindir (%79.9'a kadar).
Oluşum ve çıkarma
Alman Bakır Enstitüsü'ne göre bakır, yerkabuğunda %0,006 civarında bir içerikle oluşur ve yerkabuğundaki elementlerin sıklığı açısından 23. sıradadır. Bakır genellikle katı halde , yani elemental halde bulunur. Dünya çapında (2017 itibariyle) şu anda (2017 itibariyle) Afganistan , Arjantin , Avustralya , Belçika , Bolivya , Brezilya , Bulgaristan , Şili , Çin , Kongo Demokratik Cumhuriyeti , Almanya dahil olmak üzere katı bakır için bilinen 3000'den fazla yer var. , Finlandiya , Fransa , Yunanistan , Hindistan , İran , İrlanda , İtalya , Japonya , Kanada , Kazakistan , Fas , Meksika , Moğolistan , Namibya , Yeni Zelanda , Norveç , Avusturya , Peru , Filipinler , Polonya , Portekiz , Romanya , Rusya , Zambiya , İsveç , İsviçre , Zimbabve , Slovakya , İspanya , Güney Afrika , Çek Cumhuriyeti , Türkiye , Ukrayna , Macaristan , Amerika Birleşik Devletleri (ABD) ve Birleşik Krallık (İngiltere).
Katı bakır da tespit edilebilir birkaç kaya örneklerinde orta Atlantik sırtından ve gelen ayın , hangi sonda getirdi Luna 24 misyon gelen Mare Crisium .
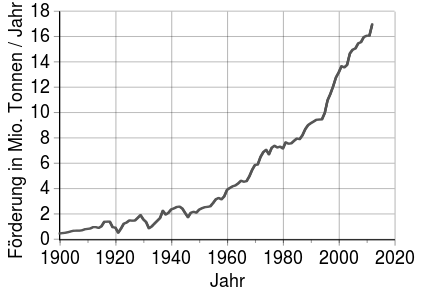
Promosyon ve rezervler
En önemli bakır üreticisi Şili'dir ve onu uzun bir yol kat eden Peru ve Çin izlemektedir. Avrupa'da Polonya , Portekiz ve İsveç dikkat çekicidir. En önemli ihracat ülkeleri, 1967'den 1988'e kadar CIPEC'de organize edildi . CIPEC, 1988'de Bougainville adasında dünyanın en büyük bakır madenlerinden birinin iç savaşa yol açtığı Şili, Peru ve Papua Yeni Gine'yi içeriyordu .
Bakır madenleri Keweenaw Peninsula içinde Lake Superior (ABD) tarihsel olarak anlamlı idi . Orada dünyanın en büyük yerli bakır yatağı vardı. Madencilik orada Kolomb öncesi zamanlarda gerçekleşti. Almanya'da 1990 yılına kadar Mansfeld bölgesinde bakır şeyl madenciliği yapıldı . Diğer tarihi maden sahaları Kupferberg / Yukarı Frankonya (13. yüzyıldan itibaren) ve Aşağı Silezya Kupferberg / Riesengebirge (12. yüzyıldan beri) Cornwall'da (İngiltere) özellikle 18. ve 19. yüzyıllarda önemli bakır madenciliği vardı.
Uluslararası Bakır Çalışma Grubu ICSG'ye göre, Amerika Birleşik Devletleri Jeolojik Araştırmaları'na (USGS) göre bakır rezervleri şu anda 870 milyon ton (Mt) civarındadır. Tanımlanmış ve keşfedilmemiş bakır kaynaklarının sırasıyla yaklaşık 2.100 Mt ve 3.500 Mt, toplam 5.600 Mt olduğu tahmin edilmektedir. İkincisi, derin deniz nodüllerinde ve karada ve denizaltı masif sülfürlerinde bulunan büyük miktarlarda bakırı hesaba katmaz.
| rütbe | ülke | ilerleme | Rezervler |
|---|---|---|---|
| 1 | Şili | 5800 | 170.000 |
| 2 | Peru | 2400 | 83.000 |
| 3 | Çin Halk Cumhuriyeti | 1600 | 26.000 |
| 4. | Amerika Birleşik Devletleri | 1200 | 48.000 |
| 5 | Kongo Demokratik Cumhuriyeti | 1200 | 20.000 |
| 6. | Avustralya | 950 | 88.000 |
| 7. | Zambiya | 870 | 19.000 |
| 8. | Endonezya | 780 | 51.000 |
| 9 | Meksika | 760 | 50.000 |
| 10 | Rusya | 710 | 61.000 |
çıkarma
ham bakır
Bakır ekstraksiyonu için en önemli fırınlar alevli fırın ve 1980'den beri flaş izabe fırınıdır .
Bakır, üretimi için sözde bakır taşı (Cu 2 değişen FeS içeriği ile S ve yaklaşık bir Cu içeriği.% 70), ilk ekstre edilir bakır sülfid (CuFeS dan 2 ) . Bu amaçla hammadde kok ilave edilerek kavrulur ve içerdiği demir oksitler silisli agregalarla cüruflanır . Bu demir silikat cürufu bakır taşı üzerinde yüzer ve böylece kolayca dökülebilir.
- Kavurma işi:
- Eritme işi:
Bu şekilde elde edilen bakır taşı işlenerek ham bakır ( siyah bakır olarak da bilinir ) haline getirilir . Bunu yapmak için bir dönüştürücüye dökülür ve bu eriyik içine hava üflenir. İlk aşamada (cüruf kabarcıkları) içerdiği demir sülfür, demir okside kavrulur ve bu, dökülebilen cüruf oluşturmak için cüruf kuvars ile bağlanır. İkinci adımda (pişirme kabarcıkları) , kalan Cu 2 S'nin üçte ikisi Cu 2 O'ya oksitlenir. Oksit daha sonra kalan sülfür ile reaksiyona girerek ham bakır oluşturur.
- Cüruf kabarcıkları:
- Pişirme baloncukları:
Ham bakırın bakır içeriği %98'dir. Demir ve çinko gibi baz metallerin yanı sıra kalan %2'lik kısım gümüş ve altın gibi değerli metalleri de içermektedir .
arıtma
Elektrolitik arıtma bir bakır içinde gerçekleştirilir bakır (II) sülfat çözeltisi sülfürik asit ihtiva eden bir ham bakır ile anot ve bir saf bakır katot . Elektroliz sırasında, bakırdan daha az soylu olan tüm metaller oksitlenir ve katyon olarak çözeltiye girerken, daha soylu metaller anot çamuru olarak batar.
Elektrolitik arıtmanın reaksiyon denklemi:
- anot
- katot
Anot, katyonların oluşumu ile yavaş yavaş çözünürken, bakır iyonlarının indirgenmesi nedeniyle yalnızca kütle fraksiyonu w (Cu) = %99,99 olan elektrolitik bakır katot üzerinde birikir.
Yan ürün olarak oluşan anot çamuru daha sonra geri dönüştürülür ve değerli metallerin çıkarılması için başlangıç malzemesi olarak hizmet eder.
Bakır rafinerilerde çıkarılır . Avrupa'da, merkezi Hamburg'da bulunan Aurubis AG (eski adıyla Norddeutsche Affinerie) bununla tanınır ve eskiden Duisburger Kupferhütte (bugün DK Geri Dönüşüm ve Pik demir ) idi.
Bakır ayrıca bakır sülfat çözeltisinden demir ile çökeltilerek çimento bakır olarak da elde edilebilir . Çökeltme işlemine sementasyon denir. Elde edilen bakır genellikle kirlenir. Bakırın doğal olarak oluşan metal tuzu çözeltilerinden demir üzerine çökeltilmesi MS 1086'dan beri Çin'de uygulanmaktadır .
Bakır ayrıca bir alüminotermik reaksiyonla da temsil edilebilir . Termit olarak bakır (II) oksit ve alüminyum kum karışımı kullanılır . Bir süper akışkanlaştırıcı (örneğin, kalsiyum florür ) kullanılarak, elde edilen cürufun aksine elementer metaller süper akışkanlaştırıcı içinde çözülemediğinden verim arttırılabilir. Alüminotermik ekstraksiyon, bunun için gerekli olan alüminyum nedeniyle ekonomik değildir.
özellikleri
İyi elektriksel ve termal iletkenlik, bir malzeme olarak bakırın önemli özellikleridir. Bu malzemenin teknoloji için büyük önemi, - bakır alaşımları şeklindeki diğer metallerle bağlantılı olarak - yıllardır kullanılan ve daha da geliştirilen çeşitli iyi özelliklerin kombinasyonundan kaynaklanmaktadır. Ayrıca bakır, mükemmel korozyon direncine sahiptir ve kalite kaybı olmaksızın yüzde 100 geri dönüştürülebilir.
Fiziki ozellikleri

Nedeniyle için yoğunluğu 8920 kg / m, bakır biridir ağır metaller , bir kristalize olur yüzey merkezli kübik bir şekilde ve böylece sahip kübik kürelerin yakın ambalaj ile uzay grubu Fm 3 m (boşluk grubu. 225) . Kristal parametresi saf bakır için 0,3615 olan mil (3.615 karşılık gelir  4) , formül birimi başına birim hücre .
Bakır çok iyi bir ısı iletkenidir . Bu , erime noktası 1083,4 olduğu ° C Bakır da çok iyi bir elektrik iletkeni , bir ile elektrik iletkenliği 58 · 10 6 S / m. Onun iletkenlik sadece biraz daha kötü olduğu gümüş ve önemli ölçüde daha iyi daha altın . Bakırda çözünen tüm katkılar, özellikle fosfor ve demir gibi safsızlıklar iletkenliği büyük ölçüde azalttığından, iletken malzemeler için genellikle en yüksek saflık dereceleri kullanılır ( Cu-ETP , eski E-bakır, %99.9 saflık).
Mohs sertliği bakır karşılık gelen 3'e 2.5 Vickers sertliği 1N bir test kuvveti ile 77-99 arasında (VHN). Tarafından soğuk şekillendirme olan çekme dayanımı 150 MPa ile 200 (yumuşak) bir> 350 MPa artmıştır. Eğer kırılma noktasındaki uzama edilir ile% 5'in altında düşük sertlik değerleri yaklaşık 100 HB . İletkenlik düşer. Deforme olmuş ve ardından yumuşak tavlanmış bakırın kopma uzaması > %40 ve sertlik değerleri 50 HB civarındadır.
Yumuşaklık bakır kısmen yüksek açıklar elektrik iletkenliği ve yüksek ısı iletkenliği olan bir ikinci en yüksek saf arasında metaller de oda sıcaklığında, sonra gümüş . Bunun nedeni, direnç , oda sıcaklığında metal elektron taşıma öncelikli olarak dayanır saçılma arasında elektron sırasında termal titreşimlerinin kafes , nispeten zayıf bir yumuşak metal .
700 ila 800 ° C sıcaklıklarda dövme yapmak çok mümkündür. Ara tavlama yapılmadan soğuk şekillendirme yapılabilir , gerinim sertleşmesi meydana gelir .
Çıplak metal olarak bakır açık kırmızı bir renge sahiptir, çizgi rengi pembe-kırmızıdır. Kırmızı rengini olmasından kaynaklanır emer tamamlayıcı yeşil ve mavi bir ışık biraz daha normale de sıcaklık . Havaya maruz kaldığında kararır ve başlangıçta kırmızı-kahverengiye döner. Daha fazla aşınma ve korozyon ile pürüzsüz yüzey çok yavaş kaybolur (genellikle yüzyıllar boyunca) ve bir patina oluşumu nedeniyle renk kırmızı-kahverengiden mavi-yeşile değişir . Bakır, 200 yılı aşkın teknik "ömrü" olan dayanıklı bir yapı malzemesidir. Bu direnç, atmosferde hava koşullarına dayanıklı, sıkıca yapışan koruyucu bir tabaka oluşturma yeteneğine dayanmaktadır. Bu oksit tabakası, doğası gereği kararlıdır ve "kendi kendini onarır". Bileşiminden bağımsız olarak, daha fazla aşındırıcı saldırılara karşı koruma sağlar.
Bakır, gri veya gümüş dışında doğal bir renge sahip birkaç metalik elementten biridir . Saf bakır yüzeyler somon kırmızısıdır ve havada kırmızımsı kahverengiye döner . Bakırın karakteristik rengi , d atom orbitalinde bulunan elektronların bantlar arası geçişlerinden kaynaklanır .
Diğer metallerde olduğu gibi , galvanik korozyon , bir elektrolit içinde bakır başka bir metalle temas ettirildiğinde meydana gelir . Bu oluşturan yerel elemanlar çinko çok az miktarda bir bileşen olarak, örneğin. Elektrokimyasal seride nispeten asil bir metal olarak , bununla birlikte, genellikle korozyondan etkilenmez.
Kimyasal özellikler
| Bakırın oksidasyon durumları | |
|---|---|
| +1 | CuCl , Cu 2 O , CuH , Cu 2 C 2 |
| +2 | CuCl 2 , CuO , CuSO 4 , bakır (II) asetat |
| +3 | KCuO 2 , K 3 CuF 6 |
| +4 | Cs 2 CUF 6 |
Bakır, 0, +1, +2, +3 ve +4 oksidasyon durumlarında meydana gelir , en yaygın olanları +1 ve +2'dir, +2 sulu çözeltilerde en kararlı oksidasyon durumudur ; Seviye +4 son derece nadirdir (örneğin Cs 2 CuF 6'da ). Bakır (II) tuzları (örneğin bakır sülfat ) genellikle mavi veya yeşil renktedir. Kimyasal olarak bakır, bazı durumlarda aynı grupta bulunan gümüş ve altın elementlerine benzer özelliklere sahiptir . Bir tabaka metalik bakır olduğu bir demir çivi üzerinde biriken daldırma a çözeltisi bakır sülfat olan, demir gider içine çözelti olarak demir sülfat , demir, bakır daha az soylu olması nedeniyle, (bakınız ayrıca gerilim dizi ). Bakır normalde hidroklorik asit tarafından saldırıya uğramaz , ancak oksijen varlığında güçlü bir şekilde saldırıya uğrar , sıcak sülfürik asit tarafından çözülür. Ayrıca nitrik asit ve aqua regia'da çözünür . Bir karışım, hidroklorik asit ya da sülfürik asit , hidrojen peroksit, çok hızlı bir şekilde çözünür bakır. Metal da bir saldırıya ile organik asitler . Alkalilere karşı stabildir. Olarak kırmızı ısı bu oksijen ile reaksiyona girer ve kalın bir tabaka oluşturan bakır oksit . Bakır, flor ve bileşikleri tarafından pasifleştirilir . Tane boyutuna bağlı olarak bakır tozu yanıcı veya yanıcıdır . Metal kompakt bir formda değil, yanıcı ince oluşturulduktan sonra ve oksit tabakasını ve hava ve su temiz hava ve suya karşı, bu yüzden saldırıya maruz dayanıklı .
Gelen sıvı bakır çözülür oksijen ve hidrojen içinde, katılaşma ve eriyik için , su buharı böylece gaz gözeneklilik neden uygulanması ve mümkün döküm şeklinde.
Çatlaklar ve boşluklar oluşabilir içinde oksijen içeren bunlar ile temas haline geldiği zaman, bakır sınıflar hidrojen içeren gazlar , potansiyel olarak bilinen için bakır hidrojen gevrekleşmesine .
biyolojik özellikler
İnsan organizması için bakır temel bir eser elementtir , yani insanların hayatta kalabilmesi için bakıra ihtiyacı vardır. Bir yetişkin için yaklaşık 2 mg'lık günlük gereksinim, genellikle büyük oranda tahıl, et, kök sebzeler, baklagiller, fındık ve hatta çikolata içeren dengeli bir diyet yiyerek sağlanır. Bakır, yerkabuğunda, okyanuslarda, göllerde ve nehirlerde çeşitli form ve konsantrasyonlarda bulunabilen doğal olarak oluşan bir elementtir. Flora ve faunanın yaşamı, bakırın bu doğal varlığı çerçevesinde gelişmiştir. Bu nedenle, çoğu organizma, kullanımları için içsel bir mekanizmaya sahiptir.
Antimikrobiyal özellikler
Bakır, düşük konsantrasyonlarda bile birçok mikroorganizma (virüsler, mikroplar) için toksiktir. Bakırın antimikrobiyal özelliğinden dolayı malzeme z'dir. B. hastanelerde büyük ölçekli deneylerde kullanılır. 2008/2009 tarihli bir klinik çalışma , Hamburg'daki Asklepios Clinic Wandsbek'te , 50 kapı kolu / levhası ve ışık anahtarını değiştirdikten sonra MRSA mikroplarının %63'e düştüğünü gösteriyor. Şili'de yapılan bir araştırma, %7,2 ila %19,7 nemde bakır alaşımlarından yapılmış nesnelerdeki mikrop sayısında %92'ye varan bir azalma olduğunu buldu. Bir çok-merkezli çalışma "bakır oda" enfeksiyon oranı neredeyse% 60 oranında düştüğünü ABD gösterileri 2010/2011 gelen ve bakır nesnelerde mikrop sayısı üzerinden% 80 azaltılmıştır. 2013 yılında, Kuzey Ren-Vestfalya'daki Niederberg Kliniğindeki Çocuk ve Ergen Tıbbı Kliniği, kapı kollarını bakır alaşımlı olanlarla değiştirdi. %60'tan fazla bakır içeren alaşımlar gereklidir. ABD'de çeşitli bakır uygulamalarıyla daha ileri denemeler devam etmektedir.
Deneyler, temasla öldürmenin, metal-bakteri temasının hücre zarına zarar verdiği bir mekanizma ile gerçekleştiğini ve bunun da hücreleri bakırdan daha fazla hasara karşı duyarlı hale getirdiğini göstermektedir. Şu anda çalışma grubu tarafından ISS uzay istasyonunda üç deney var ve bunu birkaç tane daha takip edecek.
Mikrop azaltıcı etki, bakır iyonlarının proteinlerin tiyol gruplarına bağlanması ve hücre zarı lipidlerini peroksit etmesi gerçeğinden kaynaklanır , bu da DNA ve hücre zarlarına zarar veren serbest radikallerin oluşumuna yol açar . İnsanlarda, örneğin Wilson hastalığı (bakır depolama hastalığı) durumunda bu, yüksek bakır fazlalığı ile organ hasarına yol açar.
Bakır içeriği en az %60 olan bakır alaşımları da norovirüslere karşı toksik etki gösterir .
Salyangozlara karşı etki
Nesli tükenmekte olan bitkilere bariyer görevi gören bakır tel veya bakır folyodaki bakır, salyangoz balçıkları tarafından oksitlenir. Bu, salyangozun daha fazla sürünmesini engelleyen tahriş edici bir madde oluşturur.
Biyolojik bakır talebi
Bakır özellikle metabolizma için önemli olduğundan, bakır eksikliği ciddi sağlık sorunlarına yol açabilir. Bakırın sağlığa faydaları sayısızdır, çünkü bakır, hayati enzimlerin ve proteinlerin bir bileşeni olarak birçok vücut fonksiyonunu etkiler: Bakır, bebeklerin büyümesi, kemik gücü, kırmızı ve beyaz kan hücrelerinin olgunlaşması, demir taşınması, kolesterol ve glikoz için gereklidir. metabolizma, Kalp kası kasılması ve beyin gelişimi.
Bir yetişkinin günlük ihtiyacı 1.0–1.5 miligramdır. İnsan vücudunda bakır esas olarak karaciğerde depolanır.
Bakır esas olarak çikolata, karaciğer, tahıllar, sebzeler ve kuruyemişlerde bulunur. Bakır eksikliği insanlarda nadiren görülür. Bir eksiklik esas olarak uzun süreli ishal, erken gelişen çocuklar, uzun süreli yetersiz beslenme veya aşağıdaki gibi hastalıklara bağlı emilim bozukluğundan sonra mümkündür . B. sprue , Crohn hastalığı veya kistik fibroz . Yüksek dozda çinko , demir veya molibdat almak da vücuttaki bakır seviyelerinin düşmesine neden olabilir. Menkes hastalığı bakır metabolizmasının nadir konjenital hastalıktır.
Fazla bakır ve zehirlenme
Fazla bakır, atılım için safra ile sindirim sistemine salınır .
Bakır sülfat (bakır vitriol) güçlü bir kusturucudur ve bu nedenle birçok zehirlenmeyi tedavi etmek için kullanılmıştır , örneğin bu özel durumda fosforun aynı zamanda zayıf çözünür bakır fosfit olarak bağlanması avantajına da sahip olan beyaz fosfordan .
Nadir kalıtsal hastalık Wilson hastalığında , bakırın atılımı bozulur ve önce karaciğerde, daha sonra bakırın kan dolaşımına atılmasıyla diğer organlarda da bakır birikimi artar. Bakır metabolizmasının eşit derecede nadir görülen bir başka hastalığı da Menkes sendromudur . Bakır hücreler tarafından emilebilir, ancak daha sonra artık düzenli bir şekilde taşınamaz, böylece bazı organlarda bakır içeriği artarken diğerlerinde bakır içeriği azalır.
Bakır ve Alzheimer hastalığı
Bakır ve Alzheimer hastalığının gelişimi arasındaki bağlantı tekrar tekrar tartışıldı. 2003 yılında araştırmacılar bakırın amiloid A üretimini yavaşlattığından ve bakır eksikliğinin Alzheimer hastalığını desteklediğinden şüpheleniyorlardı. Bununla birlikte, 70 Alzheimer hastasıyla yapılan sonraki bir pilot çalışma, Alzheimer hastalığının bir hastalık belirteci olan BOS'ta Abeta42'deki düşüşte bir stabilizasyon olsa bile, artan bakır alımından herhangi bir koruyucu etki gösteremedi .
Diğer çalışmalar, bakırın beyne zararlı olabileceğini gösterdi . Alzheimer hastalığına karşı aktif bir bileşen olarak iyonofor PBT2 ile yapılan bir çalışma , bir faz II çalışmasında iyi sonuçlar verdi. Aktif bileşen sadece çinkoyu değil aynı zamanda bakırı da bağlar ve böylece beyindeki bakır konsantrasyonunu azaltır.
Yeni bir çalışma, bakırın uzun süreli yüksek alımla beyin kılcal damarlarında biriktiğini ve buradaki kan-beyin bariyerine zarar verebileceğini gösteriyor. Bu beta-amiloidin uzaklaştırılmasını engeller , maddenin birikmesi daha sonra Alzheimer hastalığına neden olur .
kullanmak

Bakır, özellikle mükemmel elektriksel ve termal iletkenliği nedeniyle ve aynı zamanda mükemmel işlenebilirliği ve uzun ömürlülüğü nedeniyle, çok sayıda uygulamada ve otomotiv veya makine mühendisliği gibi birçok farklı endüstride saf veya alaşım olarak kullanılır . Yenilenebilir enerjiler de artık önemli bir uygulama alanıdır (anahtar kelime: yeşil bina). Buna telekomünikasyon, mimari, geleneksel enerjiler, sıhhi tesisat, ısıtma, trafik, denizcilik uygulamaları, elektrik mühendisliği (örneğin elektrik tesisatı ), hassas parçalar, madeni paralar , çatal bıçak takımı , sanat objeleri, müzik aletleri ve çok daha fazlası gibi alanlar da dahildir .
Diğer metallerle temas halinde kullanılırsa neme maruz kaldığında temas korozyonuna yol açar .
Gümüşten sonra bakır, altından önce tüm maddeler arasında en yüksek ikinci elektrik iletkenliğine sahiptir ve bu nedenle a'dır. için kullanılır:
- küçük kesitli elektrik hatları , atlama telleri ve güç kabloları , havai hatlar
- Baskılı devre kartlarında ve kısmen entegre devrelerde iletken yolları
- Elektrikli makineler: transformatörlerdeki tel sargılar , bobinler / bobinler ve elektrik motorları
- Bileşenler: magnetronların anot gövdeleri , kelepçeler , bileşen bağlantı ayakları, kontak taşıyıcılar, sıkıştırma manşonları
Alüminyumun daha ucuz olduğu ve uzunluk başına kütle açısından bakırdan daha iyi bir elektrik iletkeni olduğu doğrudur. Ama daha hacimli. I.a. Bu nedenle ve ayrıca bakırla daha iyi temas edilebilmesi ve daha yüksek eğilme yorulma mukavemetine sahip olması nedeniyle, ağırlık veya fiyatın önemli olduğu durumlar dışında genellikle alüminyuma iletken olarak tercih edilir.
Oksijensiz Bakır ( OFC , oksijensiz bakır için İngilizce, >% 99,99 saflığa sahip) olarak adlandırılan teller ve şeritler çok ince taneli bir kristal yapıya ve özellikle yüksek yorulma mukavemetine sahiptir. Yüksek mekanik strese maruz kalan kablolar ve teller için kullanılırlar.
Havai hatlar için bakır ve magnezyum alaşımları kullanılır. Artan çekme mukavemeti ile azalan iletkenlik arasında bir uzlaşma bulunmalıdır.
Bakır, yüksek olan bir yansıtma olarak kızıl ötesi ve bu nedenle bir aynası olarak kullanılan karbondioksit lazer ışınları ve kaplanması için cam ( yalıtım camı ).
Yüksek ısıl iletkenliği ve korozyon direnci nedeniyle, ısı eşanjörleri , ısı alıcılar ve güç yarı iletkenleri için montaj plakaları için bir malzeme olarak çok uygundur . Genellikle gastronomide tencere olarak kullanılır .
Gelen sanatlar , bakır levha olan tahrik nedeniyle yumuşaklığı için kolaylıkla mümkündür çekiçleme, deforme olduğu,. Güzel sanatlarda bakır, bakır levha gravürler ve gravürler için baskı levhaları üretmek için hala kullanılmaktadır .
Çatılar ayrıca çeşitli temel bakır hidroksitler veya bakır karbonatlardan oluşan kalıcı yeşilimsi bir patina oluşturan bakır levha ile kaplanır . Genellikle yanlış bir şekilde "verdigris" (bakınız bakır asetat ) olarak adlandırılan bu patina, altındaki metali daha fazla korozyona karşı korur , böylece bakır çatıların birkaç yüzyıllık bir ömrü olabilir. Geleneksel arduvaz çatılarda bakır çiviler kullanılmaktadır . Bakır, estetik nedenlerle de çatılar ve cepheler için giderek daha fazla kullanılmaktadır.
Alaşımlar
Bakır ayrıca aşağıdakiler gibi 400'den fazla alaşımın bir bileşenidir. B. pirinç (çinko ile), bronz (kalay ile) ve nikel gümüşü (çinko ve nikel ile). Bu bakır alaşımları , renk, korozyon direnci ve işlenebilirlik gibi iyi özelliklerinden dolayı yaygın olarak kullanılmaktadır. Dövme alaşımlar (pirinç ve nikel gümüş) ve döküm malzemeler ( tunç , bronz) arasında bir ayrım yapılır : Dövme alaşımlar, plastik şekillendirme (sıcak şekillendirme: haddeleme, dövme vb.) veya soğuk şekillendirme: tel çekme, çekiçleme, soğuk haddeleme, derin çekme vb.), döküm malzemelerin plastik olarak şekillendirilmesi genellikle zor veya imkansızdır.
Nikel ilavesine bağlı olarak bakırın kendi rengi kaybolur ve sarımsı ila beyaz korozyona dayanıklı alaşımlar ( bakır-nikel ) oluşur.
Birçok madeni para malzemesi bakır bazında yapılır, bu nedenle euro madeni paraların " İskandinav altını " olarak adlandırılan altın renkli kısımlarının metali bir bakır-çinko-alüminyum-kalay alaşımıdır. 2001 yılına kadar geçerli olan 1 DM madeni paraların madeni para metalleri ve euro madeni paraların açık renkli kısımları cupronickel alaşımlarından oluşmaktadır .
Bakır bileşikleri renk pigmentlerinde , toner olarak , tıbbi müstahzarlarda ve galvanik yüzey kaplamalarında kullanılmaktadır.
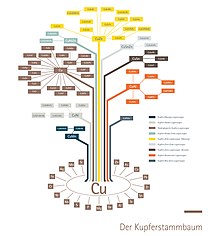
Alman Bakır Enstitüsü'nün bakır aile ağacı, farklı alaşım ailelerine genel bir bakış sunar.
kanıt
Bakır , oksitleyici alev bölgesindeki boraks incisini maviden mavi-yeşile boyar, azaltıcı alev bölgesinde renk değişikliği fark edilmez veya inci kırmızıdan kırmızı-kahverengiye boyanır. Klasik katyon ayırma işleminde bakır, hidrojen sülfür grubunda çökeltilir ve orada bakır grubunda mavi bir kompleks olarak algılanır. İkinci renk, bakır (II) iyonlarının amonyak ile çözeltilerinin koyu mavi bir bakır tetrammin kompleksi , [Cu (NH 3 ) 4 ] 2+ oluşturması gerçeğine dayanır (ayrıca bkz . kompleks oluşum reaksiyonu ).
Bir potasyum hekzasiyanoferrat (II) çözeltisi tortular bakır (II) iyonları, bakır (II) hekzasiyanoferrat (ll), Cu 2 [Fe (CN) 6 ]. Bu algılama reaksiyonu çok hassastır; yani, aynı zamanda düşük bakır seviyelerine de işaret eder.
Bakır tuzları alevi (Bunsen brülör alevi) yeşilden maviye ( alev rengi , spektral analiz ) renklendirir .
Kantitatif belirlenmesi ile gerçekleştirilebilir Elektrogravimetri bir ile platin örgü katot sülfürik asit, bakır (II) ihtiva eden bir çözeltiden. Bakır, iyodometri veya kompleksometri ( Titriplex ile titrasyon / indikatör mureksit ile komplekson III) ile boyutsal olarak belirlenebilir . Gelen izi alanı olan Differenzpulspolarographie kullanılabilir (potansiyel -0.62 V genel yarım dalga SCE 1 M tiosiyanat solüsyonu). Ultra bakır izleri , ters voltametri , grafit tüp AAS veya ICP-MS aracılığıyla belirlenir .
Bakır (II) iyonları , zayıf alkali bir çözelti içinde kuprizon (oksalik asit bissikloheksiliden hidrazit ) ile mavi bir kompleks oluşturur .
bağlantılar
Oksitler ve hidroksitler
Bakır (I) oksit kırmızı ve bir sahiptir kübik kristal yapısı ile uzay grubu Pn 3 m (boşluk grubu no. 224) . Bu şekilde kullanılan pigment olarak cam , seramik , emaye , porselen, sır ve bir şekilde optik cam cila , insektisit , katalizör için amonyak üretimi , çözücü için krom, demir cevheri olarak, galvanik elektrot olarak, piroteknik , bulut oluşumu , korozyon inhibitörleri , galvanizleme işlemler , elektronik , tekstil , alev geciktirici olarak , yakıt katkı maddesi olarak , kirlilik kontrolünde kullanılan katalizör, baskı ve fotokopi ve ahşap koruyucu olarak .
Bakır (II) oksit , bir siyah, şekilsiz veya kristal halinde bir katı ve formları monoklinik kristal yapı ile boşluk grubu C 2 / C (boşluk grubu no. 15) . Seramik endüstrisinde cam , sır ve emayelerin mavi, yeşil veya kırmızı renklendirilmesinde kullanılır . Bazen hayvan beslenmesinde bakır eksikliğine karşı koruma sağlamak için mineral katkı maddeleri eklemek için kullanılır . Diğer uygulamaları , kağıt hamuru endüstrisi için çözümlerin hazırlanmasını içerir .
Bakır (II) hidroksit , mavi ve kullanılan üretim ve hamuru , pil elektrotları kullanılır ve diğer bakır tuzlarıdır. Bu olarak kullanılan işleme maddesi olarak boyamada bir şekilde, pigment ve yem katkı maddesi kızılcık depolama çürümesinin tedavisinde ve olarak, mantar öldürücü marul, şeftali, kızılcık ve ceviz bakteriyel zayıf noktaları karşı.
Halideler
Bakır (II) klorür , kahverengi, oldukça higroskopik bir tozdur. Bu şekilde kullanılan bir katalizör için , organik ve inorganik reaksiyonlar , mordanlama için boyama ve baskı bölgesinin tekstil , pigment için cam ve seramik , ahşap koruyucu , dezenfekte edici , insektisit , fungisit ve herbisit olarak, hem de katalizör , üretim ve klor arasından hidrojen klorür kullanılır . Bakır (II) klorür dihidrat (CuCl 2 · 2 H 2 O) mavi-yeşil bir katıdır .
Bakır (I) klorür beyaz bir sahiptir kristal yapısını çinko blend olan tip boşluk grubu F 4 3 m (boşluk grubu no. 216) . Birçok organik reaksiyon için katalizör olarak kullanılır . Amonyak çözeltileri bakır (I) klorür saflaştırmak için kullanılan gazlar gelen karbon monoksit .
Diğer inorganik bileşikler
Bakır sülfat doğal olarak kalkantit (bakır sülfat pentahidrat, Cu [SO 4 ] · 5H 2 O) ve kabinit (bakır sülfat heptahidrat, Cu [SO 4 ] · 7H 2 O) olarak oluşur. Bunun için kullanılan koruma için derilerin tabaklama ve deri için, üretim için, bakır tuzları koruyucu pulpwood ve öğütülmüş odun hamuru alglerin büyümesini mücadele etmek için, durgun su . Ayrıca elektrokaplama solüsyonlarında , yıkama ve metal işaretleme boyalarında, petrol rafinerilerinde , piroteknikte ve diğer birçok endüstriyel uygulamada kullanılmaktadır.
Organik bileşikler
Bakır (II) asetat (verdigris) koyu yeşil kristaller oluşturur . Bu şekilde kullanılan mantar öldürücü , katalizör için organik reaksiyonlar , pigment için seramik , insektisit , kalıp inhibitörü , koruyucu için selülozik malzemeler , stabilizatör için poliüretanlar ve naylon , korozyon önleyici ve yakıt katkı maddesi.
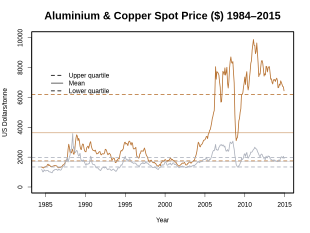
Fiyat geliştirme
Bakır nispeten pahalı bir metaldir. Fiyatı büyük ölçüde dünyanın önde gelen emtia borsalarına ve emtia vadeli işlem borsalarına dayanmaktadır . Londra Metal Borsası (LME) , bakır ticaretinde liderdir .
Dünya piyasa fiyatı bakır için güçlü tabidir dalgalanmalar : LME bakır fiyatı hala ne zaman kurulduğu 2008 yılında büyük dalgalanmalar biri deneyimli ticareti 8940 geçici yüksek seviyesinde USD / t 2 Temmuz tarihinde 2008 ve at onun 23 Aralık 2008'e kadar en yüksek seviye olan 10 yılın en düşük seviyesi 2.825 dolara düştü. Daha sonra, bakır fiyatı 15 Nisan 2009'a kadar 4 aydan kısa bir sürede toparlanarak 4.860 USD/t oldu. Bakır fiyatı 14 Şubat 2011'de 10.180 USD/t ile 10 yılın en yüksek seviyesine ulaştı.
Mart 2012'den Mart 2013'e kadar bakır fiyatı 2 Nisan 2012'de 8.619.75 USD'ye ve 2 Ağustos 2012'de 7.288.25 USD'ye yükseldi. Benzer bir aralık da Ekim 2012 ile Mart 2013 arasında 8.350 USD/ton ile 7.577 USD/ton arasında bulundu.
Ağustos 2014'te bakır için dünya piyasa fiyatı 7000 USD/ton civarındaydı. O zamanki döviz kuruna göre bu 5,931 EUR/t idi.
Bakırın yüksek fiyatı da bakır içeren eşyaların çalınmasında artışa neden oluyor . Demiryollarından gelen topraklama kabloları özellikle etkilenir. Örneğin, Deutsche Bahn AG, 2015 yılında yaklaşık 14 milyon Euro zarara uğradı.
Yakın tarihin en büyük mali skandallarından biri Sumitomo olayıdır . Bakır ticaretine dayanıyordu. Keşif sonucunda bakır fiyatı 1996 yılında bir gün içinde %27 oranında düştü.
Edebiyat
- Harry H. Binder: Kimyasal elementler sözlüğü - gerçekler, rakamlar ve verilerdeki periyodik tablo. S. Hirzel Verlag, Stuttgart 1999, ISBN 3-7776-0736-3 .
- JW Howard: Bakırın hikayesi . İçinde: Kimya Eğitimi Dergisi . bant 6 , hayır. 3 , 1929, s. 413-431 , doi : 10.1021/ed006p413 ( PDF ).
İnternet linkleri
- Mineral atlası: bakır (veri), mineral atlası: mineral portresi / bakır (tarih, ergitme vb.)
- deutschlandfunk.de , Das Feature , 18 Temmuz 2017, Michael Faulmüller: Copper - Element of Discord: A Story of Eternal Struggle
- kupfer-institut.de (Alman Bakır Enstitüsü DKI)
- Londra Metal Borsası , lme.com: Bakır Fiyatı
Uyarılar
- ↑ Özellikler (bilgi kutusu) değerleri aksi belirtilmedikçe www.webelements.com (bakır) adresinden alınmıştır.
Bireysel kanıt
- ↑ a b Harry H. Binder: Kimyasal elementler sözlüğü. S. Hirzel Verlag, Stuttgart 1999, ISBN 3-7776-0736-3 .
- ↑ CIAAW, Standart Atom Ağırlıkları Revize 2013 .
- ↑ a b c d e Kramida, A., Ralchenko, Yu., Reader, J. ve NIST ASD Ekibinde bakır girişi (2019): NIST Atomic Spectra Database (ver. 5.7.1) . Ed.: NIST , Gaithersburg, MD. doi : 10.18434 / T4W30F ( https://physics.nist.gov/asd ). 11 Haziran 2020'de alındı.
- ↑ bir b c d e üzerine kayıt bakır en WebElements, https://www.webelements.com , 11 Haziran 2020 tarihinde erişilebilir.
- ^ NN Greenwood, A. Earnshaw: Elementlerin Kimyası. 1. baskı. VCH, Weinheim 1988, ISBN 3-527-26169-9 , sayfa 1509.
- ↑ Robert C. Weast (ed.): CRC Handbook of Chemistry and Physics . CRC (Kimyasal Kauçuk Yayıncılık Şirketi), Boca Raton 1990, ISBN 0-8493-0470-9 , s. E-129 ila E-145. Oradaki değerler g/mol bazında olup cgs biriminde verilmiştir. Burada verilen değer, ölçü birimi olmaksızın ondan hesaplanan SI değeridir.
- ↑ a b Yiming Zhang, Julian RG Evans, Shoufeng Yang: El Kitaplarında Elemanların Kaynama Noktaları ve Buharlaşma Entalpileri için Düzeltilmiş Değerler. İçinde: Kimya ve Mühendislik Verileri Dergisi. 56, 2011, sayfa 328-337, doi: 10.1021 / je1011086 .
- ^ A. Kayıp: Bakır. İçinde: Ullmann'ın Endüstriyel Kimya Ansiklopedisi. Wiley-VCH Verlag, Weinheim 2005, doi : 10.1002 / 14356007.a07_471 .
- ↑ Ludwig Bergmann, Clemens Schaefer, Rainer Kassing: Deneysel Fizik Ders Kitabı. Cilt 6: Katılar. 2. Baskı. Walter de Gruyter, 2005, ISBN 3-11-017485-5 , s. 361.
- ^ Buildingmaterials.de: Bakır ( Memento 15 Kasım 2009 yılında Internet Archive )
- ^ Münih Teknik Üniversitesi Mimarlık Fakültesi'nin yapı malzemeleri koleksiyonu: Metaller - Bakır .
- ↑ Glyconet ( sayfa artık mevcut değil , web arşivlerinde arama yapın ) Bilgi: Bağlantı otomatik olarak kusurlu olarak işaretlendi. Lütfen bağlantıyı talimatlara göre kontrol edin ve ardından bu uyarıyı kaldırın. .
- ↑ bir b C ile Girdi bakır içinde arasında GESTIS madde veritabanı İFA 25 Nisan 2017 tarihinde erişilebilir. (JavaScript gerekli)
- ↑ İsviçre Kaza Sigortası Fonu (Suva): Sınır değerler - mevcut MAK ve BAT değerleri ( bakır ve inorganik bileşikleri için arama ), 4 Mart 2020'de erişildi.
- ^ Wilhelm Hassenstein: The Fireworks Book of 1420. 600 yıllık Alman barut silahları ve silah ustalığı. Standart Almancaya çeviri ve açıklamalarla birlikte 1529 tarihli ilk baskının yeniden basımı, Münih 1941, s. 104.
- ↑ Öküz derisi çubukları , bunların dağılımı ve Tunç Çağı bakır ticareti için bkz.: Serena Sabatini: Geç Tunç Çağı öküz derisi külçelerini yeniden ziyaret etmek. Anlamlar, sorular ve bakış açıları. İçinde: Ole Christian Aslaksen (Ed.): Doğu Akdeniz'de hareketlilik üzerine yerel ve küresel perspektifler (= Atina'daki Norveç Enstitüsünden Makaleler ve Monograflar, Cilt 5). Atina'daki Norveç Enstitüsü, Atina 2016, ISBN 978-960-85145-5-3 , s. 15-62 .
- ↑ Sungmin Hong, Jean-Pierre Candelone, Clair C. Patterson, Claude F. Boutron: Grönland Buzunda Kaydedilen Roma ve Ortaçağ Zamanlarında Antik Bakır Eritme Kirliliğinin Tarihi. İçinde: Bilim . Cilt 272, No. 5259, 1996, sayfa 246-249 (247, Şekil 1 ve 2; 248, Tablo 1)
- ↑ IMA / CNMNC Mineral İsimleri Listesi; Temmuz 2019 (PDF 1.67 MB; bakır bkz. s. 44)
- ↑ IMA / CNMNC Mineral İsimleri Listesi - Bakır (İngilizce, PDF 1.8 MB, s. 64)
- ↑ Webmineral - Yeni Dana sınıflandırmasına göre düzenlenmiş mineraller. 01/01/01 Altın grubu
- ^ Bakır . İçinde: John W. Anthony, Richard A. Bideaux, Kenneth W. Bladh, Monte C. Nichols (Ed.): Handbook of Mineralogy, Mineralogical Society of America . 2001 ( handbookofmineralogy.org [PDF; 58 kB ; 22 Ocak 2018'de erişildi]).
- ^ Mineral Atlası: Bakır
- ↑ Webmineral - Cu (Bakır ) elementine göre sıralanmış Mineral Türleri .
- ↑ Alman Bakır Enstitüsü - Bakır Bulunabilirliği
- ↑ a b Mineralienatlas ve Mindat'ta katı bakırın bulunduğu yerlerin listesi
- ↑ Springer: Kupferberg, Paul Zsolnay-Verlag, Viyana, 2019.
- ↑ Dünya Mirası Cornish Madencilik ( İnternet Arşivinde 17 Şubat 2011 tarihli orijinalin hatırası ) Bilgi: Arşiv bağlantısı otomatik olarak eklendi ve henüz kontrol edilmedi. Lütfen orijinal ve arşiv bağlantısını talimatlara göre kontrol edin ve ardından bu uyarıyı kaldırın. .
- ↑ ICSG (Ed.): World Copper Fact Book 2020 .
- ↑ Amerika Birleşik Devletleri Jeolojik Araştırması: Dünya Maden Üretimi ve Rezervleri
- ↑ Sayfa artık mevcut değil , web arşivlerinde arama yapın: bakır ve ondan yapılan ürünler .
- ↑ TN Akciğer: Demir üzerinde bakır sementasyonun tarihi - Ortaçağ Çin'inden dünyanın ilk hidrometalurjik süreci. İçinde: Hidrometalurji . Cilt 17, Sayı 1, Kasım 1986, sayfa 113-129; doi: 10.1016 / 0304-386X (86) 90025-3 .
- ^ Ralph WG Wyckoff: Kristal Yapılar . 2. Baskı. bant 1 . John Wiley & Sons, New York, Londra, Sidney 1963, s. 3 ( ekte ).
- ^ Hugo Strunz , Ernest H. Nikel : Strunz Mineralojik Tabloları. Kimyasal-yapısal Mineral Sınıflandırma Sistemi . 9. baskı. E. Schweizerbart'sche Verlagbuchhandlung (Nägele ve Obermiller), Stuttgart 2001, ISBN 3-510-65188-X , s. 34 .
- ↑ H. Keller, K. Eickhoff: Kuper ve Copper Alloys, Springer-Verlag 2013, 54 sayfa, sayfa 7
- ↑ George L. Trigg, Edmund H. Immergut: Uygulamalı Fizik Ansiklopedisi , Cilt 4: Diamanyetizmaya Yanma. VCH Publishers, 1992, ISBN 978-3-527-28126-8, s. 267-272 (2 Mayıs 2011'de erişildi).
- ^ Mimarlık - Alman Bakır Enstitüsü. 12 Temmuz 2021'de alındı (Almanca).
- ^ William Chambers, Robert Chambers: Chambers'ın Halk için Bilgilendirmesi , 5. Baskı, Cilt L, W. & R. Chambers, 1884, ISBN 978-0-665-46912-1 , s. 312.
- ^ Galvanik Korozyon . İçinde: Korozyon Doktorları . 29 Nisan 2011 alındı.
- ^ Siegen Üniversitesi: Metallerin hidroklorik asit ile reaksiyonu .
- ↑ Konuyla ilgili gerçekler - sülfürik asit ( 8 Mart 2001 tarihli İnternet Arşivinde Hatıra )
- ^ Siegen Üniversitesi: Metallerin nitrik asit ile reaksiyonu .
- ↑ eLexicon kimyası: bakır klorür .
- ↑ Denise Herzog: Bakırın insan vücudundaki önemi: kısa bir genel bakış . In: Beslenme tıbbı için İsviçre dergisi . Hayır. 1/10 .
- ↑ Jens Oliver Bonnet: Mikroplara karşı bakır: Beklentiler aşıldı. Asklepios Kliniken Hamburg GmbH, Informationsdienst Wissenschaft'tan (idw-online.de) 16 Haziran 2009 tarihli basın açıklaması, 15 Eylül 2015'te erişildi.
- ↑ Mikrop öldürücü bakır - "güncel bilgi: hücre korsanlarının gücü" konusu .
- ↑ günlük klinik pratikte geldi mi? Antimikrobiyal inşaat malzemeleri katı bakır dayalı , üzerinde krankenhaushygiene.de
- ↑ https://www.amcopper.com/
- ↑ Salima Mathews, Michael Hans, Frank Mücklich, Marc Solioz: Bakteriyel-Metal Teması Önlenirse ve Bakır İyonları Tarafından Demir Üzerinde İndüklenirse, Bakterilerin Bakır Üzerinde Temas Öldürmesi Bastırılır . İçinde: Uygulamalı ve Çevresel Mikrobiyoloji . bant 79 , hayır. 8 Nisan 2013.
- ↑ A. Ala, AP Walker, K. Ashkan, JS Dooley, ML Schilsky: Wilson hastalığı. İçinde: Lancet . Cilt 369, Sayı 9559, Şubat 2007, s. 397-408, doi: 10.1016 / S0140-6736 (07) 60196-2 . PMID 17276780 .
- ^ SL Warnes, CW Keevil: Norovirüsün kuru bakır alaşımlı yüzeylerde etkisiz hale getirilmesi. İçinde: PLoS One. 8 (9), 2013, e75017. PMID 24040380 , PMC 3767632 (ücretsiz tam metin, PDF).
- ↑ ratschlag24.com: Salyangoz vebasına karşı bakır tel . ( Memento Nisan 11, 2013 archive.today web arşivinden ) 17 Mart 2008.
- ↑ sat1.de: yayın 24: akıllı! - Bilgi defteri ( Memento 26 Mayıs 2011 dan Internet Archive ).
- ↑ med.de: on Entry bakır 23 Şubat 2013 tarihinde erişilen.
- ↑ a b Merck Kılavuzu: Bakır .
- ↑ JF Mercer: Menkes sendromu ve hayvan modelleri. İçinde: Amerikan klinik beslenme dergisi. Cilt 67, Sayı 5 Ek, Mayıs 1998, s. 1022S-1028S. PMID 9587146 . (Gözden geçirmek).
- ↑ S. Lutsenko, NL Barnes ve diğerleri: İnsan bakır taşıyan ATPazların işlevi ve düzenlenmesi. İçinde: Fizyolojik incelemeler . Cilt 87, sayı 3, Temmuz 2007, s. 1011-1046, doi: 10.1152 / physrev.00004.2006 . PMID 17615395 . (Gözden geçirmek).
- ↑ TA Bayer: Diyet Cu, APP23 transgenik farelerde beyin süperoksit dismutaz 1 aktivitesini stabilize eder ve amiloid Ap üretimini azaltır. İçinde: Ulusal Bilimler Akademisi Bildiriler Kitabı. 100, 2003, sayfa 14187-14192, doi: 10.1073 / pnas.2332818100 .
- ↑ Holger Kessler, Frank-Gerald Pajonk , Daniela Bach, Thomas Schneider-Axmann, Peter Falkai, Wolfgang Herrmann, Gerd Multhaup, Jens Wiltfang, Stephanie Schäfer, Oliver Wirths, Thomas A. Bayer: Hastalarda bakır alımının BOS parametreleri üzerindeki etkisi hafif Alzheimer hastalığı: bir pilot aşama, 2 klinik deneme. İçinde: Sinir İletimi Dergisi. 115, 2008, sayfa 1651-1659, doi: 10.1007 / s00702-008-0136-2 .
- ^ NG Faux, CW Ritchie, A. Gunn, A. Rembach, A. Tsatsanis, J. Bedo, J. Harrison, L. Lannfelt, K. Blennow, H. Zetterberg, M. Ingelsson, CL Masters, RE Tanzi, JL Cummings, CM Herd, AI Bush: PBT2, Alzheimer Hastalığında bilişi hızla geliştirir: ek faz II analizleri. İçinde: Alzheimer hastalığı Dergisi: JAD. Cilt 20, Sayı 2, 2010, sayfa 509-516, doi: 10.3233 / JAD-2010-1390 . PMID 20164561 .
- ↑ I. Singh, AP Sagare, M. Coma, D. Perlmutter, R. Gelein, RD Bell, RJ Deane, E. Zhong, M. Parisi, J. Ciszewski, RT Kasper, R. Deane: Düşük seviyelerde bakır kesintisi üretimini ve klirensini değiştirerek beyin amiloid-β homeostazı. İçinde: Ulusal Bilimler Akademisi Bildiriler Kitabı. S., doi: 10.1073 / pnas.1302212110 .
- ↑ Deutsches Kupferinstitut: Bakır ve uygulamaları ( bir Memento orijinal web arşivi Temmuz 16, 2012 tarihinden itibaren archive.today ) Bilgi: arşiv bağlantısı otomatik olarak takılmış ve henüz kontrol edilmedi. Lütfen orijinal ve arşiv bağlantısını talimatlara göre kontrol edin ve ardından bu uyarıyı kaldırın. .
- ↑ Bakır alaşımları. 12 Temmuz 2021'de alındı .
- ^ R. Neeb: Ters polarografi ve voltametri. Akademie-Verlag, Berlin 1969, s. 185–188.
- ↑ a b Georg Brauer (Ed.), Marianne Baudler ve diğerlerinin işbirliğiyle : Handbook of Preparative Inorganic Chemistry. 3., gözden geçirilmiş baskı. Cilt II, Ferdinand Enke, Stuttgart 1978, ISBN 3-432-87813-3 , s. 979.
- ↑ a b c d Ulusal Kirletici Envanteri: Bakır ve bileşikleri
- ↑ Georg Brauer (Ed.), Marianne Baudler ve diğerlerinin işbirliğiyle : Handbook of Preparative Inorganic Chemistry. 3., gözden geçirilmiş baskı. Cilt II, Ferdinand Enke, Stuttgart 1978, ISBN 3-432-87813-3 , s. 973.
- ↑ Bakır ticaretinde lider: London Metal Exchange - LME Copper . Erişim tarihi: 15 Mart 2013.
- ↑ Bir b c 15 Nisan 2009 2 Temmuz 2008 döneminde Londra Metal Borsası'nda bakır fiyatının Geliştirme ( içinde Memento orijinal Ağustos 12, 2014 İnternet Arşivi ) Bilgi: arşiv bağlantısı otomatik olarak yerleştirilmiştir ve henüz kontrol edilmedi. Lütfen orijinal ve arşiv bağlantısını talimatlara göre kontrol edin ve ardından bu uyarıyı kaldırın. Kaynak: Handelsblatt veritabanı. 15 Mart 2013 alındı.
- ↑ Londra Metal Borsası'nda son 10 yılın en yüksek bakır fiyatı 14 Şubat 2011 Kaynak: Handelsblatt. 15 Mart 2013 alındı.
- ↑ Londra Metal Borsası'nda son 12 ayda bakır fiyatının gelişimi Kaynak: Handelsblatt. Erişim tarihi: 15 Mart 2013.
- ↑ Londra Metal Borsası'nda son 6 ayda bakır fiyatının gelişimi Kaynak: Handelsblatt. Erişim tarihi: 15 Mart 2013.
- ↑ Bakırın Londra Metal Borsası'ndaki güncel fiyatı ( İnternet Arşivinde 12 Ağustos 2014 tarihli orijinal hatıra ) Bilgi: Arşiv bağlantısı otomatik olarak eklendi ve henüz kontrol edilmedi. Lütfen orijinal ve arşiv bağlantısını talimatlara göre kontrol edin ve ardından bu uyarıyı kaldırın. Kaynak: Handelsblatt.
- ↑ Bu rakam şu şablonla belirlenmiştir : Döviz kuru.
- ^ Deutsche Bahn'da demir dışı metal hırsızlığı . (Artık mevcut çevrimiçi.) Deutsche Bahn basın ofisi, arşivlenmiş orijinal üzerinde 23 Aralık 2016 ; 22 Aralık 2016 tarihinde erişildi .