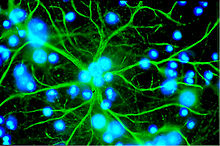
Kan beyin bariyeri
Seçici fizyolojik arasındaki bariyer akışkanlı boşluklarında ve kan akışı ve merkezi sinir sistemi olarak adlandırılır olarak , kan-beyin bariyeri , aynı zamanda , kan-beyin bariyeri , veya kan-beyin bariyeri .
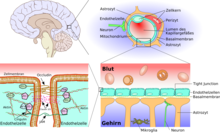
Kanın (intravasküler) beyin ve omurilikteki ekstravasküler boşluktan bu özel sınırı, tüm karasal omurgalılarda (Tetrapoda) geliştirilir ve sinir dokusunun kendi çevresel koşullarını ( homeostaz ) korumasını sağlar . Bu bariyer, esas almaktadır oluşan tarafından endotel hücreleri olan, yakından bağlantılı burada kılcal kan damarları ile sıkı bağlantıları .
Kan-beyin bariyeri, beyni kanda dolaşan patojenlerden , toksinlerden ve haberci maddelerden korur . Beynin ihtiyaç duyduğu besinlerin sağlandığı ve oluşturulan metabolik ürünlerin uzaklaştırıldığı oldukça seçici bir filtreyi temsil eder . Tedarik ve bertaraf, bir dizi özel taşıma süreci ile garanti edilmektedir .
Öte yandan, beynin bu koruyucu işlevi, birçok aktif madde de kan-beyin bariyerini geçemediğinden, çok sayıda nörolojik hastalığın ilaçla tedavisini zorlaştırmaktadır . Kan-beyin bariyerinin geçiş bu hastalıkları tedavi edebilmek için güncel bir araştırma konusudur. Çok az sayıda - çok nadir görülen - hastalıklar doğrudan kan-beyin bariyeriyle ilişkilidir, ancak kendisi önemli ölçüde daha fazla sayıda yaygın hastalıktan etkilenebilir. Kan-beyin bariyerinde bu şekilde meydana gelen bir bozulma veya hasar, çok ciddiye alınması gereken bir komplikasyondur .
Bu engelin varlığını gösteren ilk girişimler 1885'te Paul Ehrlich tarafından gerçekleştirildi . Ancak test sonuçlarını yanlış yorumladı. Kan-beyin bariyerinin son kanıtı 1967'de elektron mikroskobik incelemelerle yapıldı.


Kan-beyin bariyerinin işlevleri
İnsanlarda beyin, vücut kütlesinin yaklaşık% 2'sini oluşturur. Ancak besin maddesi ihtiyacının oranı% 20 civarındadır. Vücuttaki diğer organların aksine, beyin aşırı derecede düşük besin veya oksijen rezervine sahiptir. Sinir hücreleri ayrıca enerji gereksinimlerini anaerobik olarak , yani elementel oksijen olmadan karşılayamazlar . Beyne giden kan beslemesindeki bir kesinti, on saniye sonra bilinç kaybına neden olur ve sinir hücreleri sadece birkaç dakika sonra ölür. Bir beyin bölgesinin aktivitesine bağlı olarak, enerji gereksinimleri ve rezervleri çok farklı olabilir. Tedariki ilgili ihtiyaçlara göre uyarlayabilmek için, bu alanlar kan tedariklerini otomatik olarak düzenler.
Beynin karmaşık işlevleri, oldukça hassas elektrokimyasal ve biyokimyasal süreçlerle bağlantılıdır; bu süreçler, yalnızca sabit bir iç ortam olan homeostat'ta büyük ölçüde müdahale olmaksızın çalışabilir. Örneğin kan pH değerindeki dalgalanmalar beyne geçmemelidir . Potasyum konsantrasyonundaki dalgalanmalar, sinir hücrelerinin zar potansiyelini değiştirir. Kan damarlarında dolaşan nörotransmiterler, buradaki sinapslardaki bilgi akışını önemli ölçüde bozacakları için merkezi sinir sistemine girmemelidir . Ek olarak, ortamdaki dalgalanmanın neden olduğu hasar durumunda nöronlar yenilenemez. Nihayetinde, merkezi olarak kontrol eden bir organ olarak beyin, ksenobiyotikler ve patojenler gibi eksojen maddelerin etkilerinden de korunmalıdır . Kan-beyin bariyerinin kandaki patojenlere , antikorlara ve lökositlere karşı kapsamlı sızdırmazlığı, onu immünolojik bir bariyer haline getirir .
Öte yandan, beynin diğer organlara kıyasla yüksek enerji gereksinimi, ortalamanın üzerinde miktarlarda metabolik parçalanma ürünleri ile sonuçlanır ve bunlar, kan-beyin bariyeri yoluyla tekrar ortadan kaldırılması gerekir.
Tüm bu işlevleri (tedarik, atma ve homeostaz) garanti etmek için , omurgalıların serebral kan damarı sistemi , periferik kan damarı sistemine kıyasla bir dizi yapısal ve işlevsel farklılıklar gösterir . Bu farklılaşma, beynin çevredeki hücre dışı boşluktan büyük ölçüde ayrılmasına neden olur ve hassas sinir dokusunun korunması ve sabit bir iç ortamın sürdürülmesi için çok önemlidir.
Kan-beyin bariyerinin işlevindeki değişiklikler, merkezi sinir sisteminin durumunda değişikliklere neden olur ve bu da CNS'de işlevsel bozukluklara veya hastalıklara yol açabilir. Buna göre, bir dizi nörolojik hastalık, doğrudan veya dolaylı olarak kan-beyin bariyeriyle ilişkilidir.
Kan-beyin bariyerinin anatomisi
Kan-beyin bariyeri temel unsuru olan endotel hücreleri, kendi ile sıkı bağlantıları . Bununla birlikte, diğer iki hücre türü olan perisitler ve astrositler , kan-beyin bariyerinin işlevi ve yapısı ve gelişimi açısından büyük önem taşımaktadır. Endotel hücreleri, perisitler ve astrositler arasındaki hücre-hücre etkileşimleri, diğer hücrelerde olduğundan daha yakındır. Bu üç hücre türü birlikte, çoğu omurgalıda, endotelyal kan-beyin bariyeri olan kan-beyin bariyerini oluşturur . Aşağıdaki anatomik bilgiler, omurgalıların endotelyal kan-beyin bariyeri ile ilgilidir. Bazı omurgalılarda ve birçok omurgasızda gelişen glial kan-beyin bariyeri bu bölümün sonunda ayrı ayrı listelenmiştir.
Endotel
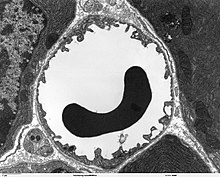
Periferik kan damarlarında olduğu gibi, kılcal damarlar endotel hücreleri tarafından oluşturulur. Periferik kılcal damarların endotelyumunda , kan ve çevreleyen dokunun hücre dışı sıvısı arasında su ve içinde çözünmüş veya asılı madde alışverişi için yaklaşık 50 nm çapında açıklıklar (fenestrasyonlar) ve 0,1 ila 1 µm genişliğinde hücreler arası boşluklar vardır. . Öte yandan, beyindeki endotel hücreleri arasında hiçbir pencere ve hücre içi boşluk yoktur, bu nedenle sürekli bir endotelyumdan söz edilir . Kılcal damarın iç kısmına bakan (lüminal) membran , interstisyuma bakan apikal taraftan membran proteinlerinin türü açısından önemli ölçüde farklılık gösterir .
Sayısı pinositoz veziküller olanak endositoz çözünmüş maddelerin beyin endotel çok azdır.

Aksine, mitokondri sayısı periferik kılcal damarlardakinden yaklaşık 5 ila 10 kat daha fazladır. Bu, aktif taşıma süreçleri için diğer şeylerin yanı sıra, endotelin yüksek enerji ihtiyacının ve yüksek metabolik aktivitenin bir göstergesidir . Kan-beyin bariyeri yalnızca fiziksel değil, aynı zamanda metabolik veya enzimatik bir bariyerdir. Endotelin hücre zarında, örneğin parankim hücrelerinde olduğundan önemli ölçüde daha fazla sayıda enzim vardır . Bunlar, γ-glutamiltransferaz , alkalin fosfataz ve glikoz-6-fosfatazı içerir . Katekol-O-metiltransferaz , monoamin oksidaz veya sitokrom P450 gibi metabolize edici enzimler de nispeten yüksek konsantrasyonlarda endotelde aktiftir. Bu şekilde, birçok madde hücre içi nakilleri öncesinde veya sırasında metabolize edilir. Endotel hücreleri, 0.3 ila 0.5 um'de son derece incedir. Olarak karşılaştırılması, enterositler , epitel hücreleri, bağırsak , önemli ölçüde daha yüksek bir 17 ila 30 um altındadır. Diğer endotelial hücrelerinde olduğu gibi, oranı kolesterol için fosfolipid 0,7 olan. Bu nedenle, hücre zarından geçen saf difüzyon süreçleri, diğer endotelyal hücrelerde olduğu gibi kan-beyin bariyerini aşar. Endotel hücreleri, beynin su dengesinin düzenlenmesi için hücre zarlarında çok sayıda akuaporine sahiptir . Bu kanallar su moleküllerinin hem beyne hem de kana serbestçe dağılmasını sağlar.
Deliklerin olmaması ve pinositotik veziküllerin olmaması, kan-beyin bariyerinin pasif bariyerini temsil eder Bu bariyer etkisi, elektrik direnci aracılığıyla fiziksel olarak ölçülebilir. Sağlıklı bir yetişkin renkli farede direnç 1500 ila 2000 Ω cm² civarındadır. Buna karşılık kas dokusundaki kılcal damarların değeri yaklaşık 30 Ω cm²'dir.
Daha sonra daha ayrıntılı olarak anlatılacak olan endotelin aktif taşıyıcı sistemleri, kan-beyin bariyerinin aktif bariyerini oluşturur.
Sıkı kavşaklar

|
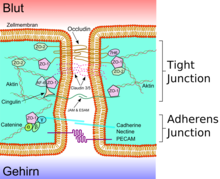
A lümen B apikal taraf C bazal taraf a mukus b apikal taraf c bazolateral yüzey d sıkı bağlantılar f paraselüler boşluk g hücre zarı |
E protein kompleksi 1 okludin 2 Klaudin -1 3 E- kadherin 4 ZO-1 5 JAM-1 6 kateninler 7 cingulin 8 aktin |

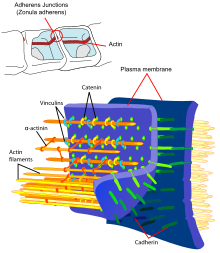
Endotel hücreleri, sıkı bağlantılar adı verilen sıkı hücre-hücre bağlantıları yoluyla birbirine bağlanır . Bu sıkı bağlantılar, komşu hücreler arasındaki yoğun bağlantıları temsil eder ve kan-beyin bariyerinin bariyer işlevine önemli bir katkıda bulunur. Bunun nedeni, hücreler arasındaki boşluğu kapatmaları ve dolayısıyla , komşu endotelyal hücreler arasındaki hücreler arası boşluk boyunca maddelerin geçişini, yani paraselüler taşınmayı pratikte dışlamalarıdır .
Çeşitli transmembran proteinleri gibi, okludin çeşitli klaudin ve birleşme yapışma moleküllerinin (JAM), çevresel protein bantlarının yanal hücre duvarlarının apikal bölgede endotelin bağlantı sıkı bağlantıları ve böylece büyük ölçüde içi boşluk yoluyla paraselüler geçişini önlemek daha büyük moleküller için iki endotel hücresi arasında. Bireysel protein-protein bağlantıları, paralel bağlanmış sigortalar gibi davranır. Kan-beyin bariyerinin endotel hücreleri ifade sadece 5-Klaudin ve Klaudin-12 24 bilinen klaudin arasında. Claudin-5, kan-beyin bariyerinin en önemli hücre yapışma proteini olarak kabul edilir . Kapatma ( gen nakavt ) CLDN5 geni, kodlar Claudin-5 için yol açar , kan-beyin bariyeri olarak farelerde haline geçirgen 800 g kadar bir molar kütleye sahip moleküllere · mol -1 . Genetiği değiştirilmiş hayvanlar doğumlarından birkaç saat sonra öldü.
Endotelin sabitlenmesi, çok farklı iki tarafta hizalanmalarını sağlar: kana bakan lümen tarafı ve beyne bakan abluminal taraf.
Bazal lamina
Endotel hücreleri tamamen bir protein tabakası olan bazal laminayla çevrilidir. Bu çift katman yaklaşık 40 ila 50 nm kalınlığındadır ve yalnızca elektron mikroskobu altında görülebilir. Esasen tip IV kollajen , heparin sülfat - proteoglikanlar , laminin , fibronektin ve diğer hücre dışı matris proteinlerinden oluşur . Bazal lamina, astrositlerin terminal ayaklarının plazma membranına bitişiktir.
Perisitler
Perisitler, özellikle kaşif Charles Marie Benjamin Rouget'ten (1824–1904) sonra Rouget hücreleri olarak anılan eski literatürde , kan-beyin bariyerinin önemli bir parçasıdır. Üç temel özellik ön plandadır: kasılma yetenekleri, endotelin düzenlenmesi ve makrofaj aktiviteleri.
Serebral kılcal damarların dış endotel yüzeyinin yaklaşık% 20'si nispeten küçük, oval şekilli perisitler ile kaplıdır ve her saniye ila dördüncü endotel hücresi bir perisite bağlanır. Perisitler tercihen iki endotelyal hücre arasındaki temas noktasında bulunur. Perisitler hemen hemen tüm arteriyollerde, venüllerde ve kılcal damarlarda bulunur - sadece serebral endotelde değil. Endotelin perisitlerle kaplanma derecesi, sıkı bağlantıların geçirimsizliği ile doğrudan ilişkilidir . Delikli kılcal damarlarda, örneğin iskelet kaslarında , endotelin perisitlere oranı 100: 1'dir.
Endotelin gibi perisitler de sürekli bir bazal laminayla çevrilidir.
Hücre teması perisit-endotelyum
Perisitler, endotel hücrelerine sıkıca tutturulmuştur. En az üç tip perisit-endotel teması , bu iki hücre tipi arasındaki bağlantıyı oluşturur. Bunlar boşluk bağlantıları (kanal oluşturan protein kompleksleri), fokal yapışma ( adezyon plakları ) ve peg-ve-soket intusepsiyondur . Boşluk bağlantıları iki sitoplazmayı doğrudan birbirine bağlar ve iki hücre türü arasında kanallar aracılığıyla iyonların ve daha küçük moleküllerin değişimini sağlar. Perisitler, fokal yapışma yoluyla mekanik olarak endoteline sıkıca tutturulur. Peg-ve-soket invajinasyonları, birbirine bağlı iki hücrenin karşılıklı olarak örülmüş çıkıntılarından oluşur. Bu tip hücre teması ayrıca perisitlerin endotelin üzerine mekanik olarak sabitlenmesine de katkıda bulunur.
Her iki hücre türü de birbirlerini mitozları ve muhtemelen fenotipik ifadeleri açısından karşılıklı olarak etkiler .
kasılma
Perisitlerin kontraktil bir yüksek oranda yapısal proteini aktin . Bu, kılcal damar çapını uzantıları aracılığıyla değiştirmenize ve böylece yerel olarak kan basıncını düzenlemenize olanak tanır.
Makrositik Özellikler
Belli ki sadece serebral kılcal damarlar üzerinde yatan perisitlerin özel bir özelliği vardır. Orada makrofaj olarak hareket ederler . Perisitlerin sitoplazmasında birçok lizozom vardır ve in vivo olarak intravenöz veya intraventriküler olarak uygulanan ve aksi takdirde sadece makrofajlar tarafından alınan çözünür izleyicileri alma yeteneği gösterirler. Doku kültürlerinde, perisitlerin antijenleri fagositoz yapabildikleri ve sunabildikleri gösterilmiştir .
Bu makrositik özellikler , beyin yönünde endotel tabakasından zaten geçmiş olan nörotoksik moleküllere karşı "ikinci bir savunma hattıdır ". Perisitler bu nedenle merkezi sinir sisteminin bağışıklık sistemine önemli bir katkıda bulunur. Öte yandan bu özellikleri sayesinde otoimmün hastalıklar başta olmak üzere çeşitli hastalıkların gelişiminde de rol almaktadırlar . Alzheimer hastalığına dolaylı bir bulaşma da tartışılmaktadır.
Serebral perisitlerin diğer özellikleri
Perisitler, hücre bölünmesini ve endotelin farklılaşmasını düzenler . Ek olarak, bunlar, osteoblastlara , adipositlere , kondrositlere ve fibroblast benzeri hücrelere farklılaşabilen pluripotent yetişkin kök hücrelerden oluşan öncü hücrelerdir ( progenitör hücreler ) . Bu nedenle bazı yazarlar perisitlerden pluripotent olarak söz ederler.
Perisitler bir dizi vazoaktif agonisti sentezler ve yeni kan damarlarının oluşumunda ( anjiyogenez ) önemli bir rol oynar.
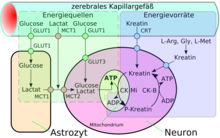
Astrositler
Astrositler, makroglia ailesinden, perisitlerden önemli ölçüde daha büyük olan yıldız şeklindeki dallı hücrelerdir . Merkezi sinir sistemine atanırlar ve doğumdan sonra hala bölünebilirler. Daha yüksek omurgalılarda, beyindeki kılcal damarların yaklaşık% 99'unu terminal ayaklarıyla kaplasalar bile, doğrudan bariyer işlevi yoktur. Bununla birlikte, endotelin ile doğrudan etkileşim içindedirler. Astrositler, serebral kan damarlarının endotelinde kan-beyin bariyerinin işlevini başlatır. Bu, nakil girişimleriyle kanıtlanmıştır. Periferal organlara nakledilen serebral kan damarları, oradaki "normal" kılcal damarlar gibi davrandı ve örneğin, fenestrasyonlar oluşturdu. Ters deneyde, merkezi sinir sistemine nakledilen periferik kılcal damarlar, burada sıkı bağlantılarla fenotipi üstlendi. Astrositlerin endotelin fenotipik ekspresyonu üzerindeki etkisi, in vitro deneylerde de görülebilir. Olarak ko-kültürler astrositler ve endotel hücrelerinden endotelin saf endotel olarak daha yoğun olan kültürler .
Astrositler, endotelin geçirgenliğini saniyeler ile dakikalar arasında değiştirebilen bir dizi haberci madde salgılar. Bunun aksine, endotel hücrelerinin salgılanmış lösemi inhibe edici faktör (LİF), bir sitokin interlökin-6 sınıf, astrositlerin farklılaşmasını indükler. Astrosit ayakları ile endotel hücreleri ve perisitler arasındaki mesafe sadece 20 nm'dir.
Bununla birlikte, astrositlerin ana görevi, nöronların besinlerle seçici olarak sağlanması ve hücre dışı iyon konsantrasyonlarının düzenlenmesidir. Beyindeki kolesterolün çoğu astrositler tarafından üretilir. Kolesterol kan-beyin bariyerini geçemez, bu yüzden beyinde lokal olarak sentezlenmesi gerekir. Vücudun kolesterolünün yaklaşık% 25'i beyinde bulunur; esasen nöronların aksonlarını kaplayan miyelinde.
Astrositlerin uç ayakları, endotel hücreleri ile hassas bir rozet benzeri temas oluşturur. Bu düzenleme, iki hücre tipinin karşılıklı olarak etkilenmesi ve iletişimi için önemlidir. Beyin parankimi ile endotelyum arasında serbest difüzyon da mümkündür.
Alzheimer hastalığı veya astrositomlar gibi astrositleri doğrudan veya dolaylı olarak etkileyen hastalıklar , astrositler ve endotelyum arasındaki yakın etkileşim nedeniyle kan-beyin bariyerinin işleyişini önemli ölçüde bozabilir.
Beynin kan-beyin bariyeri olmayan alanları
Beyindeki tüm kılcal damarlar kan-beyin bariyeri olarak inşa edilmemiştir. Örneğin , kana nöroendokrin bileşikler ( hormonlar ) salan veya duyusal bir işlevi olan beyin bölgeleri - örneğin belirli peptid hormonları için - mutlaka bir kan-beyin bariyeri yoktur. Altı çevresel organda durum budur . Epifiz bezi , eminentia mediana , Nörohipofizden , postrema alanı , Origanum vasculosum lamina terminalis ve Origanum subfornicale Var fenestralı kılcal. Örneğin, konserve bölgesindeki nöronlar vücut için toksik maddeler tespit ettikçe ve kusma merkezi bir mide bulantısını uyarır. Gelen Origanum subcommissurale , kan-beyin bariyeri circumventricular organların sadece bir tanesidir. Çevreleyen beyin dokusunu korumak için, ventriküler çevreleyen organlar tanyositlerle çevrilidir. Bunlar çok yoğun sıkı bağlantılara sahip özel ependimal hücrelerdir .
Kan-beyin bariyeri verileri
Bir yetişkinin toplam uzunluğu yaklaşık 600 km olan 100 milyardan fazla kılcal damardan oluşan bir ağ tüm beynin içinden geçer. Bu kan damarları arasındaki ortalama mesafe 40 µm'dir. Farklı beyin bölgeleri farklı derecelerde sağlanır. Kılcal damarların yoğunluğu, mm² doku başına 300 ila 800 kılcal enine kesit ile serebral kortekste ( korteks serebri ) en yüksektir .
Beyindeki kan damarlarının toplam alanı 12 ile 20 m² arasındadır. Bu damarlardan dakikada yaklaşık 610 ml kan akışı, ortalama akış hızı 1 mm / s'dir. Ortalama kan basıncı 15 ila 35 mmHg arasındadır . Ortalama geçiş süresi ( ortalama geçiş süresi MTT) 5 saniyedir. Buna karşılık, kan damarlarının yüzey alanı 180 m² olan bağırsakta yaklaşık 40 saat, karaciğerde ise 70 m² ile 30 saniye sürer.
Kan-beyin bariyerinin gelişimi
20. yüzyılın sonuna kadar, fetüslerde ve yenidoğanlarda kan-beyin bariyerinin henüz tam olarak gelişmediği (“olgunlaşmamış”) veya hatta olmadığı varsayılıyordu . Günümüzde hala yaygın olan bu görüşün nedeni, daha önceki fizyolojik deneylerdeki metodolojik yetersizliklerdir. Çoğu durumda, protein bağlayıcı boyalar veya proteinlerin kendileri hayvan fetüslerine belirteç olarak enjekte edildi. Buna yönelik ilk girişimler 1920'lerin başlarında gerçekleştirildi. Bu deneylerde, yetişkin hayvanlarda tespit edilemeyen belirteçler beyinde veya fetüslerde likörde tespit edildi. Bununla birlikte, her iki hacim de enjekte edildi, bunların bazıları test hayvanlarının kan hacmine ulaştı veya plazma proteinlerinin bağlanma kapasitesi iki kat aşıldı. Her iki durumda da, ozmotik basınç o kadar yüksektir ki hassas embriyonik kılcal damarlar kısmen yırtılabilir. Azaltılmış işaret hacimleri olan deneylerde, belirteçlerin beyne geçişi bulunamadı.
Plazmada çok erken bir embriyonik aşamada bile yüksek konsantrasyonlarda bulunabilen albümin , α-1-fetoprotein veya transferrin gibi vücudun kendi işaret moleküllerine bakıldığında, bu moleküller hücre dışı boşlukta asla tespit edilemez. beynin. Dışa akış taşıyıcı P-glikoprotein de embriyonik endotelde zaten mevcuttur. Kan-beyin bariyeri bu nedenle doğum öncesi aşamada zaten mevcuttur. Bununla birlikte, bu, embriyonik gelişim sırasında özellikle sıkı kavşaklardaki değişiklikleri dışlamaz. Sıkı bağlantılar, son derece erken bir aşamada endotel hücreleri arasında mevcuttur, ancak ilerleyici gelişime tabidir.
İnülin veya sukroz gibi küçük polar moleküller için, doğum öncesi ve yenidoğan kan-beyin bariyerinin geçirgenliği, yetişkininkinden önemli ölçüde daha yüksektir. Aynı etki iyonlarda da gözlemlenebilir. Amino asitlerin embriyonik kan-beyin bariyerinden taşınması da önemli ölçüde artmıştır - açıkça beynin daha fazla gelişmesine olan büyük ihtiyaç nedeniyle. Aynısı insülin hormonu için de geçerlidir.
Öte yandan, embriyonik beyin artık yetişkin beyninde bulunmayan ek morfolojik engeller oluşturur. Embriyonik Beyinde, örneğin var olan sözde kayış kavşaklar iç üzerinde ependima arasındaki ara yüzde likör ve beyin dokusu .
Hayvanlar aleminde ve evrim sürecinde kan-beyin engeli

Evrim sürecinde, omurgasızların ve omurgalıların sinir dokusu daha büyük, daha karmaşık hale geldi ve ilgili organizmada giderek daha merkezi bir rol üstlendi. Sonuç olarak, vücut fonksiyonlarının koordinasyonu sürekli olarak geliştirilebilir. Bu da seçimde bir avantaj sağlar. Öte yandan, giderek büyüyen ve daha karmaşık hale gelen bir beyin, besinlerle daha iyi beslenmeli ve metabolik ürünlerden arındırılmalıdır. Daha gelişmiş omurgasız durumunda, sırasına örneğin dekapodlarından veya sınıfına Kafadanbacaklılarda ve tüm omurgalıların, bu beyinde yaygın olarak dallanmış kılcal ağ tarafından sağlanmaktadır. Ksenobiyotiklere, toksinlere ve sinir sistemine zararlı diğer maddelere karşı koruyucu bir bariyerin oluşturulması, bir başka evrimsel avantajdır.
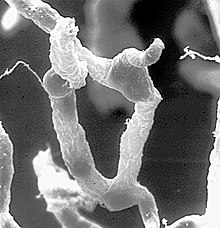
Çoğu omurgasızın kan-beyin bariyeri yoktur. Bu, endotelin genellikle sadece tam olarak kaplanmamış veya boşluklu olduğu anlamına gelir. Böcekler , yengeçler (Crustacea) ve kafadanbacaklılar (Cephalopoda) gibi kan-beyin bariyeri olan omurgasızlarda , doğası gereği yalnızca glialdir. Bu durumlarda bir glial kan-beyin bariyerinden söz edilir .
Örneğin model organizma Drosophila , bir glial kan-beyin bariyeri oluşturur.
Tüm omurgalıların bir kan-beyin bariyeri vardır ve neredeyse hepsi, endotelin sıkı bağlantılarının bariyer etkisine önemli bir katkı sağladığı endotelyal kan-beyin bariyerini oluşturur. Kan-beyin bariyerinin bariyer etkisi, yalnızca köpekbalıkları ve ışınları içeren levha solungaçının (Elasmobranchii) alt sınıfındaki perivasküler astrositler ve mersin balığı ailesi tarafından garanti edilir. Evrim sırasında endotelin yeterince yoğunsa bariyer etkisini devraldığı varsayılmaktadır. Glial kan-beyin bariyeri bu nedenle aynı zamanda kan-beyin bariyerinin orijinal formu olarak kabul edilir. Aile içinde pike balık (Polypteridae) ve sırasına akciğer balık , kan-beyin bariyeri, endotelinin sıkı bağlantıları oluşturulur. Bunun tersine, gerçek mersinbalığında, farkedilebilir sıkı bağlantılar olmaksızın glial hücrelerin karmaşık bir örtüsünden oluşur.
Bugün bu gibi glial bariyer, bazı omurgalıların elemanları bulunan membran sınırlayıcı glial avasküler (avasküler) ait omurilik ve lamprey ve bazı memelilerde ependymialen gibi Tanyzyten, bu maddeler özellikle circumventricular organlarda gibi yapılar koroid pleksus ve pigment epiteli retina (RPE). Prensip olarak, astrositler ayrıca memelilerde sıkı bağlantılar oluşturabilirler. Bu, diğer şeylerin yanı sıra, büyüyen aksonları çevreleyen koku alma zarfı hücrelerinde (OEC, İngiliz koku sarma hücreleri ) gösterilebilir.
Omurgasızlarda glial kan-beyin bariyerinin fenotipindeki yapısal farklılıklardan, bu tür engellerin evrim sırasında birkaç kez ve birbirinden bağımsız olarak ortaya çıktığı da çıkarılabilir . Endotel bariyerleri, muhtemelen endotelyum ve astrositlerin işlevinin daha sıkı ayrılması nedeniyle , seçimde önemli bir avantaj sunar . Ana seçim baskısı muhtemelen homeostaz ihtiyacından kaynaklanıyordu. Endotelyal kan-beyin bariyerinin evrim sırasında en az altı kez geliştiğine ve 400 ila 500 milyon yıl önce tüm omurgalılara glial kan-beyin bariyeri sağlandığı düşünülmektedir.
Kan likörü bariyeri
Kan-beyin bariyerine ek olarak, kan dolaşımı ile merkezi sinir sistemi arasındaki ikinci sınır kan-likör bariyeridir . Bu kan-likör bariyeri, epitel hücreleri ve koroid pleksusun sıkı bağlantıları tarafından oluşturulur . Kan likörü bariyeri ayrıca merkezi sinir sisteminin homeostazını da sağlar. Kan damarlarının damar içi boşluğundan sıvı boşluğuna veya bir koroid pleksusun ependimal hücreleri tarafından aktif olarak emilen ve salgılanan ultrafiltratlar olarak bunlardan yalnızca düşük moleküler ağırlıklı maddeler geçebilir . Bununla birlikte, madde değişimine olan katkı küçüktür ve hiçbir şekilde beynin ihtiyaçlarını karşılayamaz. Pleksus epitelinin değişim alanı, kan-beyin bariyerini oluşturan intraserebral kılcal ağınkinden yaklaşık 5000 kat daha küçüktür.
Merkezi sinir sistemi için çok önemli olan bu iki bariyere ek olarak, insan vücudunda kan yoluyla madde değişimini kontrol eden diğer benzer, oldukça seçici engeller bulunabilir. Bunlar diğerleri arasında kan-plasenta-bariyeri , kan-testis-bariyeri , kan-idrar-bariyeri , kan-göz-bariyeri , kan-timus-bariyeri ve kan-hava-bariyeridir .
Kan-beyin bariyerinin nakil süreçleri
Koruyucu bir bariyer görevi görmesine rağmen, kan-beyin bariyeri aynı zamanda besinlerin beyne taşınmasını ve metabolik ürünlerin beyinden uzaklaştırılmasını da sağlamalıdır. Suda çözünür besinler ve peptitler, kan-beyin bariyerini esas olarak hücre zarındaki belirli taşıyıcılar veya özel kanallar yoluyla geçer. Diğer çözünür bileşiklerin çoğu - eğer varsa - bu bariyeri difüzyonla geçer.
Paraselüler taşıma
Periferik kılcal damarlarda maddeler, esas olarak fenestrasyonlar ve hücre içi çatlaklar yoluyla organlara ve kaslara taşınır. Sağlıklı ve sağlam bir serebral endotelyumda, tek tek endotel hücreleri, sıkı bağlantılar yoluyla birbirine sıkıca bağlanır. Beynin kılcal damarları bu nedenle esas olarak maddelerin sadece transmembran taşınmasına izin verir ve bu da hücreler tarafından hücre içi taşınmadan daha iyi düzenlenebilir. Su, gliserin ve üre , kan-beyin bariyerinin sıkı bağlantı noktalarından yayılabilen küçük polar bileşik örnekleridir.
Serbest difüzyon
Kan-beyin bariyerinden en basit taşıma şekli serbest difüzyondur.Pasif taşıma olarak da bilinen bu değişim, prensipte hem endotelin hücre zarı yoluyla hem de sıkı bağlantılar yoluyla gerçekleşebilir . Her difüzyonda olduğu gibi, konsantrasyonun eşitlenmesi veya bir elektrokimyasal gradyanın eşitlenmesi aranır. Serbest difüzyon ile hücre zarının taşınması için enerjiye ihtiyaç duyulmaz. Materyal akışı konsantrasyonla orantılıdır ve hücre tarafından düzenlenemez.
Lipofil ( “yağ aileler”), hücre zarı özellikleri ve sıkı bağlantıları yoluyla birbirine yakın bağlantı önemli, ancak, difüzyon ile kan-beyin bariyerini geçebilen maddelerin sayısını azaltır. Belirli bir molekül için kan-beyin bariyerinin geçirgenliği, doğrudan lipofilikliği ile ilgilidir. İle ilgili olarak mol kütlesi , bu ters orantılıdır. Bu, bir bileşik ne kadar lipofilik ve ne kadar küçükse, endotelden o kadar kolay yayılabileceği anlamına gelir. Bir molekülün molar kütlesi için sınır değer olarak, sağlam bir kan-beyin bariyeri ile maksimum boyut 400 ila 500 g · mol- 1 verilir. Bu sınırın üzerindeki moleküller kan-beyin bariyerini geçemez. Bununla birlikte, kan-beyin bariyeri, belirli bir boyuttaki molekülü tamamen tutan ve daha küçük olanın beyne tamamen yayılmasına izin veren ayrı bir bariyer olarak anlaşılmamalıdır. Kan-beyin bariyerindeki difüzyon süreçleri dinamik dengelerdir. Yaklaşık 200 g · mol- 1 molar kütleye karşılık gelen 0,52 nm²'lik bir kesit alanına sahip bir molekül için , kan-beyin bariyeri, bir alanı olan bir molekülden 100 kat daha geçirgendir. 1,05 nm² (= 450 g mol −1 ).

1971'de Göttingen biyofizikçisi Hermann Träuble , küçük moleküllerin hücre zarından taşınması hakkında bir teori geliştirdi. Buna göre, lipid çift katmanlarının yağ asidi zincirleri arasındaki küçük boşluklar, difüze taşınmadan sorumludur. Boşluklar , hücre zarının fosfolipidlerinin yağ asidi kalıntılarında anti - gauche - konformasyon ( trans-gauche-trans Kinks ) geçişleriyle oluşturulur . Bu konformasyonel geçişler arasında yalnızca çok düşük enerji eşikleri vardır. Kinks (İngilizcesi. Kink , viraj ') zarından taşınacak moleküle sahip mobil ve migrate vardır. Träuble'nin teorisi, 1974'te Anna ve Joachim Seelig tarafından NMR spektroskopisiyle doğrulandı.
Lipofilisite ile ilgili olarak, oktanol / su içindeki bölme katsayısı , bir maddenin kan-beyin bariyerinden yayılma kabiliyetinin önemli bir göstergesidir. Bölme katsayısı, log P'nin belirttiği gibi genellikle logaritmik formdadır . Örneğin 3.8 olan bir maddenin log P değeri, bu maddenin oktanol (lipofilik) içinde sudan (hidrofilik) 10 3.8 kat daha yüksek bir konsantrasyonda dağıldığı anlamına gelir . Log P değeri 0 ise, madde her iki faza da eşit olarak dağılır; negatif ise madde hidrofiliktir. Prensip olarak, lipofilik maddeler, yağ asitlerinden oluşan hücrelerin plazma zarından en kolay şekilde geçebilirler. Log P değeri 3'ün üzerindeyse, bu etki genellikle tekrar azalır çünkü bu tür moleküller plazma proteinleri için yüksek bir bağlanma afinitesine sahiptir .
Bir maddenin beyne nüfuz etme kabiliyetinin tahmini, ex vivo veya in silico çeşitli modeller ve simülasyonlar kullanılarak mümkündür . İzole edilmiş endotel hücre kültürleri üzerinde güvenilir in vitro araştırmalar yürütülebilir.
Lipofiliklik ve küçük molekül boyutu, beyne olası difüzyonun garantisi değildir. Örneğin, tüm düşük moleküler ağırlıklı farmasötiklerin ( küçük moleküller ) % 98'inden fazlası kan-beyin bariyerini geçemez. Monoklonal antikorlar , rekombinant proteinler , antisens RNA veya aptamerler gibi yüksek moleküler maddeler , kendi başına kan-beyin bariyeri tarafından tutulur.
Kanal aracılı geçirgenlik
Su gibi küçük polar moleküller, hidrofobik kıvrımlar yoluyla endotelin içinden ancak çok sınırlı bir dereceye kadar yayılabilir. Bununla birlikte, kan-beyin bariyerinin su geçirgenliği çok yüksektir . Bu, William Henry Oldendorf (1925–1992) tarafından 1970 yılında trityum etiketli su ile yapılan deneylerde gösterilmiştir .
Suyun difüzyonu için hücre zarında özel hidrofilik kanal proteinleri, akuaporinler vardır . Serebral olmayan endotelin sıklıkla aquaporin-1 (AQP1) eksprese ederken, bu gen kan-beyin bariyerinde inaktive edilir. Astrositlerin varlığı, AQP1 ekspresyonunu inhibe eder. Özel serebral endoteli, esas olarak aquaporin-4 (AQP4) ve aquaporin-9'u (AQP9) ifade eder.
Beynin su dengesi aquaporinler tarafından düzenlenir. Her durumda ozmotik gradyanı takip ederek, suyun her iki yönde difüzyonu için yüksek bir kapasiteye izin verirler. Aquaglyceroporin'i oluşturan gliserol, üre ve monokarboksilatlar plazma zarında kendi kanallarına sahiptir. Kan-beyin bariyerinde, bu esasen su taşınmasından da sorumlu olan aquaporin-9'dur.
Kanallar, molekül taşınması için taşıyıcılardan çok daha hızlıdır. İyon kanalları, voltaj darbeleri veya etkileşen hormonlar ve diğer etkileyen faktörler tarafından etkinleştirilebilir veya devre dışı bırakılabilir ( geçitleme ).
Kolaylaştırılmış difüzyon
Endotel hücrelerinin hücre zarından özel bir difüzyon biçimi, kolaylaştırılmış difüzyondur (engl. Kolaylaştırılmış difüzyon ). Glikoz ve birçok amino asit gibi hayati besinler , daha önce tarif edilen nakil yollarında kan-beyin bariyeri yoluyla beyne yeterli miktarlarda sağlanamayacak kadar çok polar ve çok büyüktür. Hücre zarında bu moleküller için özel bir taşıma sistemi vardır: Taşıyıcı aracılı taşıma adı verilen . Örneğin, D- glikoz beyne GLUT-1 taşıyıcısı yoluyla taşınır. GLUT-1 taşıyıcılarının yoğunluğu, endotelinin abluminal tarafında lümen tarafına, yani kana bakan tarafa göre dört kat daha yüksektir. Taşıma yalnızca bir konsantrasyon gradyanı ile mümkündür ve herhangi bir enerji gerektirmez.
Beynin ihtiyaç duyduğu nispeten büyük miktarlarda D- glikoza ek olarak, GLUT-1'e ek olarak bir dizi başka özel taşıyıcılar da vardır. Bu taşıyıcıların çoğu, laktat , piruvat , mevalonat , çeşitli butiratlar ve asetat dahil olmak üzere bir dizi kısa zincirli monokarboksilik asit taşıyan MCT-1 ve MCT-2 dahil olmak üzere Solute Taşıyıcı (SLC) ailesindendir . SLC7 katyonik amino asitleri ( arginin , lizin ve ornitin ) taşır . İçin tarih, 307 SLC genler bilinmektedir gelen fare model organizma . Bunlardan 200'den fazlası koroid pleksus ve beynin diğer bölgelerinde ifade edilir . Ancak şimdiye kadar, aynı türün kan-beyin bariyerinde yalnızca 36 tanesi tespit edildi . 36 kişinin yaklaşık% 70'i besinlerin, vitaminlerin, hormonların ve eser elementlerin taşınmasında rol oynayan gen ürünlerine sahiptir. Tiroid taşıyıcıları SLC16a2 ve SLCO1c1, sülfat taşıyıcı SLC13a4, L - askorbik asit taşıyıcı SLC23a2, amino asit taşıyıcı SLC 38a3 ve folat taşıyıcı SLC19a1 özellikle kan-beyin bariyerinde güçlü bir şekilde eksprese edilir . Askorbik asit (C vitamini), beyne glikoz taşıyıcısı aracılığıyla oksitlenmiş biçimde sağlanır.
Taşıyıcıları iki yönde bir taşıyıcılannın olarak ve ters yönde bir anti porter olarak, (sadece bir yönde) bir uniporter olarak çalışabilir.
Aktif ulaşım
Yukarıda anlatılan endotelden pasif taşıma modlarında moleküller, herhangi bir ek enerjiye ihtiyaç duymadan beyne veya beyinden uzağa ulaşır. İlgili konsantrasyon gradyanını takip ederler. "Pompalar" adı verilen aktif taşıyıcılarla, bir konsantrasyon gradyanına karşı taşıma da mümkündür. Bununla birlikte, bu doğrudan veya dolaylı olarak adenozin trifosfat formunda enerji gerektirir. Aktif transport beyne kan gerçekleşir ise, bir söz akışı . Ters yönde, akıntıdan ("drenaj") söz edilir.
Kan-beyin bariyerinde, lö-enkefalin , arginin-vazopressin (AVP) ve [D-penisilamin2, D-penisilamin5] -enkefalin (DPDPE) için aktif akış taşıyıcıları vardır .
MDR1 geninin gen ürünü olan P-glikoprotein , kan-beyin bariyerinde tanımlanacak ilk dışa akış taşıyıcısıydı. Daha sonra , aynı zamanda ABC taşıyıcıları sınıfına ait olan çoklu ilaç direnci ile ilişkili proteinler , örneğin MRP1 geldi . Meme Kanseri direnç proteini ( Göğüs Kanseri direnç proteinleri , BCRP) P-glikoprotein endotel luminal tarafına doğru yönlendirilmiş kan esas birlikte yer almaktadır.
Bazı akış taşıyıcıları - bazı akış taşıyıcıları gibi - stereoselektif olarak çalışır . Bu , beyinden kan damarı sistemine yalnızca bir enantiyomeri taşıdıkları anlamına gelir . D - aspartik asit a, ön-madde ve N -metil- D -aspartate (NMDA) beyinde ve bu gibi çeşitli hormonların salgılanmasını etkiler lüteinleştirici hormon , testosteron veya oksitosin . İn aksine, L -aspartic asit ile birlikte L - glutamik asit, bir uyarıcı amino asitlerin biri. Kan-beyin bariyerinin dışa akış taşıyıcısı ASCT2 (alanin-serin-sistein taşıyıcısı), yalnızca birikimi nörotoksik etkilere sahip olan aspartik asidin L- enantiyomerini taşır . Bunun aksine , NMDA'nın oluşturulması için gerekli D enantiyomeri ASCT2 tarafından taşınmaz. Öte yandan EAAT taşıyıcısı ( uyarıcı amino asit taşıyıcı ) SLC1A3, SLC1A2 ve SLC1A6, aspartik asidin her iki izoformunu taşır .
Gelen epileptik doku, P-glikoprotein endotelya ve kan-beyin bariyerinin astrositlerde ve nöron aşırı eksprese edilir.
Ayrıca organik anyon taşıyıcıları (OAT ve OATP) ve organik katyon taşıyıcıları (OCT) endotelin hücre zarında bulunur. Özellikle dışa akım taşıyıcısı, çok sayıda farklı substratı endotelden kılcal damarlara aktif olarak taşıyabilir.
Endotel üzerindeki bir dizi taşıma işlemi için, bunların aktif (ATP tüketen) veya taşıyıcı aracılı süreçler olup olmadığı hala belirsizdir.
Vesiküler taşıma
Reseptör aracılı transsitoz
Seçilmiş büyük moleküllerin taşınması için reseptör aracılı transitoz vardır . Hücre zarından lümene çıkıntı yapan özel reseptörler, absorbe edilecek maddelerin tanınmasından sorumludur. Böylece örneğin 75,2 kDa'lık ağır ve 679 amino asitten oluşan transferrini kandan beynin hücre dışı sıvısına geçirir . Lümendeki reseptörler, transferrin bağlandıktan sonra içselleştirilir, yani hücrenin içine sokulurlar. Daha sonra hücrenin diğer tarafına (abluminal taraf) taşınır ve kaplanmış çukurlardan boşaltılır. Aynı mekanizma , düşük yoğunluklu lipoproteinin LDL reseptörü aracılığıyla beyne taşınmasını sağlar, böylece burada kolesterol üretilebilir. Ayrıca insülin ve diğer peptit hormonları ve sitokinler de bu yoldan beyne gider.
Adsorpsiyon aracılı transsitoz
Adsorpsiyon aracılı transitozda ( AMT), glikoproteinler tarafından negatif yüklü hücre yüzeyi ile pozitif yüklü moleküller ( katyonlar ) arasındaki elektrostatik etkileşimler , endotelin sitoplazması yoluyla taşınmaya neden olur . Bu taşıma şekli aynı zamanda katyonik taşıma olarak da bilinir . Peptidler ve proteinler, olan örneğin, izoelektrik noktası olan temel pozitif bir yüke sahiptir . Kan-beyin bariyerinin endotelyumundan geçen katyonik transitoz, reseptör aracılı transitozdan daha yüksek derecede madde taşınmasına imkan verir.
Kan-beyin bariyerindeki en önemli taşıyıcılar
| Taşıyıcı | Tanımlama (İngilizce) | gen | Kromozom, gen lokusu | aile | kaynak |
| Kolaylaştırılmış difüzyon | |||||
| GLUT1 | glikoz taşıyıcı 1 | SLC2A1 | 1 p35-p31.3 | çözünen taşıyıcı | |
| LAT1 | büyük nötr amino asit taşıyıcı 1 | SLC7A5 | 16 q24.3 | çözünen taşıyıcı | |
| CAT1 | katyonik amino asit taşıyıcı 1 | SLC7A1 | 13 q12.3 | çözünen taşıyıcı | |
| MCT1 | monokarboksilik asit taşıyıcı 1 | SLC16A1 | 1 s13.2-p12 | çözünen taşıyıcı | |
| CNT2 | konsantre nükleosit taşıyıcı 2 | SLC28A2 | 15 q15 | çözünen taşıyıcı | |
| CHT1 | kolin taşıyıcı 1 | SLC5A7 | 2 q12 | çözünen taşıyıcı | |
| NBTX | nükleobaz taşıyıcı | ? | ? | ||
| Aktif akış | |||||
| MDR1 | P-glikoprotein | ABCB1 | 7 q21.1 | ATP bağlayıcı kaset | |
| MRP1 | çoklu ilaca dirençli protein 1 | ABCC1 | 16 s13.1 | ATP bağlayıcı kaset | |
| MRP3 | çoklu ilaca dirençli protein 3 | ABCC3 | 17 q22 | ATP bağlayıcı kaset | |
| MRP4 | çoklu ilaca dirençli protein 4 | ABCC4 | 13 q32 | ATP bağlayıcı kaset | |
| MRP5 | çoklu ilaca dirençli protein 5 | ABCC5 | 3 q27 | ATP bağlayıcı kaset | |
| BCRP | meme kanseri direnç proteini | ABCG2 | 4 Q22 | ATP bağlayıcı kaset | |
| YULAF3 | organik anyon taşıyıcı 3 | SLC22A8 | 11 | çözünen taşıyıcı | |
| YULAF-A | organik anyon taşıyıcı polipeptit A | SLC21A3 | 12 s12 | çözünen taşıyıcı | |
| OATP3A1 | organik anyon taşıyıcı polipeptitler 3 | SLCO1A2 | 15 Q26 | çözünen taşıyıcı | |
| EAAT1 | uyarıcı amino asit taşıyıcı 5 | SLC1A3 | 5 s13 | çözünen taşıyıcı | |
| GERGİN | taurin taşıyıcı | SLC6A6 | 3 p25-q24 | çözünen taşıyıcı | |
| Reseptör aracılı taşıma | |||||
| INSR | İnsülin reseptörü | INSR | 19 s. 13.2 | ||
| TFR1 | transferin reseptörü | TFRC | 3 q29 | ||
| IGF1R | insülin benzeri büyüme faktörü 1 reseptörü | IGF1R | 15 q25-q26 | ||
| LEPR | leptin reseptörü | LEPR | 1 s31 | ||
| FCGRT | IgC'nin Fc parçası, reseptör taşıyıcısı | FCGRT | 19 q13.3 | ||
| SCARB1 | çöpçü reseptör sınıfı B 1 | SCARB1 | 12 q24.31 |
Solute Carrier ailesinin çeşitli üyelerinin ve ABC taşıyıcısının etkileşimi, ksenobiyotiklerin beyne girmesini önlemek için kan- beyin bariyerinin son derece etkili bir koruyucu mekanizmasıdır .
Kan-beyin bariyerinin geçirgenliğinin ölçülmesi ve görüntülenmesi
Yeni farmasötikler geliştirirken, bir maddenin kan-beyin bariyerini ne ölçüde geçebildiği önemli bir farmakolojik parametredir ( beyin alımı ). Bu , hem etkilerini esas olarak merkezi sinir sisteminde göstermesi beklenen nörofarmasötikler için hem de yalnızca periferide etki etmesi beklenen farmasötikler için geçerlidir. Bir maddenin kan-beyin bariyerini geçip geçemeyeceğini, ne ölçüde ve hangi mekanizma ile geçebileceğini araştırmak için geçmişte bir dizi farklı yöntem geliştirilmiştir. Klasik yöntemler , in vivo model organizmalarla çalışır . Daha yeni yaklaşımlar hücre kültürlerini ( in vitro ) kullanır ve çok yeni bir yöntem bilgisayar simülasyonları ( in silico ) aracılığıyla çalışır . Memelilerde kan-beyin bariyerinin büyük ölçüde özdeş yapısı nedeniyle, in vivo sonuçlar insanlara kolayca aktarılabilir.
Fiziksel temeller
Kan-beyin bariyerinin geçirgenliğinin ölçümleri için Renkin (1959) ve Crone (1965) tarafından tek bir kılcal damara dayalı basitleştirilmiş bir model oluşturulmuştur. Sadeleştirmelere rağmen, bu model gerçek koşullara en iyi yaklaşımdır. Sözde geçirgenlik yüzeyi ( geçirgenlik yüzey alanı ürünü ) PS, kılcal yatağın geçirgenliğinin bir ölçüsüdür. Crone-Renkin sabiti olarak da bilinen geçirgenlik yüzey ürünü, belirli bir maddenin geçirgenlik katsayısı ile mevcut transfer alanının ürünüdür. Ölçüm birimi ml min -1 -g -1 (g yaş doku) ve tekabül perfüzyon (kan akışı) Q düğmesine tek taraflı ( tek yönlü bir madde olduğu oranıdır) ekstre fraksiyon E taşınır, sonra beyinden geçer:
.
Perfüzyon (Q), geçirgenlik yüzey ürününden (PS) daha büyükse, kütle transferi perfüzyonla sınırlıdır. Durum tersine dönerse, kütle transferi difüzyonla sınırlanır.
Prensip olarak, tüm maddeler için E'nin değeri her zaman 1'den küçüktür, çünkü akış, madde arzından daha büyük olamaz. 0.2'nin altındaki değerlerde, genellikle, maddelerin beyne taşınması için sınırlayıcı faktörün nüfuz etme olduğu söylenir. 0,2 ila 0,8 aralığında nüfuz etme orta düzeydedir.
In silico prosedürü
Simülasyon süreçleri esas olarak ilaç tasarımının çok erken safhalarında kullanılmaktadır . Hesaplama modelleri şu anda difüzyon yoluyla pasif taşıma ve lipofiliklik, yük, molar kütle ve hidrojen bağlarının sayısı gibi bazı moleküler tanımlayıcılarla sınırlıdır .
In vitro yöntem
En basit in vitro yöntem, izole edilmiş, hala canlı kılcal damarlar kullanmaktır. Bu, hücresel düzeyde taşıma mekanizmalarını araştırmayı mümkün kılar. Bazı durumlarda, otopsilerden elde edilen insan kaynaklı kılcal damarlar da kullanılır. Kılcal damarlar , hücrelerdeki ATP kaynağı büyük ölçüde kullanılmış olsa bile, izolasyondan sonra bile metabolik olarak aktiftir. Ancak bu prosedürde endotelinin hem lüminal hem de abluminal tarafı incelenecek aktif maddeye maruz bırakılır. Bu nedenle etken madde alımı açısından iki taraf arasında ayrım yapmak mümkün değildir. İnkübe edilmiş kılcal damarların uzamsal dağılımı, konfokal floresan mikroskobu kullanılarak analiz edilebilir . Örneğin , transferrin reseptöründe floresan etiketli monoklonal antikorların alımı incelenebilir. Yöntem , endotelin lümen tarafında aktif bileşenlerin dışarı akışına yönelik yarı kantitatif deneylerin de mümkün olacağı şekilde rafine edilebilir .
İle ölümsüzleştirilmiş endotel hücre hatları, kantitatif ifadeleri bir maddenin geçirgenliği yaklaşık yapılabilir. Artık farklı türlerden çeşitli farklı hücre dizileri var . Bu hücre hatları hem temel araştırma hem de ilaç geliştirme için kullanılır. Kılcal damarlarda olduğu gibi, endotel hücreleri tek katmanlar halinde ( tek katmanlı ) büyütülür. Bu katmanların kalitesi, örneğin endotel katmanının elektriksel direnci aracılığıyla değerlendirilebilir. Transendotelyal elektrik direnci ( TEER ) mümkün olduğu kadar yüksek olmalıdır. Canlı organizmada bu değer 2000 cm²'nin üzerindedir ve esas olarak sıkı bağlantıların kalitesiyle belirlenir. İn vitro değerler genellikle bir olan büyüklük sırası kadar düşük olur. Bu değerler, endotelin ve astrositlerin ortak kültürleri kullanıldığında önemli ölçüde iyileşir. Astrositler, sıkı bağlantılar oluşturmak için endotelinin gen ekspresyonunu olumlu yönde etkiler. Bu şekilde 800 cm²'ye kadar değerler elde edilebilir. Hücre kültürü kortizol içeriyorsa , astrositler olmadan da benzer şekilde yüksek değerler elde edilebilir .
In vivo yöntem

Paul Ehrlich tarafından kan-beyin bariyerinin (im) geçirgenliğini göstermek için kullanılan ilk yöntem, bir boya enjeksiyonu ve ardından test hayvanının diseksiyonuydu. Kan-beyin bariyerini aşabilen boyalar, beynin interstisyumunu kalıcı olarak lekeler. Yöntem, boyalarla sınırlıdır ve yalnızca kalitatif değerlendirmelere izin verir. Kan-beyin bariyerini hedefli bir şekilde açmayı amaçlayan çalışmalarda boyalar günümüzde hala kullanılmaktadır. Aynı nedenle, mikrobiyolojide çok sık kullanılan floresan etiketleme yöntemi, kan-beyin bariyerindeki küçük moleküllerin taşıma mekanizmalarını araştırmak için tamamen uygun değildir. Floresan etiketleme yalnızca, floresan boya molekülünün peptide göre nispeten küçük olduğu polipeptitler gibi çok büyük moleküller için kullanılabilir.
Geçmişte, bazıları bugün hala uygulamada kullanılan bir dizi farklı in vivo yöntem geliştirilmiştir. Genel olarak, in vivo yöntemler referans yöntemlerdir. Bir aktif bileşenin bir model organizmada gerçek fizyolojik koşullar altında intravenöz veya intra-arteriyel uygulaması ve daha sonra beyin dokusunun analizi, halihazırda herhangi bir in vitro yöntemle veya hatta simülasyon hesaplamalarıyla değiştirilemez. Bunlar, beyindeki bir maddenin alımının uzun süreler boyunca ve kan-beyin bariyerinden birkaç geçişle belirlenebildiği en hassas yöntemlerdir.
Beyin alım indeksi
Kan-beyin bariyerindeki besin ve aktif maddelerin alımını ölçmek için ilk yöntem , 1970 yılında William H. Oldendorf tarafından geliştirilmiştir. Bir radyoaktif işaretli madde olan enjekte bir aynı şekilde radyoaktif olarak işaretlenmiş ile birlikte referans örneği direkt olarak ve olabildiğince hızlı bir şekilde içine dış karotid arteri bir test hayvanına (genellikle bir sıçan). Enjeksiyondan yaklaşık beş saniye sonra hayvanın kafası kesilir , beyin izole edilir ve içerdiği etiketlenmiş maddelerin konsantrasyonunu belirlemek için radyoaktivite kullanılır. Sözde beyin alım indeksi (BUI), enjekte edilen maddelerin dozunun oranından ve test maddesi ve referans numunesi için izole edilmiş beyinde ölçülen dozdan hesaplanır .
Uygulanan maddelerin uygulandığı ve nüfuz edebildiği çok kısa süreden dolayı, yöntem sadece kan-beyin bariyerini hızla aşan maddeler için uygundur. Bunun aksine, birçok peptid gibi hidrofilik bileşikler yalnızca yavaş emilir. Yöntem, bu tür maddeler için uygun değildir.
Araştırılacak olan bileşiklerin çoğunlukla trityum ya da 14 ° C etiketlenmiştir. Örneğin, toz haline getirilmiş, su ya da 14 C-bütanol , referans madde olarak kullanıldığında, . Test hayvanına enjekte edilen hacim mümkün olduğu kadar küçük tutulur. 10 µl'den küçük hacimler , ölçülen BUI'yi etkilediğinden, akış ve dağıtım artefaktlarından kaçınmak için gereklidir . Öte yandan, BUI'nin enjekte edilen maddenin konsantrasyonuna bağımlılığı oldukça düşüktür.
Çeşitli maddelerin beyin alım indeksi
| bağ | BUI [%] | günlük P | M [g / mol] |
| Sitozin | 1.2 | −1.72 | 243.2 |
| üre | 1.4 | −1,52 | 60.1 |
| Mannitol | 2 | −2.11 | 182.2 |
| Tiyoüre | 5 | −0,96 | 76.12 |
| EtilenGlikol | 18'i | −1.3 | 62.1 |
| Asetamit | 23 | −1.1 | 59.1 |
| Metanol | 103 | −0,52 | 32 |
| Propilen glikol | 27 | 0,92 | 76.1 |
| Etanol | 107 | −0,18 | 46.1 |
| Butanol | 117 | 0.93 | 74.1 |
| Benzil alkol | 94 | 1.1 | 108.1 |
| fenobarbital | 56 | 1.42 | 232.2 |
| Fenazon | 83 | 0.38 | 188.2 |
| kafein | 103 | 0.02 | 194.2 |
| Fenitoin | 71 | 2.4 | 252.3 |
| Estradiol | 94 | 2.61 | 272.4 |
| testosteron | 85 | 3.28 | 288.4 |
| eroin | 87 | 1.14 | 369.4 |
| Morfin | 2.6 | −0,2 | 285.3 |
| nikotin | 120 | 0.7 | 162.2 |
göre :, veriler, aksi belirtilmedikçe, şuradan:
Beyin Akıntı İndeksi
1995 yılında geliştirilen bu prosedürde beyinden bir maddenin kan-beyin bariyerini geçerek kana geçişi belirlenir.
Beyin alım indeksinde olduğu gibi, radyoaktif olarak işaretlenen test maddesi, yine radyoaktif olarak işaretlenmiş bir referans bileşiği ile birlikte doğrudan test hayvanının beynine enjekte edilir. Bununla birlikte, geçirgen olmayan bir izleyici - çoğunlukla inülin - referans bileşik için kullanılır. Burada da belirli bir süre sonra test hayvanının başı kesilir ve beyin izole edilir. Radyoaktivite daha sonra beynin aynı tarafında ( ipsilateral ) ölçülür. Beyin efluks indeksi (BEI) daha sonra kan-beyin bariyerini geçen ve kanda dolaşan test maddesinin oranı ve beyinde kalan orandan hesaplanır:
- .
Beyin perfüzyonu
Perfüzyon tekniğinde, incelenecek radyoaktif olarak etiketlenmiş madde, test hayvanının dış karotid arterine perfüze edilir. Hayvan daha sonra öldürülür ve beyin çıkarılır. Beyin homojenleştirilir ve içindeki radyoaktivite ölçülür. Bu yöntemin avantajı, test maddesinin örneğin içerdiği enzimler tarafından kandaki olası bir parçalanmasının büyük ölçüde önlenmesidir. Gine domuzları, test hayvanları olarak özellikle uygundur çünkü karotis arteri, örneğin sıçanda olduğu gibi, boyun ile beyin arasında dallanmaz. Bu, perfüzyon süresinin 30 dakikaya çıkarılmasını mümkün kılarken, sıçanda sadece 20 saniye mümkündür. Bu yöntemin operasyonel eforu son derece yüksektir. Bu nedenle, esasen sadece plazmada yeterli stabiliteye sahip olmayan veya beyne çok düşük perfüzyon kapasitesine sahip maddeler için kullanılır.
Geliştirilmiş bir varyant, kılcal boşaltma yöntemi (Engl. Kılcal boşaltma yöntemi ). Kılcal kısımlar beyin dokusundan ayrılmış göre santrifüj . Bu, transitoz veya difüzyon, yani beyne gerçek nüfuz ve endoteldeki olası endositoz arasında bir ayrım yapılmasına izin verir.
Gösterge difüzyon tekniği
İndikatör difüzyon tekniğinde incelenecek aktif bileşen, geçirgenlik kapasitesi olmayan bir referans madde ile birlikte dış karotid artere uygulanır. Her iki maddenin de radyoaktif olarak etiketlenmesine gerek yoktur. Örneğin dahili şah damarı gibi kanın geri akışından, her iki maddenin konsantrasyonu kan alınarak ve plazmayı analiz ederek belirlenebilir. Maddenin beyne nüfuz etmesi , kan geri akışındaki test maddesinin azalmasından hesaplanabilir.
Beyinde, indikatör difüzyon tekniği sadece bu organa yüksek nüfuz etme kapasitesine sahip maddeler için uygundur.
Kantitatif otoradyografi
ana makaleye bakın: Otoradyografi

Kantitatif otoradyografi (QAR) 1970'lerde geliştirilmiştir. Genellikle radyoaktif olarak 14 C ile etiketlenen madde intravenöz olarak uygulanır. Zamanın belirli bir noktasında organlar izole edilir ve kurutulmuş donmuş bölümler bir X-ışını filmi veya yüksek çözünürlüklü bir sintigrafik detektör plakası üzerine yerleştirilir. Karartma derecesi veya tespit edilen radyasyon dozu, çok düşük geçirgenliğe sahip maddelerle - örneğin 125 I etiketli albümin ile karşılaştırmalı deneyler yoluyla beyinde ve aynı zamanda diğer organlarda maddenin emilimini ölçmek için kullanılabilir . Lokal perfüzyon ayrı bir ölçümde belirlenirse, geçirgenlik yüzey ürünü hesaplanabilir.
İntraserebral mikrodiyaliz
İntraserebral olarak mikrodiyaliz , bir yarı-geçirgen membran olup , beyin dokusunda implante. Maddeler, zarın içine yerleştirilmiş bir mikrodiyaliz kateteriyle perfüze edilebilir . Perfüzat numuneleri daha sonra alınabilir ve aynı kateter kullanılarak analiz edilebilir.
Test hayvanında kan-beyin bariyerinde çeşitli incelemeler ve deneyler yapılabilir. Bunun bir örneği, aşağıda açıklandığı gibi hipertonik solüsyonlar kullanılarak kan-beyin bariyerinin açılmasıdır. Yöntem, sürekli sıvı çekilmesi için uygundur. Bu şekilde, intravenöz veya oral yoldan uygulanan maddeler için konsantrasyon-zaman profilleri oluşturulabilir.
Kan-beyin bariyerindeki taşıma mekanizmalarını araştırmak için çok çeşitli deneyler intraserebral mikrodiyaliz ile gerçekleştirilebilir.
İnsan tıbbında, intraserebral mikrodiyaliz, felçlerin nörokimyasal izlenmesi için kullanılır .
Görüntüleme prosedürleri
Yardımıyla görüntüleme yöntemleri , bir invasif olmayan çeşitli maddelerle, kan-beyin bariyerinin geçirgenliğinin ekran ve ölçümü mümkündür. Bu yöntemlerden bazıları insan tıbbında klinik uygulamada kullanılmaktadır. Ayrıca pozitron emisyon tomografisi (PET), manyetik rezonans spektroskopisi (MRS) ve manyetik rezonans görüntüleme (MRI) kullanılır.
- EVCİL HAYVAN
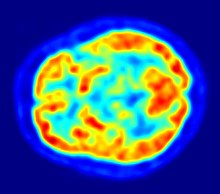
Pozitron emisyon tomografisi ile, esasen P-glikoproteinli potansiyel aktif maddelerin dışarı akış süreçlerinin kan-beyin bariyerini incelediği gösterilmiştir. P-glikoproteinin kan-beyin bariyerindeki işlevini ve etkisini anlamak, nörofarmasötiklerin gelişimi için büyük önem taşımaktadır. Bu tamamen bilimsel araştırmalar, pozitron yayıcı (beta artı bozunma (β +)) ile işaretlenmiş maddelerle gerçekleştirilir . İzotop 11 C esas olarak bunun için kullanılır. Flor içeren bileşikler durumunda, kısa ömürlü izotop 18 F tercih edilir . Çünkü için 20.39 çok kısa yan-ömrü 11 ° C ya da 110 dakika 18 F, bu tür deneyler yalnızca hangi yakın araştırma tesislerinde yürütülebilir siklotron bulunmaktadır. Uygun şekilde işaretlenmiş ve araştırılmış bileşiklerin örnekleri verapamil , karazolol , loperamid ve karvediloldür . Verapamil, P-glikoproteini inhibe edebildiğinden özellikle farmakolojik açıdan ilgi çekicidir .
PET, aktif bileşen ve P-glikoprotein arasındaki etkileşim açısından klinik öncesi aşamada kullanılan model organizmalar ile insanlar arasında doğrudan bir in vivo karşılaştırmayı mümkün kılan birkaç yöntemden biridir.
- Manyetik rezonans görüntüleme
Manyetik rezonans tomografi (MRT), aktif maddelerin beyne geçişini göstermek için bir görüntüleme yöntemi olarak çok duyarsızdır. Hasarlı bir kan-beyin bariyeri ile durum tamamen farklıdır. Bu durumlarda, kontrastlı MRG beyindeki çeşitli nörodejeneratif hastalıklar ve kanserler için tanısal bir yöntem olarak önemli bir rol oynar . Bu, kan-beyin bariyeriyle dolaylı olarak ilişkilendirilen hastalıklar bölümünde daha ayrıntılı olarak açıklanmaktadır .
- Manyetik rezonans spektroskopisi

Manyetik rezonans spektroskopi (MRS) üzerinde olan nükleer manyetik rezonans manyetik rezonans görüntüleme tarayıcıya tabanlı yöntemle bir yürütmek için nükleer spin rezonans spektroskopisi verir. Beyinde belirli maddeler veya bunların metabolik ürünleri spektroskopik olarak tespit edilebilir ve ölçülebilir. Suyun proton spinine dayanan manyetik rezonans tomografisine kıyasla , burada diğer atomik çekirdekler ilgi çekicidir. Bunlar özellikle 19 F, 13 C, 31 P ve susuz protonlardır. Sudaki çok daha büyük miktarlarda bulunan protonlarla karşılaştırıldığında, genellikle sadece izlerde bulunan bu çekirdekler, buna uygun olarak zayıf sinyaller sağlar. Uzamsal çözünürlük yaklaşık 1 cm³'lük bir hacim elemanına karşılık gelir . MRS ve MRT birbirleriyle kolayca birleştirilebilir. MRT, anatomik yapıyı ve MRS, anatominin karşılık gelen uzamsal çözümlenmiş analizini sağlar. Örneğin MRS ile, nöroleptikler trifluoperazin ve flufenazin gibi florin içeren aktif bileşenlerin farmakokinetiği bir kişinin beyninde gözlemlenebilir ve ölçülebilir. Manyetik rezonans spektroskopi ile aktif madde ve metabolitleri arasında niceliksel bir ayrım yapılabilir. Serbest ve bağlı aktif madde arasında da bir ayrım yapılabilir.
MRS'nin dezavantajları, yöntemin düşük hassasiyeti ve düşük uzaysal çözünürlük nedeniyle gereken uzun ölçüm süreleridir. İkincisi, özellikle küçük hayvanlarla yapılan deneylerde sorunludur.
Kan-beyin bariyerini aşmak için kavramlar
ana makaleye bakın: Kan-Beyin Engelini Aşmak İçin Kavramlar
Taşıma süreçleri ile ilgili bölümde gösterildiği gibi , sadece birkaç madde kan-beyin bariyerini geçebilir, bu yüzden birçok potansiyel nörofarmasötik sonuçta kan-beyin bariyerinde başarısız olur. Bu maddelerin% 98'i kan-beyin bariyerini geçemez.
Bu nedenle, on yıllardır, aktif maddelerin beyne taşınmasını bypass ederek veya - ideal olarak daha seçici olarak - kan-beyin bariyerini açarak sağlamayı amaçlayan yöntemler üzerinde yoğun araştırmalar yapılmıştır. Kan-beyin bariyerini aşmak için bir dizi strateji geliştirilmiştir veya halen geliştirme aşamasındadır.
Kan-beyin bariyerinin bozuklukları
Ana madde: Kan-beyin bariyerinin bozulması
Kan-beyin bariyerindeki bozukluklara bir dizi farklı hastalık neden olabilir. Kan-beyin bariyerinin kendisi de genetik olan çok nadir bazı nörolojik hastalıkların başlangıç noktası olabilir .
Kan-beyin bariyerinin koruyucu etkisinin bozulması, birçok nörodejeneratif hastalığın ve beyin hasarının bir komplikasyonudur . Diabetes mellitus veya enflamasyon gibi bazı periferik hastalıklar da kan-beyin bariyerinin işleyişi üzerinde zararlı bir etkiye sahiptir.
Diğer hastalıklar ise endotelin işlevini "içeriden" bozar, yani kan-beyin bariyerinin bütünlüğü hücre dışı matriksten gelen etkilerle bozulur. Bunun bir örneği glioblastomdur .
Aksine, beyindeki bazı hastalıklar, belirli patojenlerin kan-beyin bariyerini geçebilmesiyle kendini gösterir. Bunlar, örneğin HI virüsü, insan T-lenfotropik virüsü 1 , Batı Nil virüsü ve Neisseria meningitidis veya Vibrio cholerae gibi bakterileri içerir .
Multipl skleroz durumunda, "patojenler" vücudun kendi bağışıklık sisteminin kan-beyin bariyerini geçen hücreleridir . Benzer şekilde bazı serebral olmayan tümörlerde metastatik hücreler kan-beyin bariyerini geçer ve beyinde metastaza neden olabilir .
Kan-beyin bariyeri üzerindeki eksojen etkiler
alkol
Alkol kötüye kullanımı , nöroetolojik hastalıklar, enflamatuar hastalıklar ve bakteriyel enfeksiyonlara yatkınlık için önemli bir risk faktörüdür . Ek olarak, kronik alkol tüketimi, bazı nörodejeneratif hastalıkların gelişimini etkileyen önemli bir faktör olarak görülen kan-beyin bariyerine zarar verir. Kan-beyin bariyerindeki hasar , alkol bağımlılarının nöropatolojik çalışmaları ve hayvan deneyleriyle kanıtlanmıştır.
Hayvan deneylerinde, alkol tüketimi ile aktive edilen miyozin hafif zincir kinaz enziminin (MLCK), endoteldeki birkaç sıkı bağlantı veya hücre iskeleti proteininin fosforilasyonuna yol açtığı ve bu da kan-beyin bariyerinin bütünlüğünü etkileyen bulundu. Ek olarak, alkolün neden olduğu oksidatif stres , kan-beyin bariyerine daha fazla zarar verir.
Alkolün kendisi değil , endoteldeki MLCK enzimini aktive eden metabolitleridir . Kan-beyin bariyerinin disfonksiyonu, lökositlerin beyne göçünü kolaylaştırarak nöroinflamatuar hastalıkları teşvik eder.
nikotin
Kronik nikotin kötüye kullanımı sadece akciğer kanseri riskini artırmakla kalmaz, aynı zamanda kardiyovasküler hastalık riskini de artırır . Buna karşılık, kardiyovasküler risk faktörleri ile artan demans riski arasında doğrudan bir ilişki vardır . Birkaç meta araştırmada, sigara içenlerin sigara içmeyenlere göre Alzheimer hastalığına bağlı demans riskinin önemli ölçüde daha yüksek olduğu bulundu. Vasküler demans ve hafif bilişsel bozukluk riski çok az artmış veya çok az artmıştır. Kronik nikotin uygulaması, hayvan deneylerinde test hayvanlarının kan-beyin bariyerinin hem işlevini hem de yapısını değiştirir. Sükroz model maddesi endotelini önemli ölçüde daha kolay geçebilir, bu da esasen sıkı bağlantı proteini ZO-1'in değişen dağılımından ve klaudin-3'ün azalmış aktivitesinden kaynaklanmaktadır. Ayrıca, kronik nikotin uygulamasından sonra kan-beyin bariyerinin endotelyumunda artmış mikrovilli oluşumu , düzenlenmiş Na + K + 2Cl - simporterleri ve düzenlenmiş sodyum-potasyum pompaları gözlenmiştir.
Gelen epidemiyolojik çalışmalar, sigara içen sigara içmeyenlere göre daha bakteriyel menenjit yakalanma risklerinin çok daha yüksek olduğu görüldü. Nikotin , endotelinin hücre iskeletinin aktin ipliklerini değiştirir , bu da görünüşe göre E. coli gibi patojenlerin beyne geçişini kolaylaştırır.
Nikotin asetilkolin reseptörüne (nAChrs) bağlanan nikotin antagonisti metillikakonitin (MLA) gibi bazı difüzyon kısıtlı bileşikler için , kan-beyin geçişi kronik nikotin tüketimi ile kötüleşir.
Nikotine özgü bir immünoglobulin G'ye dayalı bir aşı geliştirme aşamasındadır. Bu aşının amacı, nikotini spesifik olarak bağlayan ve böylece BBB'den geçişi engelleyen antikorların oluşumunu uyarmaktır.
Elektromanyetik dalgalar (hücresel iletişim)
Yüksek enerji yoğunluğu ile megahertz'den gigahertz'e kadar elektromanyetik radyasyonun sağlık üzerindeki olumsuz etkileri kanıtlanmıştır. Aksine, esas olarak mobil ve veri radyosunda kullanıldığı gibi, bunun daha düşük enerji yoğunluğu ile etkileri tartışmalı olarak tartışılmaktadır. Kan-beyin bariyeri üzerindeki etkiler de bir sorundur.
Elektromanyetik radyasyonun enerji yoğunluğu yüksek olduğunda, etkilenen vücut dokusunda önemli bir ısınma gözlenir. Kafatasındaki bu ısınma kan-beyin bariyerini etkileyebilir ve onu daha geçirgen hale getirebilir. Bu tür etkiler, ısı kaynaklarının vücudun çevresel kısımları üzerindeki etkisiyle de gösterilir. Mobil iletişimde kullanılan servisler ile beyin maksimum 0.1 K (maksimum iletim gücü ile 15 dakikalık mobil iletişim çağrısı ) kadar ısıtılabilmektedir. Ilık bir banyo veya fiziksel eforla beyin zarar görmeden daha fazla ısınabilir. İsveçli beyin cerrahı çalışma grubundan özellikle 1990'ların başından bu yana bilimsel çalışmalarda, Leif G. Salford de Lund Üniversitesi , sonuçları elde edilmiştir maruz kaldıktan sonra ısıl olmayan aralıkta açık kan-beyin bariyeri GSM Frekansları tanımlayın. Hücre kültürleri üzerinde yapılan in vitro deneyler daha sonra benzer sonuçlara ulaştı.
Diğer çalışma grupları Salford'un bulgularını doğrulayamıyor. Diğer çalışma grupları da özellikle kullanılan metodolojiyi sorgulamaktadır.
İnsan teşhisi
Kontrastlı manyetik rezonans görüntüleme
Manyetik rezonans görüntüleme için ilk kontrast ajanı olan gadopentetat dimegluminin (Gd-DTPA) geliştirilmesinden kısa bir süre sonra, 1984 yılında, kan-beyin bariyerinin lokal bozukluklarının teşhisi için kontrastlı manyetik rezonans görüntüleme potansiyeli fark edildi. Oldukça polar bir molekül olarak Gd-DTPA, sağlıklı kan-beyin bariyerini geçemeyecek kadar hidrofiliktir. Glioblastomalar tarafından tetiklenenler gibi sıkı bağlantılardaki değişiklikler, bu kontrast maddenin interstisyuma paraselüler taşınmasını sağlar. Orada, çevreleyen suyun protonlarıyla etkileşim yoluyla kontrastı yoğunlaştırır ve böylece kan-beyin bariyerinin kusurlu bölgelerini görünür kılar. Bu kan damarları tümörü beslemekten sorumlu olduğu ve ona çok yakın olduğu için tümörün boyutu gösterilebilir.
Akut iskemik inme durumunda , kan-beyin bariyerinin bozulması, kontrastlı MRI kullanılarak bir tanı koymak için de kullanılabilir.
Gevşeme süresinin belirlenmesiyle, interstisyumdaki Gd-DTPA miktarı ölçülebilir.
Diğer görüntüleme testleri
Normalde sağlıklı kan-beyin bariyerini geçmeyen radyoaktif olarak etiketlenmiş izleyiciler kullanılarak, insanlarda kan-beyin bariyerinin işlevini kontrol etmek için testler de yapılabilir. Prensip olarak, hem tek foton emisyonlu bilgisayarlı tomografi ( SPECT) hem de pozitron emisyon tomografisi (PET) kullanılabilir. Örneğin, akut inme geçiren hastalarda , beyinde 99m Tc-heksametilpropilamin oksim (HMPAO) alımında artış tespit edilebilir.
Bilgisayarlı tomografi (BT) kusurlarının yardımıyla , kan-beyin bariyeri, uygun kontrast ortamının kılcal damarlardan interstisyel boşluğa difüzyonu ile ölçülebilir.
Keşif hikayesi
Kan-beyin bariyerinin varlığının ilk kanıtı Alman kimyager Paul Ehrlich'ten geliyor . 1885 yılında, suda çözünür asidik vital boyalar sıçanların kan dolaşımına enjekte edildiğinde, beyin ve omurilik dışındaki tüm organların boyayla lekelendiğini buldu.
1904'te, beyin dokusunun enjekte edilen boyaya düşük afinitesinin bu bulgunun nedeni olduğu yanlış sonucuna vardı.
Paul Ehrlich'in eski bir meslektaşı olan Edwin Goldmann , Paul Ehrlich'in ilk kez 1909'da beş yıl önce sentezlediği di-azo boya tripan mavisini enjekte etti . Koroid pleksusun çevreleyen beyin dokusunun aksine belirgin şekilde lekelendiğini fark etti . 1913'te aynı boyayı doğrudan köpeklerin ve tavşanların omurilik sıvısına enjekte etti . Tüm merkezi sinir sistemi (beyin ve omurilik) boyandı, ancak başka bir organ yoktu. Goldmann, beyin omurilik sıvısının ve koroid pleksusun besinlerin merkezi sinir sistemine taşınmasında önemli bir rol oynadığı sonucuna vardı . Dahası, nörotoksik maddeler için bir bariyer işlevinden şüpheleniyordu.
1898'de Artur Biedl ve Rudolf Kraus safra asitleri ile deneyler yaptı . Kan dolaşımına sistematik olarak uygulandığında, bu bileşikler toksik değildi. Ancak beyne enjekte edildiklerinde komaya kadar tepkilerle nörotoksikti .
1900'de Max Lewandowsky , benzer deneylerde potasyum hekzasiyanidoferrat (II) (sarı kan likörü tuzu) kullandı ve Biedl ve Kraus ile benzer sonuçlara ulaştı. Lewandowsky ilk kez "kan-beyin bariyeri" terimini kullandı.
1890'da Charles Smart Roy ve daha sonra Nobel Ödülü sahibi Charles Scott Sherrington , beynin, vasküler beslemenin fonksiyonel aktivitedeki yerel dalgalanmalara karşılık geldiği içsel bir mekanizmaya sahip olduğunu varsaydı .
"Beyin, işlevsel aktivitenin yerel varyasyonlarına uygun olarak vasküler beslemesinin yerel olarak değiştirilebildiği kendine özgü bir mekanizmaya sahiptir."
Rusya Bilimler Akademisi'nin ilk kadın üyesi olan Lina Stern , 1921'de hemato-ensefalik bariyer olarak adlandırdığı kan-beyin bariyerinin araştırılmasına önemli katkılarda bulundu .
Kan-beyin ve kan-likör engelleri arasındaki ayrım, 1930'larda Friedrich Karl Walter ve Hugo Spatz tarafından yapıldı . Merkezi sinir sistemindeki gaz değişimi için beyin omurilik sıvısının akışının tamamen yetersiz olduğunu varsaydılar.
Goldmann ve Ehrlich'in girişimleri kan dolaşımı ile merkezi sinir sistemi arasında bir bariyer olduğunu öne sürse de, 1960'lara kadar varlığından şüpheler vardı. Goldmann'ın deneyinin bir eleştiri noktası , boyaların enjekte edildiği iki sıvı olan kan ve likörün önemli ölçüde farklı olması ve bu nedenle difüzyon davranışının ve sinir dokusuna olan afinitesinin etkilendiğiydi. Bazik azo boyalarının sinir dokusunu boyadığı, yani kan-beyin bariyerini geçerken asidik boyaların geçmediği deneysel bulgusuyla anlamak daha da zorlaştı. Ulrich Friedemann , boyaların elektrokimyasal özelliklerinin bundan sorumlu olduğu sonucuna vardı. Serebral kılcal damarlar, kanın pH değerinde pozitif olan ve asidik maddeleri geçirmeyen yüksüz maddeler veya yüklü maddeler için geçirgendir. Bu tez, takip eden dönemde çok sayıda maddenin kan-beyin bariyerindeki geçirgenlikleri açısından incelendiğinde yetersiz kaldı. Aşağıdaki açıklayıcı modellerde, molar kütle, molekül boyutu, bağlanma afiniteleri, ayrılma sabitleri, yağ çözünürlüğü, elektrik yükü ve bunların en çeşitli kombinasyonları gibi çok sayıda parametre tartışılmıştır.
Kan-beyin bariyerinin temel yapısının bugünkü anlayışı, 1960'ların sonunda gerçekleştirilen fare beyinlerinin elektron mikroskobik görüntülerine dayanmaktadır. Thomas S. Reese ve Morris J. Karnovsky deneylerinde yaban turpu peroksidazını test hayvanlarına intravenöz olarak enjekte etti . Elektron mikroskobu ile incelendiklerinde, enzimi yalnızca kan damarlarının lümeninde ve endotel hücreleri içindeki mikropinositik veziküllerde buldular. Hücre dışı matrikste endotel dışında hiçbir peroksidaz bulamadılar. Endotel hücreleri arasındaki sıkı bağlantıların beyne geçişi engellediğinden şüpheleniyorlardı .
Edebiyat
- D. Kobiler ve diğerleri: Blood-brain Barrier. Verlag Springer, 2001, ISBN 0-306-46708-9 .
- AG De Boer, W. Sutanto: Kan-Beyin Bariyerinde İlaç Taşınması. CRC Press, 1997, ISBN 90-5702-032-7 .
- WM Pardridge: Kan-beyin Bariyerine Giriş. Cambridge University Press, 1998, ISBN 0-521-58124-9 .
- EM Taylor: Akıntı Taşıyıcıları ve Kan-beyin Bariyeri. Nova Publishers, 2005, ISBN 1-59454-625-8 .
- DJ Begley ve diğerleri: The Blood-Brain Barrier and Drug Delivery to the CNS. Informa Health Care, 2000, ISBN 0-8247-0394-4 .
- E. de Vries, A. Prat: Kan-beyin Bariyeri ve Mikro Ortamı. Taylor ve Francis, 2005, ISBN 0-8493-9892-4 .
- M. Bradbury: Kan-Beyin Bariyeri Kavramı. Wiley-Interscience, 1979, ISBN 0-471-99688-2 .
- P. Ramge: Nanopartiküller yardımıyla kan-beyin bariyerini aşmaya yönelik araştırmalar. Shaker Verlag , 1999, ISBN 3-8265-4974-0 .
- P. Brenner: Kan-beyin ve kan-likör bariyerlerinin yapısı. Tez, LMU Münih, 2006
- Yasunobu Arima ve diğerleri: Bölgesel Sinir Aktivasyonu, Kan-Beyin Bariyerini Aşmak için Otomatik Reaktif T Hücreleri için bir Geçidi Tanımlar. İçinde: Hücre . 148, 2012, s. 447-457, doi: 10.1016 / j.cell.2012.01.022 .
İnternet linkleri
- Norman R. Saunders ve diğerleri: Kan-beyin bariyeri geçirgenliği çalışmalarının doğruları ve yanlışları: 100 yıllık tarih boyunca bir yürüyüş . In: Sinirbilimde Sınırlar . bant 8 , 16 Aralık 2014, doi : 10.3389 / fnins.2014.00404 , PMID 25565938 .
Bireysel kanıt
- ↑ a b c d e f g h i j S. Wolf ve diğerleri: Kan-beyin bariyeri: serebral mikro sirkülasyon sisteminin özel bir özelliği. İçinde: Naturwissenschaften 83, 1996, s. 302-311. doi: 10.1007 / BF01152211 .
- ↑ W. Risau ve diğerleri: Kan-beyin bariyerinin immün işlevi: in vitro sıçan beyni mikrovasküler endotelyum tarafından protein (oto) antijenlerinin tam sunumunda. İn: Hücre Biyolojisi Dergisi . 110, 1990, s 1757-1766. PMID 1692329 .
- ↑ a b c B. Bauer: İlaçların nüfuzunu ve P-glikoprotein etkileşimini araştırmak için kan-beyin bariyerinin in vitro hücre kültürü modelleri. Tez, Ruprecht-Karls-Universität Heidelberg, 2002.
- ↑ a b c d e f g h i j S. Ohtsuki: Kan-beyin bariyeri taşıyıcılarının yeni yönleri; merkezi sinir sistemindeki fizyolojik rolleri İçinde: Biol Pharm Bull . 27, 2004, s. 1489-1496. PMID 15467183 (İnceleme).
- ↑ a b c d e M. Bundgaard. NJ Abbott: Tüm omurgalılar, 4-500 milyon yıl önce bir glial kan-beyin bariyeriyle yola çıktı. İçinde: Glia . 56, 2008, s. 699-708. PMID 18338790 .
- ↑ a b c d e W. M. Pardridge: Kan-beyin bariyerinin moleküler biyolojisi. İçinde: Mol Biotechnol , 30, 2005, s. 57-69. PMID 15805577 (İnceleme).
- ^ JC Lee: Kan-beyin bariyeri fenomeni kavramındaki evrim. In: Nöropatolojide ilerleme . Cilt 1. Verlag Grune ve Stratton, 1971, ISBN 0-88167-188-6 , s. 84-145.
- ↑ a b c M. Pavelka, J. Roth: Fonksiyonel üst yapı. Verlag Springer, ISBN 3-211-83563-6 , s. 234-235.
- ↑ J. Cervos-Navarro: Serebral korteksin kılcal damarlarında elektron mikroskobik bulgular. İçinde: Arch Psychiatr Nervenkr 204, 1963, s. 484-504. PMID 14082797 .
- ↑ a b c d B. T. Hawkins ve TP Davis: Sağlık ve hastalıkta kan-beyin bariyeri / nörovasküler birim. In: Pharmacol Rev 57, 2005, s 173-185.. PMID 15914466 (İnceleme).
- ↑ a b c d e f g h i j k S. Nobmann: Kan-beyin bariyerinin in vitro modeli olarak izole edilmiş beyin kılcal damarları. Tez, Ruprecht-Karls-Universität Heidelberg, 2001.
- ↑ RS el-Bacha, A. Minn: Serebrovasküler endotel hücrelerinde ilaç metabolize eden enzimler beyne metabolik bir koruma sağlar. İçinde: Cell Mol Biol 45, 1999, s. 15-23. PMID 10099836 (İnceleme).
- ↑ M. Chat ve diğerleri: Primer ve ölümsüzleştirilmiş sıçan beyin endotel hücrelerinde ilaç metabolize eden enzim aktiviteleri ve süperoksit oluşumu. İçinde: Life Sci 62, 1998, s. 151-163. PMID 9488113 .
- ↑ A. Minn ve diğerleri: Beyindeki ve serebral mikrodamarlarda ilaç metabolize eden enzimler. İçinde: Brain Res Brain Res Rev 116, 1991, s. 65-82. PMID 1907518 (İnceleme).
- ↑ a b c d Y. Takahura ve diğerleri: Kan-beyin bariyeri: izole edilmiş beyin kılcal damarlarında ve kültürlenmiş beyin endotel hücrelerinde taşıma çalışmaları. İn: Adv Pharmacol 22, 1991, s 137-165.. PMID 1958501 (İnceleme).
- ↑ S. Meresse ve diğerleri: Sığır beyin endotel hücreleri, uzun süreli kültürde sıkı bağlantılar ve monoamin oksidaz aktivitesi ifade eder. İn: , J Neurochem 53, 1989, s 1363-1371.. PMID 2571674 .
- ↑ R. Perrin ve diğerleri: Sıçan beyin bölgelerinde, hücre altı fraksiyonlarında ve izole edilmiş serebral mikrodamarlarda sitokrom P450 aktivitelerinin alkoxyresorufin türevlerine doğru dağılımı. İn: Biochem Pharmacol 40, 1990, s 2145-2151.. PMID 2242042 .
- ↑ R. Bendayan ve diğerleri: Kan beyin bariyerinde P-glikoproteinin fonksiyonel ifadesi ve lokalizasyonu. İçinde: Microsc Res Tech 57, 2002, s. 365-380. PMID 12112443 (İnceleme).
- ↑ Y. Su, PJ Sinko: Kan-beyin bariyerini aşan ilaç dağıtımı: neden zor? nasıl ölçülür ve geliştirilir? İçinde: Expert Opin Drug Deliv 3, 2006, s. 419-435. PMID 16640501 (İnceleme).
- ^ A b H. Fischer et al.: Kan-beyin bariyeri geçirgenliği: pasif difüzyonu yöneten moleküler parametreler. İçinde: J Membr Biol 165, 1998, s. 201-211. PMID 9767674 .
- ↑ a b U. Fagerholm: Son derece geçirgen kan-beyin bariyeri: beyin alım kapasitesi hakkındaki mevcut görüşlerin bir değerlendirmesi. In: Drug Discovery Today 12, 2007, s.1076-1082. PMID 18061888 (İnceleme).
- ↑ B. Nico ve diğerleri: Kan-beyin bariyerinin gelişimi ve bütünlüğünde aquaporin-4 su kanalının rolü. İçinde: J Cell Sci 114, 2001, s. 1297-1307. PMID 11256996 .
- ↑ a b A. M. Butt ve diğerleri: Anestezi uygulanmış sıçanlarda kan-beyin bariyeri boyunca elektrik direnci: gelişimsel bir çalışma. İn: J Physiol 429, 1990, s 47-62.. PMID 2277354 .
- ^ P. Claude, DA Goodenough: Sıkı ve sızdıran epitelden zona occludentes'in kırık yüzleri. İçinde: J Cell Biol , 58, 1973, s. 390-400. PMID 4199658 .
- ^ H. Wolburg ve diğerleri: Kan-beyin bariyeri endotel hücrelerinde sıkı bağlantı yapısının modülasyonu. Doku kültürünün, ikinci habercilerin ve ortak kültürlü astrositlerin etkileri. İçinde: J Cell Sci 107, 1994, s. 1347-1357. PMID 7929640 .
- ↑ a b H. B. Newton: Beyin tümörlerine ilaç verilmesini iyileştirme stratejilerindeki gelişmeler. İçinde: Expert Rev Neurother 6, 2006, s. 1495-1509. PMID 17078789 (İnceleme).
- ↑ JL Madara: Sıkı bağlantı dinamikleri: Parasellüler taşıma düzenleniyor mu? İçinde: Cell 53, 1988, s. 497-498. PMID 3286009 .
- ^ HC Bauer ve diğerleri: Kan-beyin bariyerindeki sıkı bağlantıların proteinleri. İçinde: Sağlık ve Hastalıkta Kan-Omurilik ve Beyin Engelleri . Verlag Elsevier, 2004, s. 1-10.
- ↑ R. Cecchell ve diğerleri: İlaç keşfi ve geliştirilmesinde kan-beyin bariyerinin modellenmesi. İn: Nat Rev Drug Discov , 6, 2007, sayfalar 650-661.. PMID 17667956 (İnceleme).
- ↑ K. Madde, MS Balda: Holey bariyeri: klozinler ve beyin endotelyal geçirgenliğinin düzenlenmesi. İn: J Celi Biol , 161, 2003, sayfa 459-460.. PMID 12743096 (İnceleme).
- ↑ T. Nitta ve diğerleri: Claudin-5 eksikliği olan farelerde kan-beyin bariyerinin boyut seçici gevşemesi. İn: J Celi Biol , 161, 2003, sayfa 653-660.. PMID 12743111 .
- ↑ a b P. Dore-Duffy: Perisitler: kan beyin bariyerinin pluripotent hücreleri. İçinde: Curr Pharm Des 14, 2008, s. 1581-1593. PMID 18673199 (İnceleme).
- ^ R. Balabanov, P. Dore-Duffy: CNS mikrovasküler perisitin kan-beyin bariyerindeki rolü. İn: J Neurosci Res 53, 1998, sayfa 637-644.. PMID 9753191 (İnceleme).
- ↑ a b c d H.K. Rucker ve diğerleri: CNS perisitlerinin hücresel mekanizmaları. İçinde: Brain Res Bull 51, 2000, s. 363-369. PMID 10715555 (İnceleme).
- ^ PA D'Amore: Perisitlerin Kültürü ve Çalışması. İçinde: Kalp ve Damar Araştırmalarında Hücre Kültürü Teknikleri . Verlag Springer, 1990, ISBN 3-540-51934-3 , s.299 .
- ↑ NJ Abbott: Nörobiyoloji: Glia ve kan-beyin bariyeri. İçinde: Nature , 325, 1987, s. 195. PMID 3808015 .
- ^ CH Lai, KH Kuo: In vitro BBB modelini oluşturmak için kritik bileşen: Pericyte. In: Brain Res Brain Res Rev , 50, 2005, s. 258-265. PMID 16199092 (İnceleme).
- ↑ a b D. Shepro, NM Morel: fizyoloji perisiti . İçinde: FASEB J , 7, 1993, s. 1031-1038. PMID 8370472 (İnceleme).
- ↑ K. Fujimoto: Sıçan serebral kılcal damarlarının geliştirilmesinde perisit-endotelyal boşluk bağlantıları: İnce bir yapısal çalışma. İçinde: Anat Rec 242, 1995, s. 562-565. PMID 7486026 .
- ↑ L. Diaz-Flores: Mikrovasküler perisitler: Morfolojik ve fonksiyonel özelliklerinin bir incelemesi. İçinde: Histol Histopath 6, 1991, s. 269-286. PMID 1802127 (İnceleme).
- ↑ DE Sims: Perisit biyolojisindeki son gelişmeler - Sağlık ve hastalık için çıkarımlar. İçinde: Can J Cardiol 7, 1991, s. 431-443. PMID 1768982 (İnceleme).
- ↑ a b c D. E. Sims: Perisitlerdeki çeşitlilik. İn: Clin Exp Pharmacol Physiol 27, 2000, sayfa 842-846.. PMID 11022980 (İnceleme).
- ↑ IM Herman, PA D'Amore: Mikrovasküler perisitler, kas ve kas dışı aktinler içerir. İn: J Celi Biol , 101, 1985, sayfa 43-52.. PMID 3891763 .
- ↑ KK Hirschi, PA D'Amore: Mikrovaskülatürdeki perisitler. İçinde: Cardiovasc Res , 32, 1996, s. 687-698. PMID 8915187 (İnceleme).
- ↑ M. Mato ve diğerleri: Beyindeki floresan granüler peritel hücrelerinin yüksek moleküler ağırlıklı atık ürünlerin temizleyicileri olarak olası işlevi için kanıt. İçinde: Experientia 40, 1984, s. 399-402. PMID 6325229 .
- ↑ R. Balabanov ve diğerleri: CNS mikrovasküler perisitler, makrofaj benzeri işlevi, hücre yüzeyi integrini alfaM'yi ve makrofaj markörü ED-2'yi ifade eder. İn: Microvasc Res 52, 1996, s 127-142.. PMID 8901442 .
- ↑ WF Hickey ve H. Kimura: CNS'nin perivasküler mikroglial hücreleri kemik iliğinden türetilmiştir ve in vivo olarak antijen sunar. İçinde: Science 239, 1988, s. 290-292. PMID 3276004 .
- ↑ Z. Fabry ve diğerleri: Th1 ve Th2 CD4 + hücrelerinin murin beyin mikrodamar endotel hücreleri ve düz kas / perisitler tarafından diferansiyel aktivasyonu. İn: J Immunol 151, 1993, s 38-47.. PMID 8100844 .
- ↑ D. Krause ve diğerleri: Serebral perisitler - kan-beyin bariyeri peptit metabolizmasının kontrolünde ikinci bir savunma hattı. İçinde: Adv Exp Med Biol 331, 1993, s. 149-152. PMID 8101424 .
- ^ WE Thomas: Beyin makrofajları: perisitlerin ve perivasküler hücrelerin rolü üzerine. In: Brain Res Brain Res Rev 31, 1999, s. 42-57. PMID 10611494 (İnceleme).
- ↑ C. Iadecola: Normal beyinde ve Alzheimer hastalığında nörovasküler düzenleme. In: Nat Rev Neurosci 5 2004, s 347-360.. PMID 15100718 (İnceleme).
- ^ B. Engelhardt: Kan-beyin bariyerinin gelişimi. İçinde: Cell Tissue Res 314, 2003, s. 119-129. PMID 12955493 (İnceleme).
- ^ CE Johanson: Gelişmekte olan beynin geçirgenliği ve vaskülaritesi: serebelluma karşı serebral korteks. İçinde: Brain Res 190, 1980, s. 3-16. PMID 6769537 .
- ^ J. Neuhaus ve diğerleri: Transfiltre kok kültüründe sıçan astroglial hücreleri tarafından sığır beyin endotel hücrelerinde kan-beyin bariyeri özelliklerinin indüksiyonu. İçinde: Ann NY Acad Sci 633, 1991, s. 578-580. PMID 1789585 .
- ↑ PA Stewart, MJ Wiley: Gelişen sinir dokusu, istilacı endotel hücrelerinde kan-beyin bariyeri özelliklerinin oluşumunu indükler: bıldırcın-civciv transplantasyon kimeralarının kullanıldığı bir çalışma. İçinde: Dev Biol , 84, 1981, s. 183-192. PMID 7250491 .
- ^ TJ Raub ve diğerleri: İn vitro sığır beyin mikrodamar endotel hücrelerinin geçirgenliği: astroglioma hücrelerinden salınan bir faktör tarafından bariyer sıkılaştırma. İçinde: Exp Celi Res , 199, 1992, s. 330-340. PMID 1347502 .
- ↑ a b c d N. J. Abbott: Astrosit-endotel etkileşimleri ve kan-beyin bariyeri geçirgenliği. İçinde: J Anat 200, 2002, s.629-638. PMID 12162730 (İnceleme).
- ↑ a b O. B. Paulson, EA Newman: Astrosit ayak parmaklarından potasyum salınımı serebral kan akışını düzenler mi? İçinde: Science , 237, 1987, s. 896-898. PMID 3616619 .
- ↑ NJ Abbott ve diğerleri: Kan-beyin bariyerinde astrosit-endotel etkileşimleri. In: Nat Rev Neurosci , 7, 2006, s 41-53.. PMID 16371949 (İnceleme).
- ↑ I. Björkhem, S. Meaney: Beyin Kolesterolü: Bir Bariyerin Ardındaki Uzun Gizli Yaşam. In: Arteriosder Thromb Vase Biol , 24, 2004, s 806-815.. PMID 14764421 (İnceleme).
- ↑ HM Duvernoy, PY Risold: Çevresel ventriküler organlar: karşılaştırmalı anatomi ve vaskülarizasyon atlası. İçinde: Brain Res Rev 56, 2007, s. 119-147. PMID 17659349 (İnceleme).
- ↑ C. Lohmann: İn vitro kan-beyin bariyeri: matris metaloproteazlar tarafından geçirgenliğin düzenlenmesi. Tez, Westfälische Wilhelms-Universität Münster, 2003.
- ↑ Dünya Kupası Pardridge: Beyne Peptid İlaç Verilmesi . Raven Press, 1991, ISBN 0-88167-793-0 , s.123.
- ↑ WL Chiou, A. Barve: 64 ilacın emilen oral doz fraksiyonunun insanlar ve sıçanlar arasında doğrusal korelasyonu. İn: Pharm Res , 15, 1998, s 1792-1795.. PMID 9834005 .
- ^ JT Goodwin ve DE Clark: Kan-beyin bariyeri penetrasyonunun in siliko tahminleri: "akılda tutulması" gereken hususlar. İçinde: J Pharmacol Exp Ther 315, 2005, s. 477-483. PMID 15919767 (İnceleme).
- ^ SL Lindstedt ve PJ Schaeffer: Memelilerin anatomik ve fizyolojik parametrelerini tahmin etmede allometrinin kullanımı. İçinde: Lab Anim 36, 2002, sayfa 1-19. PMID 11833526 .
- ↑ RW Leggett, LR Williams: Referans adam için önerilen bir kan dolaşım modeli. In: Health Phys , 69, 1995, s. 187-201. PMID 7622365 .
- ^ S. Willmann ve diğerleri: İnsanlarda absorbe edilen fraksiyon dozunun tahmini için fizyolojik bir model. In: J Med Chem 47, 2004, s. 4022-4031. PMID 15267240 .
- ↑ U. Fagerholm ve diğerleri: Sıçan ve insan jejunumunda geçirgenlik katsayıları arasındaki karşılaştırma. İn: Pharm Res , 13, 1996, s 1336-1342.. PMID 8893271 .
- ↑ RW Leggett, LR Williams: İnsanlarda bölgesel kan hacimleri için önerilen referans değerleri. In: Health Phys , 60, 1991, s. 139-154. PMID 1989937 .
- ↑ GB Wislocki: Fetal absorpsiyon üzerine deneysel çalışmalar. I. Hayati boyanmış fetüs. İn: Katkı Embryol Carnegie Inst , 5, 1920, sayfa 45-52..
- ↑ S. Wakai, N. Hirokawa: Civciv embriyosunda yaban turpu peroksidazına karşı kan-beyin bariyerinin gelişimi. İçinde: Cell Tissue Res , 195, 1979, s. 195-203. PMID 737715 .
- ^ W. Risau ve diğerleri: Kan-beyin bariyerinin gelişimi sırasında beyin endotelyumundaki proteinlerin farklılaşmaya bağlı ifadesi. İçinde: Dev Biol 117, 1986, s. 537-545. PMID 2875908 .
- ↑ ML Reynolds ve diğerleri: Preterm koyun fetüsünde intrakraniyal hemoraji. İçinde: Early Hum Dev 3, 1979, s. 163-186. PMID 575326 .
- ↑ L. Stern ve R. Peyrot: Le fonctionnement de la barrière hémato-éncephalique aux divers stades de développement chez les diverses espèces hayvanlar. İçinde: Compte Rendu des Societe de Biologie (Paris) 96, 1927, s. 1124-1126.
- ↑ L. Stern ve diğerleri: Le fonctionnement de la barrière hémato-éncephalique chez les nouveau-nés. İçinde: Compte Rendu Soc Biol 100, 1929, s. 231-233.
- ↑ a b N. R. Saunders ve diğerleri: Beyindeki bariyer mekanizmaları, II. Olgunlaşmamış beyin. İn: Clin Exp Pharmacol Physiol 26, 1999, sayfa 85-91.. PMID 10065326 (İnceleme).
- ^ NR Saunders: Makromoleküllere kan-beyin bariyerinin gelişimi. In: The Fluids and Barriers of the Eye and Brain Editor: MB Segal, Verlag MacMillan, 1991, ISBN 0-8493-7707-2 , s. 128-155.
- ↑ U. Schumacher, K. Møllgård: Çoklu ilaç direnci P-glikoprotein (Pgp, MDR1), gelişmekte olan insan beyninin mikrodamarlarında kan-beyin bariyeri gelişiminin erken bir belirtecidir. İn: Histochem Celi Biol , 108, 1997, sayfa 179-182. PMID 9272437 .
- ↑ KM Dziegielewska et al.: Fetal koyunlarda lipitte çözünmeyen moleküllere beyin bariyer sistemlerinin geliştirilmesi üzerine çalışmalar. İn: J Physiol , 292, 1979, s 207-231.. PMID 490348 .
- ^ RK Ferguson, DM Woodbury: Gelişmekte olan sıçanların beyin, beyin omurilik sıvısı ve iskelet kasına 14C-inulin ve 14C-sükrozun penetrasyonu. In: Exp Brain Res , 7, 1969, s. 181-194. PMID 5795246 .
- ^ MD Habgood ve diğerleri: Sıçanlarda doğum sonrası beyin gelişimi sırasında kan-beyin omurilik sıvısı bariyeri değişimindeki azalmanın doğası. İn: J Physiol 468, 1993, s 73-83.. PMID 8254533 .
- ^ CE Johanson: Kan-beyin bariyerinin doğası. In: Implications of the Blood-Brain Barrier and Its Manipulation Editor: EA Neuwelt, Plenum Press, 1989, s. 157-198.
- ↑ LD Braun ve diğerleri: Yeni doğmuş tavşan kan-beyin bariyeri seçici olarak geçirgendir ve yetişkinden önemli ölçüde farklıdır. İçinde: J Neurochem 34, 1980, s. 147-152. PMID 7452231 .
- ^ EM Cornford ve diğerleri: Beyindeki değişen beslenme gereksinimlerinin bir göstergesi olarak kan-beyin bariyeri geçirgenliğinin gelişimsel modülasyonları. İn: Pediatr Res 16, 1982, s 324-328.. PMID 7079003 .
- ↑ DP Brenton, RM Gardiner: L-fenilalanin ve ilgili amino asitlerin koyun kan-beyin bariyerinde taşınması. İn: J Physiol , 402, 1988, sayfa 497-514.. PMID 3236248 .
- ↑ HJL Frank ve diğerleri: Yeni doğan tavşanlarda in vivo kan-beyin bariyerine ve in vitro beyin mikrodamarlarına gelişmiş insülin bağlanması. İçinde: Diabetes , 34, 1985, s. 728-733. PMID 3894116 .
- ^ NR Saunders: Olgunlaşmamış beyindeki engeller. İçinde: Cell Mol Neurobiol , 20, 2000, s. 29-40. PMID 10690500 (İnceleme).
- ↑ NJ Abbott, M. Bundgaard: Mürekkep balığı, Sepia officinalis'te bir kan-beyin bariyeri için elektron yoğun izleme kanıtı. İn: J Neurocytol , 21, 1992, s 276-294.. PMID 1588347 .
- ↑ NJ Abbott, Y. Pichon: Kabuklular ve kafadanbacaklıların glial kan-beyin bariyeri: bir inceleme. İn: J Physiol (Paris) , 82, 1987, s 304-313.. PMID 3332691 (İnceleme).
- ↑ a b N. J. Abbott: CNS engellerinin dinamiği: evrim, farklılaşma ve modülasyon. İçinde: Cell Mol Neurobiol 25, 2005, sayfa 5-23. PMID 15962506 (İnceleme).
- ↑ NJ Abbott: Kan-beyin bariyerinin karşılaştırmalı fizyolojisi. In: Kan - beyin bariyerinin fizyolojisi ve farmakolojisi Editör: MWB Bradbury, Springer-Verlag, 1992, ISBN 0-387-54492-5 , s. 371-396.
- ^ T. Stork ve diğerleri: Drosophila'daki kan-beyin bariyerinin organizasyonu ve işlevi. İçinde: J Neurosci 28, 2008, s.587-597. PMID 18199760 .
- ↑ J. Fraher ve E. Cheong: bir geçiş siklostomunun merkezi-periferik sinir sistemindeki glial-Schwann hücre uzmanlıkları: ultra yapısal üzerine çalışma. İn: Açta Anat 154, 1995, s 300-314.. PMID 8773716 .
- ↑ NJ Abbott ve diğerleri: Kan-beyin bariyerinin karşılaştırmalı fizyolojisi. İçinde: Sağlık ve hastalıkta kan-beyin engeli. Editörler: AJ Suckling ve diğerleri, Ellis Horwood Verlag, 1986, s. 52-72.
- ↑ F. Miragall ve diğerleri: Koku alma sistemindeki sıkı bağlantı proteini ZO-1'in ifadesi: Koku alma duyu nöronları ve glial hücreler üzerinde ZO-1 varlığı. İn: J Comp Neurol 341, 1994, s 433-448.. PMID 8201022 .
- ↑ a b c N. Hettenbach: Cep telefonu radyasyonuna (GSM ve UMTS) kronik elektromanyetik maruziyetin sıçanlarda kan-beyin bariyerinin bütünlüğü üzerindeki etkisi. Tez, Ludwig Maximilians Üniversitesi Münih, 2008.
- ^ SI Rapoport: Fizyoloji ve Tıpta Kan-beyin Bariyeri. Raven Press, 1976, ISBN 0-89004-079-6 .
- ↑ a b c M. Fromm: İnsan fizyolojisi - zarlarda ve epitelde taşıma. (Editör: RF Schmidt, F. Lang), Verlag Springer, ISBN 978-3-540-32908-4 , s. 41-54.
- ↑ I. Sauer: Apolipoprotein E'den türetilmiş peptidler, kan-beyin bariyerini aşmak için vektörler olarak. Tez FU Berlin, 2004. urn : nbn: de: kobv: 188-2004003141
- ↑ a b R. D. Egleton, TP Davis: Nöropeptid ilaçların geliştirilmesi kan-beyin bariyerini aştı . İçinde: NeuroRx 2, 2005, s. 44-53 . PMID 15717056 (İnceleme).
- ^ WH Oldendorf: Lipid çözünürlüğü ve kan-beyin bariyerinin ilaç penetrasyonu. İçinde: Proc Soc Exp Biol Med 147, 1974, s. 813-816. PMID 4445171 .
- ↑ a b c R. Kaliszan ve M. Markuszewski: Beyin / kan dağılımı Bölme katsayısı ve moleküler kütlenin bir kombinasyonu ile tanımlanır. In: International Journal of Pharmaceutics 145, 1996, s. 9-16. doi: 10.1016 / S0378-5173 (96) 04712-6 .
- ^ H. Träuble: Membranlarda taşıyıcılar ve özgüllük. 3. Taşıyıcı tarafından kolaylaştırılan taşıma. Membranlarda taşıyıcı olarak kıvrımlar. In: Neurosci Res Program Bull 9, 1971, s. 361-372. PMID 5164654 .
- ^ H. Träuble: lipidlerdeki faz değişiklikleri. Biyolojik zarlarda olası anahtarlama süreçleri. İçinde: Naturwissenschaften 58, 1971, s. 277–284. PMID 4935458 (İnceleme).
- ↑ O. Vostowsky: Doğal ürünlerin kimyası - lipoproteinler ve zarlar. Erlangen Üniversitesi, 2005, s.42.
- ^ W. Hoppe, RD Bauer: Biophysik. Verlag Birkhäuser , 1982, ISBN 0-387-11335-5 , s. 447-448.
- ^ A. Seelig ve J. Seelig: Döteryum manyetik rezonansı ile ölçülen bir fosfolipid çift tabakasındaki yağlı asil zincirlerinin dinamik yapısı. İçinde: Biochemistry 13, 1974, s. 4839-4845. PMID 4371820 .
- ↑ A. Elbert: Küçük polar moleküllerin fosfolipid model membranlardan geçirgenliği. Tez, Kaiserslautern Üniversitesi, 1999. urn : nbn: de: bsz: 386-kluedo-12797
- ^ VA Levin: Oktanol / su bölme katsayısı ve moleküler ağırlığın sıçan beyni kılcal geçirgenliği ile ilişkisi. İn: J Med Chem 23, 1980, sayfa 682-684.. PMID 7392035 .
- ↑ A. Seelig ve diğerleri: İlaçların kan-beyin bariyerinden yayılma yeteneğini belirleyen bir yöntem. İçinde: PNAS 91, 1994, s. 68-72. PMID 8278409 .
- ↑ a b G. A. Dhopeshwarkar ve JF Mead: Yağ asitlerinin beyne alınması ve taşınması ve kan-beyin bariyer sisteminin rolü. İçinde: Adv Lipid Res 11, 1973, s. 109-142. PMID 4608446 (İnceleme).
- ↑ G. Gerebtzoff, A. Seelig: Ana parametre olarak hesaplanan moleküler kesit alanı kullanılarak kan-beyin bariyeri geçirgenliğinin siliko tahmininde. In: AJ Chem Inf Modeli , 46, 2006, s 2638-2650.. PMID 17125204 .
- ↑ a b W. W. Pardridge: Kan-beyin bariyeri: beyin ilacı gelişimindeki darboğaz. İçinde: NeuroRx 2, 2005, sayfa 3-14. PMID 15717053 (İnceleme).
- ↑ a b W. H. Oldendorf: Bir tritiatlı su iç standardı kullanılarak radyo etiketli maddelerin beyin alımının ölçülmesi. İçinde: Brain Res , 24, 1970, s.372-376. PMID 5490302 .
- ↑ D. Dolman ve diğerleri: Kültürde sıçan birincil beyin mikrodamar endotel hücrelerinde aquaporin 1'in indüksiyonu ancak aquaporin 4 haberci RNA'nın indüksiyonu. İçinde: J Neurochem 93, 2005, s. 825-833. PMID 15857386 .
- ^ O. Bloch ve GT Manley: Serebral su taşınmasında ve ödemde aquaporin-4'ün rolü. In: Neurosurg Focus 22, 2007, s. E3 PMID 17613234 (Gözden Geçirme).
- ↑ AS Verkman: Su kanallarından daha fazlası : akuaporinlerin beklenmedik hücresel rolleri. İçinde: J Cell Sci 118, 2005, s. 3225-3232. PMID 16079275 (İnceleme).
- ↑ a b J. Badaut ve diğerleri: Beyindeki akuaporinler: su kemerinden "çok kanala". İçinde: Metab Brain Dis 22, 2007, s. 251-263. PMID 17701333 (İnceleme).
- ↑ Farrell ve diğerleri: Kan-beyin bariyeri glikoz taşıyıcısı, beyin kılcal endotelyal lümenal ve ablumenal membranlar üzerinde asimetrik olarak dağıtılır: Bir elektron mikroskobik immünogold çalışması . İçinde: Proc. Natl. Acad. Sci. USA , Cilt 88, 1991, sayfa 5779-5783.
- ^ A. Dahlin, J. Royall, JG Hohmann, J. Wang: Fare Beyninde Çözünen Taşıyıcı (SLC) Gen Ailesinin İfade Profili. İn: J. Pharmacol. Exp Ther. 329, 2009, s. 558-570 PMID 19179540 PMC 267287 (ücretsiz tam metin).
- ↑ D. Agus ve diğerleri: C vitamini, kan-beyin bariyerini oksitlenmiş formda glikoz taşıyıcıları yoluyla geçer. İçinde: J Clin Invest 100, 1997, s. 2842-2848. PMID 9389750 .
- ↑ EM Cornford ve S. Hyman: Küçük ve büyük moleküllere kan-beyin bariyeri geçirgenliği. In: Advanced Drug Delivery Reviews 36, 1999, s. 145-163. PMID 10837713 (İnceleme).
- ↑ BV Zlokovic ve diğerleri: perfüze kobay beynindeki kan-beyin bariyerinden lösin-enkefalinin taşınması . İçinde: J Neurochem 49, 1987, s. 310-315. PMID 3585338 .
- ↑ BV Zlokovic ve diğerleri: Yerinde perfüze edilmiş bir kobay beyninin kan-beyin bariyerinin lümen tarafında lösin-enkefalin hücresel alımının kinetik analizi. İn: , J Neurochem 53, 1989, s 1333-1340.. PMID 2795003 .
- ↑ BV Zlokovic ve diğerleri: Kan -beyin bariyerinde arginin-vazopressin alımının kinetiği. İçinde: Biochim Biophys Açta 1025, 1990, s. 191-198. PMID 2364078 .
- ^ SA Thomas ve diğerleri: [D-penisilamin2,5] enkefalinin merkezi sinir sistemine girişi: doygunluk kinetiği ve özgüllük. İçinde: J Pharmacol Exp Ther 280, 1997, s. 1235-1240. PMID 9067309 .
- ↑ VV Rao ve diğerleri: MDR1 P glikoproteinin koroid pleksus epitel ekspresyonu ve çoklu ilaç direnci ile ilişkili protein, kan-beyin omurilik sıvısı ilaç geçirgenliği bariyerine katkıda bulunur. İçinde: PNAS 96, 1999, s. 3900-3905. PMID 10097135 .
- ↑ F. Thiebaut ve diğerleri: Çoklu ilaç taşıma proteini P170'de farklı epitopların normal dokularında immünohistokimyasal lokalizasyon: beyin kılcal damarlarında lokalizasyon için kanıt . İçinde: J Histochem Cytochem 37, 1989, s. 159-164, PMID 2463300 .
- ^ DJ Begley: ABC taşıyıcıları ve kan-beyin bariyeri. İçinde: Curr Pharm Des 10, 2004, s. 1295-1312. PMID 15134482 (İnceleme).
- ↑ S. Seetharaman ve diğerleri: İzole edilmiş insan beyni mikrodamarlarında ve bu izolatlardan kültürlenen hücrelerde çoklu ilaç direnci ile ilgili taşıma proteinleri. İçinde: J Neurochem 70, 1998, s. 1151-1159. PMID 9489736 .
- ↑ a b H.C. Cooray ve diğerleri: İnsan beyninin mikrodamar endotelyumunda meme kanseri direnç proteininin lokalizasyonu. İçinde: Neuroreport 13, 2002, s. 2059-2063. PMID 12438926 .
- ^ T. Eisenblätter ve HJ Galla: Kan-beyin bariyerinde yeni bir çoklu ilaç direnci proteini. İçinde: Biochem Biophys Res Commun 293, 2002, s. 1273-1278. PMID 12054514 .
- ^ Y. Tanaka ve diğerleri: İnsan gliomalarında kılcal endotelyal hücreler üzerinde P-glikoproteinin ultrastrüktürel lokalizasyonu. İçinde: Virchows Arch 425, 1994, s. 133-138. PMID 7952498 .
- ↑ EC de Lange: ABC taşıyıcılarının kan-CSF bariyerinde bir detoksifikasyon sistemi olarak potansiyel rolü. İçinde: Adv Drug Deliv Rev 56, 2004, s. 1793-1809. PMID 15381334 (İnceleme).
- ↑ H. Wolosker ve diğerleri: Aynanın içinden nörobiyoloji : Yeni bir glialden türetilmiş verici olarak D-serin. İçinde: Neurochem Int , 41, 2002, s. 327-332. PMID 12176074 (İnceleme).
- ↑ CF Zorumski ve JW Olney: Eksitotoksik nöronal hasar ve nöropsikiyatrik bozukluklar : Pharmacol Ther 59, 1993, s. 145-162. PMID 7904075 (İnceleme).
- ↑ K. Hosoya ve diğerleri: Kan-beyin bariyeri, önemli ölçüde L-aspartik asit akışı üretir, ancak D-aspartik asit üretmez: beyin efluks indeksi yöntemini kullanan in vivo kanıt. İn: , J Neurochem , 73, 1999, sayfa 1206-1211.. PMID 10461913 .
- ↑ M. Palacin ve diğerleri: Memeli plazma membran amino asit taşıyıcılarının moleküler biyolojisi. İçinde: Physiol Rev , 78, 1998, s. 969-1054. PMID 9790568 (İnceleme).
- ^ W. Löscher ve H. Potschka: Kan-beyin bariyeri aktif dışa akım taşıyıcıları: ATP-bağlayıcı kaset gen ailesi. İçinde: NeuroRx , 2, 2005, s. 86-98. PMID 15717060 (İnceleme).
- ↑ DM Tishler ve diğerleri: Tıbbi olarak inatçı epilepsili hastaların beyninde MDR1 gen ekspresyonu. İn: Epilepsia , 36, 1995, s 1-6.. PMID 8001500 .
- ↑ H. Kusuhara ve diğerleri: Fare beyninden yeni bir multispesifik organik anyon taşıyıcısının moleküler klonlaması ve karakterizasyonu. İn: J. Biol Chem , 274, 1999, s 13.675-13.680.. PMID 10224140 .
- ↑ B. Gao ve diğerleri: Sıçan beyninin kılcal endotelyumunda ve koroid pleksus epitelinde organik anyon taşıyan polipeptit 2'nin (Oatp2) lokalizasyonu. ( Memento 5 Eylül 2008 , Internet Archive ) 'de: J Histochem, Cytochem , 47, 1999, sayfalar 1255-1264.. PMID 10490454 .
- ^ LZ Bito: Kan-Beyin Bariyeri: Kan ve Beynin Ekstraseliüler Sıvısı Arasında Aktif Katyon Taşınmasına İlişkin Kanıt. İçinde: Science 165, 1969, s. 81-83. PMID 17840696 .
- ↑ Y. Kido ve diğerleri: Karnitin taşıyıcısı OCTN2'nin kan-beyin bariyerindeki L-karnitin ve asetil-L-karnitinin beyin dağılımı ile fonksiyonel ilişkisi. İçinde: J Neurochem 79, 2001, s. 959-969. PMID 11739607 .
- ^ RL Roberts ve diğerleri: Kan-beyin bariyerinde transferrinin reseptör aracılı endositozu. İçinde: J Cell Sci 104, 1993, s. 521-532. PMID 8505377 .
- ↑ B. Dehouck ve diğerleri: Kan-beyin bariyerinde düşük yoğunluklu lipoprotein reseptörünün yukarı regülasyonu: beyin kılcal endotel hücreleri ve astrositler arasındaki iletişim. İçinde: J Cell Biol 126, 1994, s. 465-473. PMID 8034745 .
- ↑ KR Duffy ve diğerleri: İnsan kan-beyin bariyeri insülin benzeri büyüme faktörü reseptörü. In: Metabolism 37, 1988, s. 136-140. PMID 2963191 .
- ↑ MW Smith ve M. Gumbleton: Kan-beyin bariyerinde endositoz: temel anlayıştan ilaç verme stratejilerine kadar. In: J Drug Target 14, 2006, s. 191-214. PMID 16777679 (İnceleme).
- ↑ F. Hervé ve diğerleri: Adsorptif transitoz yoluyla CNS iletimi. İçinde: AAPS J 10, 2008, s. 455-472. PMID 18726697 (İnceleme).
- ↑ JM Scherr adamı: Kan-beyin bariyeri yoluyla beyne ilaç verilmesi. İçinde: Vascul Pharmacol 38, 2002, s. 349-354. PMID 12529929 (İnceleme).
- ↑ I. Tamai ve diğerleri: Kan-beyin bariyerindeki temel peptidlerin adsorptif aracılı endositozu için yapı-içselleştirme ilişkisi. İçinde: J Pharmacol Exp Ther 280, 1997, s. 410-415. PMID 8996222 .
- ↑ a b c d e f g h i j k l m n W. M. Pardridge: Kan-beyin bariyeri iletimi. In: Drug Discov Today 12, 2007, s.54-61 . PMID 17198973 .
- ↑ a b c d e f H. Bronger ve diğerleri: ABCC ilaç dışa akış pompaları ve insan gliomalarında ve kan-tümör bariyerinde organik anyon alım taşıyıcıları. İçinde: Cancer Res 65, 2005, s. 11419-11428. PMID 16357150 .
- ^ H. Kusuhara ve Y. Sugiyama: Kan-beyin bariyeri boyunca aktif akış: çözünen taşıyıcı ailesinin rolü. İçinde: NeuroRx 2, 2005, s. 73-85. PMID 15717059 (İnceleme).
- ↑ JM Scherrmann: Kan-beyin bariyerlerindeki çoklu ilaç direnci taşıyıcılarının ifadesi ve işlevi. İçinde: Expert Opin Drug Metab Toxicol 1, 2005, s. 233-246. PMID 16922639 (İnceleme).
- ↑ N. Bodor ve P. Buchwald: Nörofarmasötiklerin kimyasal dağıtım sistemleri ile beyinde hedeflenmesindeki son gelişmeler. İçinde: Adv Drug Deliv Rev 36, 1999, sayfa 229-254. PMID 10837718 (İnceleme).
- ↑ a b c d e f U. Bickel: Kan-beyin bariyerindeki ilaç taşınması nasıl ölçülür? İçinde: NeuroRx 2, 2005, s. 15-26. PMID 15717054 (İnceleme).
- ^ A b J. Fenstermacher, L. Wei: Kantitatif otoradyografi ile lokal serebral kılcal geçirgenlik yüzey alanı ürünlerinin ölçülmesi. İçinde: Kan-beyin Bariyerine Giriş WM Pardridge (Editör), Cambridge University Press, 1998, ISBN 0-521-58124-9 , s. 122-132.
- ↑ C. Crone ve DG Levitt: Küçük çözünen maddelere kılcal geçirgenlik. In: Handbook of Physiology American Physiological Society, 1984, s. 375-409.
- ↑ H. Pötzsch: Oral kavite ve orofarenksin skuamöz hücreli karsinomunun klinikopatolojik özellikleri bağlamında perfüzyon bilgisayarlı tomografik ölçüm parametreleri. Tez, FU Berlin, 2007.
- ↑ AM Peters: Radyologlar için izleme kinetiğinin temelleri. İn: Br J Radiol 71, 1998, sayfalar 1116-1129.. PMID 10434905 (İnceleme).
- ↑ F. Lasbennes ve diğerleri: Sıçan beyninden izole edilen mikrodamarlarda enerji metabolizması kapasitesi. İçinde: Neurochem Res 9, 1984, s. 1-10. PMID 6325972 .
- ↑ J. Huwyler ve WM Pardridge: Kan-beyin bariyeri transferrin reseptörünün, sabitlenmemiş izole edilmiş sıçan beyin kılcal damarlarının konfokal floresan mikroskobu ile incelenmesi. İn: , J Neurochem 70, 1998, s 883-886.. PMID 9453586 .
- ↑ DS Miller ve diğerleri: Konfokal mikroskopi ile incelenen izole edilmiş beyin mikrodamarları arasında Xenobiyotik taşıma. İçinde: Mol Pharmacol 58, 2000, s. 1357-1367. PMID 11093774 .
- ↑ a b M. Gumbleton ve diğerleri: Kan-beyin bariyeri için bir geçirgenlik taraması olarak hizmet etmek üzere in vitro hücre kültürlerinin kullanımındaki ilerleme ve sınırlamalar. İçinde: J Pharm Sci 90, 2001, s. 1681-1698. PMID 11745727 (İnceleme).
- ^ A. Reichel ve diğerleri: Kan-beyin bariyeri çalışmaları için in vitro tekniklere genel bakış. İçinde: Methods Mol Med 89, 2003, s. 307-324. PMID 12958429 .
- ↑ R. Cecchelli ve diğerleri: Kan-beyin bariyeri boyunca ilaç taşınmasını değerlendirmek için in vitro model. İçinde: Adv Drug Deliv Rev 36, 1999, s. 165-178. PMID 10837714 .
- ↑ D. Hoheisel ve diğerleri: Hidrokortizon, bir serumsuz hücre kültürü sisteminde kan-beyin özelliklerini güçlendirir. İçinde: Biochem Biophys Res Commun 247, 1998, sayfa 312-315. PMID 9679029 .
- ↑ SB Raymond ve diğerleri: Alzheimer Hastalığı Fare Modellerinde Moleküler Görüntüleme ve Terapötik Ajanların Ultrasonla Geliştirilmiş İletimi. İçinde: PLoS ONE 3, 2008, e2175. PMID 18478109 .
- ↑ JD Fenstermacher ve diğerleri: İlaçların kan-beyin sistemi boyunca taşınmasını ölçmek için yöntemler. İçinde: Pharmacol Ther 14, 1981, s. 217-248. PMID 7031708 .
- ^ G. Molema, DKF Meijer: İlaç Hedefleme: Organa Özgü Stratejiler. Wiley-VCH, 2001, ISBN 3-527-29989-0 .
- ↑ JE Hardebo, B. Nilsson: Beyin alım indeksi yöntemi ile dolaşımdaki bileşiklerin serebral ekstraksiyonunun tahmini: dolaşım süresi, hacim enjeksiyonu ve serebral kan akışının etkisi. İn: Açta Physiol Scand 107, 1979, sayfa 153-159.. PMID 525379 .
- ^ Y. Moriki ve diğerleri: Beyin alım indeksi yöntemi kullanılarak sıçanlarda pentazosinin kan-beyin bariyeri taşınmasında P-glikoproteinin rolü . İçinde: Biol Pharm Bull 27, 2004, s. 932-935. PMID 15187451 .
- ↑ LJ Murphey ve GD Olsen: İlaca bağlı solunum depresyonu sırasında morfin-6-beta-D-glukuronidin neonatal kobay beynine difüzyonu. İn: , J Pharmacol Exp Ther 271, 1994, sayfa 118-124.. PMID 7965704 .
- ^ WH Oldendorf ve diğerleri: Nikotinin N-metil kuaternizasyonu ile kaldırılan kan-beyin bariyer penetrasyonu. İçinde: PNAS 90, 1993, s. 307-311. PMID 8419935 .
- ↑ D. Magnani: Kalıcı keratinosit ve melanosit hücre hatlarında yabancı maddelerin bağlanmasının yanı sıra insan saç köklerinden alınan birincil kültürlerin saçtaki yabancı madde alımının in vitro ölçümü için uygunluğunun araştırılması. Tez, Carl von Ossietzky Oldenburg Üniversitesi, 2005. urn : nbn: de: gbv: 715-oops-1151
- ↑ a b E. M. Cornford ve diğerleri: Yenidoğanlarda ve yetişkinlerde lipid aracılı kan-beyin bariyeri penetrasyonunun karşılaştırılması. İçinde: Am J Physiol-Cell Physiol 243, 1982, s. 161C-168C. PMID 7114247 .
- ↑ A. Kakee ve diğerleri: Kan-beyin bariyerinde bir akış pompası olarak işlev gören organik anyon taşıma sistemi: yeni geliştirilmiş bir beyin akış indeksi (BEI) yöntemi ile gösteri. İçinde: Proc Int Symp Control Release Bioact Mater 22, 1995, s. 16-18.
- ↑ a b I. Tamai, A. Tsuji: Kan-beyin bariyerinden ilaç iletimi. İçinde: Adv Drug Deliv Rev 19, 1996, s. 401-424. doi: 10.1016 / 0169-409X (96) 00011-7 (İnceleme).
- ↑ BV Zlokovic et al .: Perfüze kobay beyninde çözünen taşınmanın ölçülmesi. N-metil-alfa-aminoizobütirik aside yöntem uygulaması. İçinde: J Neurochem 46, 1986, s. 1444-1451. PMID 3083044 .
- ↑ D. Triguero ve diğerleri: Dolaşan peptidlerin ve plazma proteinlerinin kan-beyin bariyeri taşınmasının nicelendirilmesi için kılcal tükenme yöntemi. İn: , J Neurochem 54, 1990, s 1882-1888.. PMID 2338547 .
- ↑ C. Crone: 'Gösterge Difüzyonu' yöntemi kullanılarak belirlenen çeşitli organlardaki kılcal damarların geçirgenliği. In: Scand Açta Physiol 58 1963 sayfa 292-305.. PMID 14078649 .
- ↑ JB van Bree ve diğerleri: Kan-beyin bariyerinden ilaç taşınması, II. İlaç taşınmasını incelemek için deneysel teknikler. İn: İlaç VVeekbl Sci 14, 1992, sayfa 338-348.. PMID 1475172 (İnceleme).
- ↑ L. Sokoloff ve diğerleri: Lokal serebral glikoz kullanımının ölçümü için [14C] deoksiglukoz yöntemi: bilinçli ve anestezi uygulanmış albino sıçanda teori, prosedür ve normal değerler. İçinde: J Neurochem 28, 1977, s. 897-916. PMID 864466 .
- ↑ JD Fenstermacher, L. Wei: Kantitatif otoradyografi ile lokal serebral kılcal geçirgenlik yüzey alanı ürünlerinin ölçülmesi. İçinde: Kan-beyin bariyerine giriş: metodoloji, biyoloji ve patoloji Cambridge University Press, 1998, ISBN 0-521-58124-9 , s. 122-132.
- ↑ a b E. CM de Lange ve diğerleri: Kan-beyin bariyeri taşıma özelliklerindeki değişiklikleri belirlemek için intaserebral mikrodiyaliz kullanımı. İn: Pharm Res 12, 1995, s 129-133.. PMID 7724474 .
- ↑ ECM de Lange ve diğerleri: Fare beynindeki ilaçların farmakokinetiğini belirlemek için bir teknik olarak intraserebral mikrodiyalizin kritik faktörleri. İçinde: Brain Res 666, 1994, sayfa 1-8. PMID 7889356 .
- ↑ a b E. CM de Lange ve diğerleri: Kan-beyin bariyeri boyunca ilaç taşınmasına ilişkin farmakokinetik çalışmalarda intraserebral mikrodiyalizin metodolojik değerlendirmeleri. In: Brain Res Brain Res Rev 25, 1997, s. 27-49. PMID 9370049 (İnceleme).
- ↑ ECM de Lange ve diğerleri: MDR1A (- / -) ve vahşi tip fareler kullanılarak BBB aktarımı ve P-glikoprotein işlevselliği. Rodamin-123'ün mikrodiyaliz konsantrasyonuna karşı toplam beyin. İn: Pharm Res 15, 1998, s 1657-1665.. PMID 9833984 .
- ↑ T. Terasaki ve diğerleri: Dinorfin benzeri bir analjezik peptidin, E 2078, kan-beyin bariyerinden in vivo taşınması: bir mikrodiyaliz uygulaması. İn: , J Pharmacol Exp Ther 251, 1991, sayfa 815-820.. PMID 1681528 .
- ↑ C. Berger ve diğerleri: İnmede serebral mikrodiyaliz. İçinde: Der Nervenarzt 75, 2004, s. 113–123. PMID 14770280 .
- ↑ G.Paterno: Die serebral mikrodiyaliz (PDF; 186 kB) bir uygulama raporu, Eylül 2001.
- ↑ a b S. Syvänen ve diğerleri: P-glikoprotein taşınmasına vurgu yapılarak üç PET radyoligandının kan-beyin bariyeri taşınmasındaki tür farklılıkları. In: Drug Metab Dispos 37, 2009, s. 635-643. PMID 19047468 .
- ↑ a b J. Bart ve diğerleri: Yeni pozitron emisyon tomografi izleyicisi (11) C-karvedilol, P-glikoprotein modülasyon kinetiğini ortaya çıkarır. İn: Br J Pharmacol 145, 2005, sayfa 1045-1051.. PMID 15951832 .
- ^ NH Hendrikse ve diğerleri: Tümörlerdeki P-glikoprotein taşınmasını ve kan-beyin bariyerini incelemek için yeni bir in vivo yöntem. İçinde: Cancer Res 59, 1999, s.2411-2416. PMID 10344751 .
- ↑ SS Zoghbi ve diğerleri: 11C-loperamid ve N-desmetil radyometabolit beyin geçirgenliği-glikoprotein çıkışı için hevesli substratlardır. İçinde: J Nucl Med 49, 2008, s. 649-656. PMID 18344435 .
- ^ V. Josserand ve diğerleri: Beyne İlaç Penetrasyonunun Değerlendirilmesi: Pozitron Emisyon Tomografisi ile in Vivo Görüntüleme ve İnsan Kan-Beyin Bariyerinin in Vitro Modelini Kullanan Çift Çalışma. İn: , J Pharmacol Exp Ther 316, 2006, sayfa 79-86.. PMID 16210395 .
- ↑ D. Matsuzawa ve diğerleri: Şizofrenide Beyin Glutatyon Düzeyi ile Negatif Semptomlar Arasındaki Negatif Korelasyon: Bir 3T 1H-MRS Çalışması. İçinde: PLoS ONE 3, 2008, e1944. PMID 18398470 .
- ↑ M. Bartels ve diğerleri: Nöroleptiklerin 19F Nükleer Manyetik Rezonans Spektroskopisi: Sıçan beyninde trifluoperazinin ilk in vivo farmakokinetiği ve insan beyninde flufenazinin ilk in vivo spektrumu. İçinde: Biol Psychiatry 30, 1991, s. 656-662. PMID 2386658 .
- ↑ JJH Ackerman ve diğerleri: Yüzey bobinleri kullanılarak 31P NMR ile bütün hayvanlarda metabolitlerin haritalanması. İçinde: Nature 283, 1990, s. 167-170. PMID 7350541 .
- ↑ JW Prichard ve diğerleri: 31P NMR ile in vivo serebral metabolik çalışmalar. İçinde: PNAS 80, 1983, s. 2748-2751. PMID 6573678 .
- ↑ Dünya Kupası Pardridge: Kan-beyin bariyeri ilacı hedefleme: beyin ilacı geliştirmenin geleceği. İçinde: Mol Interv 3, 2003, s. 90-105. PMID 14993430 (İnceleme).
- ^ DJ Begley: Terapötik ajanların merkezi sinir sistemine teslimi: sorunlar ve olasılıklar. İn: Pharmacol Ther , 104, 2004, s 29-45.. PMID 15500907 (İnceleme).
- ↑ WM Pardridge: Küresel CNS ilaç pazarına neden bu kadar az giriliyor ? In: Drug Discovery Today , 7, 2002, s. 5-7. PMID 11790589 .
- ^ AG de Boer, PJ Gaillard: Kan-beyin bariyerinde ilaç dağıtımını iyileştirme stratejileri. İn: Clin Pharmacokinet , 46, 2007, s 553-576.. PMID 17596102 (İnceleme).
- ^ AG de Boer ve PJ Gaillard: Beyne yönelik ilaç. İçinde: Annu Rev Pharmacol Toxicol , 47, 2007, s. 323-355. PMID 16961459 (İnceleme).
- ↑ BT Hawkins, RD Egleton: Kan-beyin bariyerinin patofizyolojisi: hayvan modelleri ve yöntemleri. İçinde: Curr Top Dev Biol 80, 2008, s. 277-309. PMID 17950377 (İnceleme).
- ^ A b c N. Weiss, F. Miller, S. Cazaubon, PO Couraud: Beyin homeostazı ve nörolojik hastalıklarda kan-beyin bariyeri. İçinde: Biochim. Biophys. Açta 1788, 2009, s. 842-857 PMID 19061857 (İnceleme).
- ^ I. Elmas ve diğerleri: Akut ve kronik olarak etanol ile tedavi edilen sıçanlarda derin hipoterminin kan-beyin bariyeri geçirgenliği üzerindeki etkileri. In: Forensic Science International 119, 2001, s. 212-216. PMID 11376985 .
- ^ SC Phillips, BG Cragg: Sıçandaki alkole bağlı stresler nedeniyle kan-beyin bariyerinin zayıflaması. İn: J. Neurol Sci , 54, 1982, sayfa 271-278.. PMID 7.201.507 .
- ↑ AK Singh ve diğerleri: Kronik etanol içmenin kan beyin bariyeri üzerindeki etkileri ve intraperitoneal LPS enjeksiyonuna tabi tutulmuş alkol tercih eden sıçanlarda nöronal toksisite. İçinde: Alkol Alkol , 42, 2007, s. 385-399. PMID 17341516 .
- ↑ a b J. Haorah ve diğerleri: Alkole bağlı kan-beyin bariyeri disfonksiyonuna, inositol 1,4,5-trifosfat reseptörü (IP3R)-kapılı hücre içi kalsiyum salınımı aracılık eder. İçinde: J Neurochem , 100, 2007, s. 324-336, PMID 17241155 .
- ↑ J. Haorah ve diğerleri: Miyozin hafif zincir kinazın etanol kaynaklı aktivasyonu, sıkı bağlantıların işlev bozukluğuna ve kan-beyin bariyeri uzlaşmasına yol açar. Alkolizm. In: Clinical and Experimental Research 29, 2005, pp. 999-1009. PMID 15976526 .
- ↑ J. Haorah ve diğerleri: Beyin endotel hücrelerinde alkole bağlı oksidatif stres, kan-beyin bariyer disfonksiyonuna neden olur. ( Memento arasında Mart 16, 2010 , Internet Archive ) in: Lökosit Biyoloji Dergisi , 78, 2005, s 1223-1232.. PMID 16204625 .
- ^ R. Peters ve diğerleri: Yaşlılarda sigara, demans ve bilişsel gerileme, sistematik bir derleme. İçinde: BMC Geriatr 8, 2008, s. 36. PMID 19105840 (İnceleme).
- ↑ bir B P.R. Lockman et al. , Kronik nikotin maruz kaldıktan sonra nikotin ve kotininin kinetik alımı Beyin. İn: , J Pharmacol Exp Ther 314, 2005, sayfa 636-642.. PMID 15845856 .
- ↑ TJ Abbruscato ve diğerleri: Nikotin ve kotinin, beyin endotel hücrelerinde eksprese edilen nikotinik asetilkolin reseptörleri aracılığıyla ZO-1'in serebral mikrovasküler geçirgenliğini ve protein ekspresyonunu modüle eder. İn: J Pharm Sci 91, 2002, sayfalar 2525-2538.. PMID 12434396 .
- ↑ BT Hawkins ve diğerleri: Nikotin, in vivo kan-beyin bariyeri geçirgenliğini arttırır ve serebral mikrovasküler sıkı bağlantı protein dağılımını değiştirir. İçinde: Brain Res 1027, 2004, s. 48-58. PMID 15494156 .
- ↑ YH Chen ve diğerleri: İnsan beyni mikrovasküler endotel hücrelerinin gelişmiş Escherichia coli istilası, nikotin tarafından indüklenen hücre iskeletindeki değişimlerle ilişkilidir. İçinde: Cell Microbiol 4, 2002, s. 503-514. PMID 12174085 .
- ↑ PR Lockman ve diğerleri: Kronik nikotin maruziyeti, kan-beyin bariyer geçirgenliğini değiştirir ve metillikakonitinin beyin alımını azaltır. İn: , J Neurochem 94, 2005, s 37-44.. PMID 15953347 .
- ↑ M. Kotlyar ve DK Hatsukami: Nikotin bağımlılığını yönetmek. İçinde: J Dent Educ 66, 2002, s.1061-1073. PMID 12374267 .
- ^ PR Pentel et al.: Nikotin konjugat aşısı beyne nikotin dağılımını azaltır ve farelerde davranışsal ve kardiyovasküler etkilerini azaltır. İn: Pharmacol Biochem Behav 65, 2000, sayfa 191-198.. PMID 10638653 .
- ^ DE Keyler ve diğerleri: Nikotine karşı maternal aşılama, sıçanlarda fetal beyne nikotin dağılımını azaltır. İn: , J Pharmacol Exp Ther 305, 2003, sayfa 587-592.. PMID 12606612 .
- ↑ MG LeSage ve diğerleri: Bir nikotin konjugat aşısının sıçanlarda kendi kendine nikotin uygulamasının kazanılması ve sürdürülmesi üzerindeki etkileri. İçinde: Psychopharmacology 184, 2006, s. 409-416. PMID 15991003 .
- ^ DA D'Andrea ve ark. , Sinir sistemi üzerinde Mikrodalga etkileri. In: Biyoelektromanyetik 6, 2003, sayfa 107-147.. PMID 14628310 (İnceleme).
- ↑ TH Patel ve diğerleri: Periferik termal yaralanmayı takiben doku ve ürokinaz plazminojen aktivatörlerinin artan ekspresyonu ile ilişkili kan beyin bariyeri (BBB) disfonksiyonu. İçinde: Neurosci Lett 444, 2008, s. 222-226. PMID 18718505 .
- ^ I. Ruppe: Kan-beyin bariyerinin yapısı ve işlevi. ( Memento arasında Şubat 16, 2010 , Internet Archive ) (PDF; 113 kB) in: Haber Bülteni 1, 2003, s 15-17..
- ^ BR Persson ve diğerleri: Manyetik ve elektromanyetik alanların neden olduğu kan-beyin bariyerinin artan geçirgenliği. In: Ann NY Acad Sci 649, 1992, s. 356-358. PMID 1580510 .
- ^ LG Salford ve diğerleri: GSM cep telefonlarından mikrodalgalara maruz kaldıktan sonra memeli beyninde sinir hücresi hasarı. İçinde: Environ Health Perspect 111, 2003, s. 881-883. PMID 12782486 .
- ↑ H. ve diğerleri: Nittby radyo frekansı ve kan-beyin bariyeri üzerindeki aşırı düşük frekanslı elektromanyetik alan etkileri. İçinde: Electromagn Biol Med 27, 2008, s. 103-126. PMID 18568929 (İnceleme).
- ↑ JL Eberhardt ve diğerleri: GSM cep telefonlarından mikrodalgalara maruz kaldıktan 14 ve 28 gün sonra sıçan beyninde kan-beyin bariyeri geçirgenliği ve sinir hücresi hasarı. İçinde: Electromagn Biol Med 27, 2008, s. 215-229. PMID 18821198 .
- ^ LG Salford ve diğerleri: 915 MHz elektromanyetik radyasyon, sürekli dalga tarafından indüklenen ve 8, 16, 50 ve 200 Hz'de modüle edilen kan-beyin bariyerinin geçirgenliği. In: Microsc Res Tech 27, 1994, s. 535-542 . PMID 8012056 .
- ↑ A. Schirmacher ve diğerleri: Elektromanyetik alanlar (1.8 GHz), in vitro olarak kan-beyin bariyerinin sükroz geçirgenliğini arttırır. In: Bioelectromagnetics 21, 2000, s 338-345.. PMID 10899769 .
- ↑ H. Franke ve diğerleri: Elektromanyetik alanlar (GSM 1800), yüksek bariyer sıkılığına sahip in vitro modellerde kan-beyin bariyerinin sükroza geçirgenliğini değiştirmez. In: Bioelectromagnetics 26, 2005, s 529-535.. PMID 16142784 .
- ^ HJ Weinmann ve diğerleri: Gadolinyum-DTPA Kompleksinin Özellikleri: Potansiyel Bir NMR Kontrast Ajanı. İçinde: Am J Roentgenol 142, 1984, s. 619-624. PMID 6607655 .
- ↑ RC Brasch ve diğerleri: Kontrastlı NMR görüntüleme: gadolinyum-DTPA kompleksi kullanan hayvan çalışmaları. İçinde: Am J Roentgenol 142, 1984, s. 625-630. PMID 6607656 .
- ↑ VM Runge ve diğerleri: Akut Serebral Enfarktüslü Kedilerin MR Görüntülerinde Kan-Beyin Bariyeri Bozulmasının Görselleştirilmesi: Yüksek Doz Kontrast Malzemenin Uygulanmasının Değeri. İn: AJR Am J Roentgenol 162, 1994, sayfa 431-435.. PMID 8310940 .
- ↑ MA Ibrahim ve diğerleri: İnsan beyin omurilik sıvısında manyetik rezonans görüntüleme gevşeme süreleri ve gadolinyum-DTPA gevşeme değerleri. In: Invest Radiol 33, 1998, s. 153-162. PMID 9525754 .
- ↑ AV Alexandrov ve diğerleri: Akut inmede beyin SPECT taramalarında HMPAO alımının artmasının klinik önemi. In: J Neuroimaging , 6, 1996, s. 150-155. PMID 8704289 (inceleme).
- ↑ JC Masdeu, J. Arbizu: Beyin tek foton emisyonlu bilgisayarlı tomografi: teknolojik yönler ve klinik uygulamalar. İçinde: Semin Neurol 28, 2008, s. 423-434. PMID 18843571 (İnceleme).
- ↑ M. Essig: İnme için BT görüntüleme teşhisi. In: Visions 12, 2005, s. 15-17.
- ^ KA Miles: Tümör vaskülaritesinin değerlendirilmesi için Perfüzyon CT: hangi protokol? İn: Br J Radiol 76, 2003, sayfa 36-42.. PMID 15456712 .
- ↑ DA Leggett ve diğerleri: Fonksiyonel BT kullanarak serebral gliomun kan-beyin bariyeri ve kan hacmi görüntülemesi: resimli bir inceleme. İçinde: Eur J Radiol 30, 1999, s. 185-190. PMID 10452716 (İnceleme).
- ↑ P. Ehrlich: Organizmanın oksijen ihtiyacı: Renk-analitik bir çalışma. August Hirschwald, Berlin, 1885, 167 s. (Paul Ehrlich'in habilitasyon tezi).
- ↑ P. Ehrlich: Kimyasal yapı, dağıtım ve farmakolojik etki arasındaki ilişki hakkında. Bağışıklık araştırması üzerine toplu çalışma. August Hirschwald, Berlin, 1904, s.574.
- ↑ EE Goldmann: Sağlıklı ve hastalıklı organizmanın yaşamsal renk ışığında iç ve dış salgılanması. İçinde: Beitr Klin Chirurg 64, 1909, s. 192-265.
- ↑ EE Goldmann: merkezi sinir sistemi üzerinde yaşamsal boyama. İçinde: Abh K. Preuss. Akad Wiss. Phys. Med. 1, 1913, sayfa 1-60.
- ↑ A. Biedl, R. Kraus: Safra asitlerinin merkezi sinir sistemi üzerindeki önceden bilinmeyen toksik etkisi hakkında. İçinde: Zentralblatt Innere Medizin , 19, 1898, s. 1185–1200.
- ^ M. Lewandowsky: Beyin omurilik sıvısı doktrini üzerine. İçinde: Zentralblatt Klinische Medizin , 40, 1900, s. 480-494.
- ^ CS Roy, CS Sherrington: Beynin kan tedarikinin düzenlenmesi üzerine. (PDF; 3.7 MB) İçinde: J Physiol , 11, 1890, s. 85-108.
- ↑ AA Damar: Lina Stern: Bilim ve kader .
- ↑ FK Walter: Merkezi sinir sistemi ile vücudun geri kalanı arasındaki madde değişiminin genel temelleri. İçinde: Arch Psychiatr Nervenkr 101, 1930, s. 195-230.
- ↑ H. Spatz: Merkezi sinir sistemi ile vücudun geri kalanı arasındaki madde değişimi teorisi için hayati rengin önemi. İn: Arch Psychiatr Nervenkr 101, 1933, s 267-358..
- ^ U. Friedemann: Kan-beyin engeli. İçinde: Physiol Rev 22, 1942, s. 125-145.
- ↑ RD Tschirgi: Kan-beyin bariyeri: gerçek mi yoksa fantezi mi? İçinde: Fed Proc 21, 1962, s.665-671. PMID 13922779 .
- ^ G. Miller: Uyuşturucu hedefleme. Engelleri yıkmak. İçinde: Science 297, 2002, s. 1116-1118. PMID 12183610 .
- ↑ TS Reese, MJ Karnovsky: Eksojen peroksidaza karşı bir kan-beyin bariyerinin ince yapısal lokalizasyonu. İçinde: J Cell Biol 34, 1967, s. 207-217. PMID 6033532 .