Glukoneogenez
| Ebeveyn |
| Glikoz metabolizması |
| Gen ontolojisi |
|---|
| QuickGO |
Glukoneojenez ( latinisierte durumunda glukoneogenez , bir bileşik, bir kelime ile ilgili eski Yunan γλυκύς glykys "tatlı", νέος Neos "yeni" ve γένεσις oluşum "nesil") oluşumudur D - glukoz gibi organik olmayan karbonhidrat öncüllerinin piruvat , oksaloasetat ve dihidroksiaseton fosfat . Metabolik yol, evrensel olarak tüm canlılarda bulunabilir. İnsanlarda ve omurgalılarda , başlangıç malzemeleri , proteinlerin parçalanmasından gelen amino asitlerdir . Bitkiler , mantarlar , çoğu bakteri ve bazı omurgasızlar , asetil-CoA'dan ve dolayısıyla yağ asitlerinden glikoz üretmek için glioksilat döngüsünü kullanabilir .
İnsanlarda glukoneogenez ihtiyacı
Yetişkin bir kişinin günlük glikoz ihtiyacı istirahatte yaklaşık 200 gr olup, bunun% 75'i beyin tarafından, geri kalanının büyük bir kısmı eritrositler tarafından kullanılmaktadır . Vücutta depolanan glikojen miktarı yaklaşık 400 ila 450 gr'dır. Bunun yaklaşık üçte ikisi kaslarda ve yaklaşık üçte biri karaciğerde depolanır. Kandaki mevcut glikoz miktarı yaklaşık 5 mmol / L'dir ve bu yaklaşık 900 mg / L veya 90 mg / dL'ye karşılık gelir.
Eritrositler insan ve memeli olmayan mitokondri ve dolayısıyla enerji üretmek için glukoz kaynağı, doğrudan bağlantılıdır kırmak üzerinden aşağı glikoliz ve daha sonra laktik asit fermentasyonu . Beyin, hızla elde edilebilen enerjiye olan muazzam ihtiyacını, esas olarak glikozun parçalanması yoluyla karşılar. Bu, esas olarak karaciğer ve böbrek korteksinde ve daha az beyin, iskelet ve kalp kaslarında gerçekleşen nispeten kısa açlık dönemlerinde bile glikoz sentezinin başlamasının ana nedenidir . Glukoneojenezde glikoz birikmesi nedeniyle, glikoz konsantrasyonu hiçbir zaman 3,5 mmol / L'nin (yaklaşık 600 mg / L, 60 mg / dL) altına düşmez. Günde yaklaşık 180 ila 200 g glikoz oluşturulabilir.
Glukoneogenez seyri
Hücresel yerelleştirme
Ökaryotlarda glukoneogenezin seyri, bir hücrenin üç bölmesine dağılmıştır . Çoğunluk sitozolde yer alır . Bir reaksiyon aşaması yer alır mitokondri , başka bir düz endoplazmik retikulum (sonra SER İngilizce endoplazmik retikulum düz her biri için gerekli olduğundan,) , enzim ( piruvat karboksilaz ve glikoz-6-fosfataz sadece burada vardır).
Tepki adımları
Glukoneojenez için başlangıç malzemeleri, (1) amino asit parçalanması ve laktik asit fermantasyonunun ürünleri olarak piruvat veya oksaloasetattır ( laktattan ), (2) kaslarda anaerobik olarak oluşan piruvat ( Cori döngüsü ), (3) dihidroksiaseton fosfat türevi olarak yağ parçalanmasından kaynaklanan gliserol veya 4) Çift sayılı yağ asitleri parçalandığında β-oksidasyonun son adımından sonra kalan propiyonat . Bu dönüştürülür propionil-CoA karboksilaz ve rasemaz içerisine (metilmalonil-CoA epimeraz) sukkinil-CoA olan, oksaloasetat oluşturulur esnasında sitrik asit döngüsü .
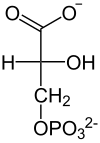
L- laktattan glukoz yapısı aşağıda gösterilmiştir:
 |
NAD + NADH + H + laktat dehidrojenaz  |
 |
HCO 3 - ATP, ADP + U i piruvat karboksilaz |
 |
GTP GSYİH + CO 2 PEPCK |
 |
|
| L- laktat | Piruvat | Oksaloasetat | Fosfoenolpiruvat |
 |
+ H 2 O enolaz  |
 |
Fosfo gliserat mutaz 
|
 |
ATP ADP fosfo gliserat kinaz |
|
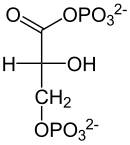
| Fosfoenolpiruvat | D - 2-fosfogliserat | D - 3-fosfogliserat | D -1,3-bifosfogliserat |
 |
NADH NAD + + H + + U i , gliseraldehit-3-fosfat dehidrojenaz  |
 |
Trioz fosfat izomeraz  |
 |
Fruktoz 1,6 bifosfat aldolaz |

|
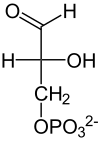
| D - 1,3-bifosfogliserat |
D - gliserol aldehit 3-fosfat |
Dihidroksi aseton fosfat |
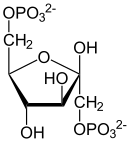
β- D - fruktoz-1,6-bifosfat |
 |
H 2 O P i fruktoz 1,6-bifosfataz |
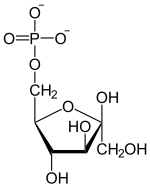 |
Glikoz-6-fosfat izomeraz |
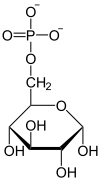 |
H 2 O P i glikoz-6-fosfataz |

|
| β- D - fruktoz-1,6-bifosfat | β- D - fruktoz-6-fosfat | α- D - glikoz-6-fosfat | α- D - glikoz |
Glukoneogenez , glikolizin ters reaksiyonuna sadece kısmen karşılık gelir . Bununla birlikte, glikolizde, kimyasal dengenin hemen hemen sadece reaksiyon ürünleri tarafında olduğu üç reaksiyon vardır . Hepsi kinazlar tarafından katalize edilen bu adımlar şunlardır:
- glikozun glikoz-6-fosfata dönüşümü,
- fruktoz-6-fosfattan fruktoz-1,6-bifosfata ve
- fosfoenolpiruvatın (PEP) piruvata reaksiyonu.
Bu reaksiyonları tersine çevirmek için hücrenin aşırı konsantrasyonlar oluşturabilmesi gerekir. Bu nedenle, glikolizdeki bu üç adım fiilen geri döndürülemezdir ve glukoneogenezde aşağıdaki gibi ters sırada atlatılır:
- ATP ( piruvat karboksilaz ) kullanılarak piruvatın oksaloasetata karboksilasyonu ve ardından oksaloasetatın GTP (fosfoenolpiruvat karboksikinaz) kullanılarak PEP'e fosforile dekarboksilasyonu ;
- fruktoz 1,6-bifosfatın fruktoz 6-fosfata reaksiyonunu katalize eden fruktoz-1,6-bifosfataz ;
- Glukoz-6-fosfat olan dönüştürülmüş içine glukoz ile glükoz-6-fosfataz (glikolizde bir heksokinaz veya glukokinaz (heksokinaz IV) katalize reaksiyonu ters yönde ).
Diğer dönüşüm süreçleri denge halindedir, bu yüzden glukoneogenezde de rol oynarlar.
Glikolizden bir diğer önemli fark, reaksiyonun yeridir. Bu sadece sitozolde gerçekleşirken , glukoneogenez üç bölmeye dağılmıştır . Piruvatın oksaloasetata dönüşümü mitokondrinin lümeninde gerçekleşir . Bununla birlikte, oksaloasetat mitokondrinin iç zarından serbestçe geçemez ve önce dönüştürülmelidir. Bunu yapmanın iki yolu var. Her iki mitokondriyal oksaloasetat, bir mitokondriyal PEP karboksikinaz tarafından PEP'e dönüştürülür. PEP daha sonra mitokondriyi özel bir anyon mekik sistemiyle terk eder. Sitoplazmada, PEP, glukoneogenezin bir sonucu olarak glikoza dönüştürülür.
Açsanız ulaşım için ikinci bir rota alınır. Olarak karaciğer , L - alanin olan piruvata deamine ve böylece oksaloasetat bir kaynağı olarak işlev görür. Acıktığınızda, NADH formundaki indirgeyici ajan miktarı sitozolde düşük ve mitokondride yüksektir. Bununla birlikte, sitozolde glukoneogenez için NADH gereklidir. Sözde malat-aspartat mekik sistemi, hem NADH hem de oksaloasetatı mitokondriden sitozole taşımak için kullanılır. Mitokondride üretilen oksaloasetat olan düşük için L - malat mitokondriyal ile malat dehidrojenaz ve daha sonra, iç zar içinden transloke edilebilir. Malat-aspartat mekiğine ek olarak, mitokondriyal dikarboksilat taşıyıcı da taşıma için kullanılabilir. Sitozolde, bir sitosolik malat dehidrojenaz, malatı oksaloasetata okside eder, böylece NAD +, NADH'ye indirgenir ve glukoneojenezde kullanılır.
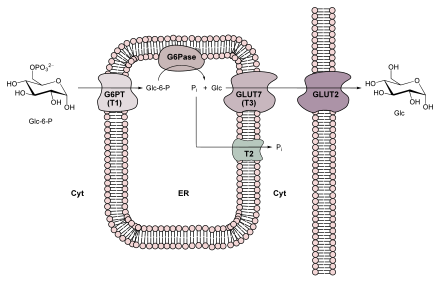
Glukoneogenezdeki son reaksiyon adımı sitozolde değil, endoplazmik retikulumun (ER) lümeninde gerçekleşir . ER'ye taşıma ve glikoz-6-fosfatın hidrolizi, glikoz- 6-fosfat translokaz ve glikoz-6-fosfatazdan oluşan bir glikoza özgü zar enzim kompleksi tarafından gerçekleştirilir (ayrıca bkz. Sağdaki şekil).
Piruvat karboksilaz
Piruvat karboksilaz sadece protez grubu olan biotin ile aktiftir . Biotin, aktif karbondioksitin hareketli bir taşıyıcısı olarak işlev görür . Biyotin, karboksi grubu yoluyla belirli bir lizin kalıntısının ε-amino grubuna bağlanır . Bu, biyotin grubunun bir aktif merkezden diğerine "sallanmasına" izin veren esnek bir kol oluşturur. Karboksilasyon iki adımda gerçekleşir:
İlk kısmi reaksiyon asetil-CoA varlığına bağlıdır, bu olmadan biotinin karboksilasyonu mümkün değildir. Yüksek asetil-CoA seviyesi sitrik asit döngüsünde daha fazla oksaloasetat ihtiyacının bir işareti olduğundan, bu düzenleme bir alaşım şeklidir . Asetil-CoA, enzimin güçlü ve tek efektörüdür. Oksaloasetat, glukojenez için kullanılabilir veya sitrik asit döngüsüne dahil edilebilir . Piruvat karboksilazın katalize reaksiyonu, bir anaplerotik reaksiyon örneğidir . Aşırı ATP varsa, oksaloasetat glukoneojenezde tüketilir, bu da zengin olmadığı anlamına gelir. Piruvat karboksilazın ikinci reaksiyon adımı asetil-CoA bağımsızdır.
Glukoneogenez ve glikolizin karşılaştırılması
Glikolizin tersine çevrilmesine kıyasla enerji dengesi
Piruvattan başlayarak bir glikoz molekülünün biyosentezi için dört ATP molekülü ve her biri GTP ve NADH'den iki molekül gereklidir.
Aşağıda gösterilen denge, glikolizin doğrudan tersine çevrilmesi termodinamik olarak elverişsiz bir reaksiyonu temsil ettiğinden, üst reaksiyonun tercihli olarak gerçekleşeceğini açıkça ortaya koymaktadır:
Bu, altı ATP eşdeğeri (2 GTP + 4 ATP) gerektiği anlamına gelir, böylece bir molekül glikoz oluşturmak için glukoneojenez gerçekleşebilir.
Glukoneogenez ve Glikoliz - Karşılıklı Düzenleme
Glukoneogenez ve glikoliz birkaç enzimatik reaksiyonu paylaşır, ancak iki tamamen zıt metabolik yolaktır. Bu nedenle düzenlemeye ihtiyaç vardır. İki yerde gerçekleşir:
- piruvattan PEP'e reaksiyonlarda ve
- fruktoz-1,6-bifosfatın fruktoz-6-fosfata dönüştürülmesinde.
İlk reaksiyon: PEP'in glikolizde meydana gelen piruvata dönüşümü, piruvat kinaz tarafından katalize edilir . Aktivitesi , bu enzimin früktoz-1,6-bisfosfat artarak ATP ve alanin tarafından inhibe edilir. Glukoneogenez enzimleri (piruvat karboksilaz ve PEP karboksilinaz) asetil-CoA tarafından aktive edilir ve ADP tarafından inhibe edilir. ATP, hidroliz yoluyla ADP'ye dönüştürüldüğünden, iki karşıt reaksiyonun bu tür düzenlemesi, karşılıklı düzenleme olarak adlandırılabilir. Diğer bir örnek, 2'nin altında listelenen reaksiyondur. Glikolizde yer alan fosfofruktokinaz, fruktoz-2,6-bifosfat ve adenozin monofosfat (AMP) tarafından uyarılır, ancak diğer şeylerin yanı sıra sitrat tarafından inhibe edilir . Karşılıklı olarak, glukoneogenezde yer alan fruktoz-1,6-bifosfatazın düzenlenmesi gerçekleşir (sitrat tarafından aktive edilir ve fruktoz-2,6-bifosfat ve AMP tarafından inhibe edilir).
Edebiyat
- Geoffrey Zubay: biyokimya. 4. baskı. Mcgraw-Hill Professional, 1999, ISBN 3-89028-701-8 .
- Donald Voet, Judith G. Voet: Biyokimya . Wiley-VCH, 1994, ISBN 3-527-29249-7 .
- Jeremy M. Berg, John L. Tymoczko, Lubert Stryer: Biyokimya. 6. baskı. Spectrum Akademischer Verlag, Heidelberg 2007, ISBN 978-3-8274-1800-5 .
- H. Robert Horton, Laurence A. Moran, K. Gray Scrimgeour, Marc D. Perry, J. David Rawn, Carsten Biele (çevirmen): Biochemie . 4. güncellenmiş baskı. Pearson Studies, 2008, ISBN 978-3-8273-7312-0 .
- Reginald Garrett, Charles M. Grisham: Biyokimya . (Uluslararası Öğrenci Sürümü). 4. baskı. Cengage Learning Services, 2009, ISBN 978-0-495-11464-2 .
- David L. Nelson, Michael M. Cox, Albert L. Lehninger (ilk): Lehninger Biochemie . 4., tamamen revize edildi ve exp. Baskı. Springer, Berlin 2009, ISBN 978-3-540-68637-8 .
İnternet linkleri
Bireysel kanıt
- ↑ Gerd P. Püschel, Hartmut Kühn, Thomas Kietzmann, Wolfgang Höhne, Bruno Christ: Pocket Textbook Biochemistry . 1. baskı. Georg Thieme Verlag, 2018, ISBN 9783132429031 , s.252 .
- ^ BH Robinson: Memeli mitokondrilerinde trikarboksilat taşıma sistemi ile fosfoenolpiruvatın taşınması. İçinde: FEBS Lett . 14 (5), 1971, s. 309-312. PMID 11945784 .
- ↑ S. Jitrapakdee, M. St. Maurice ve diğerleri: Piruvat karboksilazın yapısı, mekanizması ve düzenlenmesi. İn: Biochem J . 413 (3), 2008, s. 369-387. PMID 18613815 ; doi: 10.1042 / BJ20080709 .
- ^ H. Robert Horton, Laurence A. Moran, K. Gray Scrimgeour, Marc D. Perry, J. David Rawn, Carsten Biele (çevirmen): Biochemie. 4. güncellenmiş baskı. Pearson Studium, 2008, ISBN 978-3-8273-7312-0 , s. 483.
- ↑ Jeremy M. Berg, John L. Tymoczko, Lubert Stryer: Biochemistry. 6. baskı. Spektrum Akademischer Verlag, Heidelberg 2007, ISBN 978-3-8274-1800-5 , s.518 .







