Bakır (II) sülfür
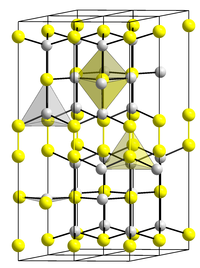
| Kristal yapı | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||
| __ Cu 2+ __ S 2− | |||||||||||||||||||
| Genel | |||||||||||||||||||
| Soyadı | Bakır (II) sülfür | ||||||||||||||||||
| diğer isimler |
|
||||||||||||||||||
| Oran formülü | CuS | ||||||||||||||||||
| Kısa açıklama |
siyah katı |
||||||||||||||||||
| Harici tanımlayıcılar / veritabanları | |||||||||||||||||||
| |||||||||||||||||||
| özellikleri | |||||||||||||||||||
| Molar kütle | 95,61 g · mol -1 | ||||||||||||||||||
| Fiziksel durum |
sıkıca |
||||||||||||||||||
| yoğunluk |
4,6 g cm −3 |
||||||||||||||||||
| Erime noktası |
507 ° C (ayrışma) |
||||||||||||||||||
| çözünürlük |
suda neredeyse çözünmez (0.33 mg l 1 , 18 ° C) |
||||||||||||||||||
| güvenlik talimatları | |||||||||||||||||||
| |||||||||||||||||||
| MAK |
0.1 mg m- 3 |
||||||||||||||||||
| Mümkün olduğunca ve geleneksel olarak, SI birimleri kullanılır. Aksi belirtilmedikçe, verilen veriler standart koşullar için geçerlidir . | |||||||||||||||||||
Bakır (II) sülfat , bir olan kimyasal bileşik arasında bakır ve kükürt . CuS oran formülüne sahip siyah, kırılgan bir katıdır. Bu orana rağmen, bileşik sadece Cu 2+ iyonları içermez , aynı zamanda Cu + ve Cu 2+ iyonlarının yanı sıra sülfür iyonları ve disülfür iyonlarının bir karışımından oluşur . Kesin oran Cu 2 I Cu II (S 2 ) S'dir.
Oluşum
Bakır (II) sülfit, mineral kovellin olarak doğal olarak bulunur .
Çıkarma ve sunum
Bakır (II) sülfit, örneğin hidrojen sülfit katılarak sulu çözeltiden çökeltme yoluyla (laboratuvarda) üretilir .
Bakır (I) sülfür / sülfür karışımının oda sıcaklığında reaksiyona sokulmasıyla oldukça saf bakır (II) sülfit elde edilir .
özellikleri
Fiziki ozellikleri
Bakır (II) sülfür, sülfidik bakır cevheri olarak doğal olarak oluşan siyah, suda çözünmeyen bir katıdır. Elektriksel olarak iletkendir. Nemli havada, cevher bakır (II) sülfür, bakır sülfata oksitlenir. Bileşik, oda sıcaklığında kuru havada stabildir. Bakır (II) sülfür havasız ortamda ısıtılırsa 507 ° C'de bakır (I) sülfür ve sülfüre dönüşür. Elde edilen bakır sülfit, stokiyometrik olarak oluşturulmaz ve Cu 2-x S formuyla daha iyi tanımlanabilir.
Cevherin havada kavrulması ise bakır (II) oksit ve kükürt dioksite yol açar.
Bakır (II) sülfat ile Bir altıgen kristal yapıya sahip olan boşluk grubu P 6 3 / MMC (boşluk grubu sayısı 194) , (a = 3.794 Â, c = 16.33 A) ve -48,5 KJ / mol oluşumunun entalpisi.
Kimyasal özellikler
Bakır (II) sülfür yalnızca konsantre, oksitleyici asitlerde çözünür . Örneğin, 3 mol CuS, 8 mol kons. Nitrik asitten bakır sülfata (3 mol), nitrojen monoksite (8 mol) ve suya ( redoks reaksiyonu ). Seyreltik asitlerde çözünmez. Gelen katyon ayırma işlemi , bu nedenle daha önce olduğu çökeltilmiş olarak hidrojen sülfür grubunun pH 4-5 de nitrik asit içinde eritildi ve, tespit bakır tetrammine olarak kompleks ile amonyak , su ( katyonların kanıt , tespit reaksiyonu ).
kullanım
Bakır (II) sülfür, kirlenme önleyici kaplamalar için kullanılır.
1970'lerde ve 1980'lerde, bakır (II) sülfür, kalp pilleri için lityum pillerde bir katot malzemesi olarak kullanıldı .
Bireysel kanıt
- ↑ bir b c d e üzerine kayıt bakır (II) sülfat olarak ve GESTIS madde veritabanı IFA , 19 Aralık 2019 tarihinde erişilebilir. (JavaScript gerekli)
- ↑ a b R. Blachnik, A. Müller: Elementlerden Cu 2 S oluşumu . I. Toz halinde kullanılan bakır . İçinde: Thermochimica Açta . bant 361 , hayır. 1-2 , Ekim 2000, s. 31-52 , DOI : 10.1016 / S0040-6031 (00) 00.545-1 .
- ^ AF Holleman , E. Wiberg , N. Wiberg : Ders Kitabı İnorganik Kimya . 102. baskı. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1 .
- ↑ a b c Georg Brauer (Ed.), Marianne Baudler ve diğerlerinin işbirliği ile : Hazırlayıcı İnorganik Kimya El Kitabı. 3., gözden geçirilmiş baskı. Cilt II, Ferdinand Enke, Stuttgart 1978, ISBN 3-432-87813-3 , s. 982.




