Nikotinamid adenin dinükleotid
| Yapısal formül | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
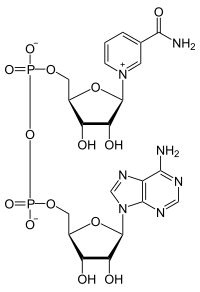
| ||||||||||||||||||||||
| NAD + (oksitlenmiş form) | ||||||||||||||||||||||
| Genel | ||||||||||||||||||||||
| Soyadı | Nikotinamid adenin dinükleotid | |||||||||||||||||||||
| diğer isimler | ||||||||||||||||||||||
| Moleküler formül |
|
|||||||||||||||||||||
| Kısa açıklama |
renksiz, higroskopik toz ( oksitlenmiş form, iç tuz ) |
|||||||||||||||||||||
| Harici tanımlayıcılar / veritabanları | ||||||||||||||||||||||
| ||||||||||||||||||||||
| özellikleri | ||||||||||||||||||||||
| Molar kütle |
|
|||||||||||||||||||||
| Fiziksel durum |
sıkıca |
|||||||||||||||||||||
| Erime noktası |
140–142 ° C (ayrışma) ( oksitlenmiş form, iç tuz ) |
|||||||||||||||||||||
| çözünürlük |
az suda (10 g l −1 ) |
|||||||||||||||||||||
| güvenlik talimatları | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Mümkün olduğunca ve geleneksel olarak, SI birimleri kullanılır. Aksi belirtilmedikçe, verilen veriler standart koşullar için geçerlidir . | ||||||||||||||||||||||
Nikotinamid adenin dinükleotid ( nikotinamid - adenin - dinükleotid kısaltılır, NAD ) a, koenzim resmi bir şekilde olan hidrit (iki transfer elektronlar : 2 E Kısacası, - ve bir proton , H + ). Bu çok sayıda katılır redoks reaksiyonlarının ait metabolizması ait hücrenin içeriyordu.
IUPAC / IUBMB göstermektedir kısaltmalar NAD + oksitlenmiş form için, NADH + H + , genel olarak indirgenmiş biçimdedir ve NAD. Bazen NAD + yerine NAD ve NADH + H + yerine NADH 2 vardır . NADH 2'nin yazılışı yanlıştır çünkü protonlar molekülün farklı yerlerine bağlanırlar.
Koenzim tarafından 1906 yılında keşfedilmiştir Arthur Harden'la ve William Young (sertleşir ve genç esterleri). NAD + , 1960'ların başlarına kadar, Diphosphopyridinnucleotid kısaltılmış DPN olarak da bilinen veya Codehydrase I , Codehydrogenase I veya bilinen koenzim I adı altında olan eski literatürdeydi .
Kıyasla nikotinamid adenin dinükleotid fosfat (NADP + ) ve nikotin asit adenin dinükleotid fosfat , iki koenzimler, aksi hemen hemen aynı şekilli (NAADP), 2 'C atomu hem de adenozin bir fosfat radikali olması, NAD de normal bir hidroksil vardır.
kimya
NAD'nin Redoks reaksiyonu: NAD + , iki elektron (e - ) ve bir proton (H + ) alarak NADH'ye indirgenebilir.
biyokimya
işlevi
Nernst denklemine göre, NAD + / NADH redoks çiftinin redoks potansiyeli , NAD + / NADH konsantrasyon oranına bağlıdır . Bu büyükse, redoks potansiyeli daha pozitiftir (daha yüksek oksitleme kapasitesi); eğer bu küçükse, daha negatiftir (daha yüksek indirgeme gücü). NAD + organizmada çoğunlukla bir oksitleyici ajan olarak görev yaptığından, NAD + / NADH oranı büyüktür (≫1). Buna karşılık, düşük bir NADP + / NADPH (≪1) oranına sahip olan NAD P H, birincil olarak indirgeme ajanı olarak kullanılır . Tek bir redoks çiftinin aynı anda biyolojik oksidasyonlar için yüksek bir redoks potansiyeli ve biyolojik indirgeme için düşük bir redoks potansiyeli sağlayamaması gerçeği, iki farklılaştırılabilir redoks kofaktörünün olmasının sebebidir .
Enerji açısından zengin indirgenmiş form NADH, oksidatif metabolizmada solunum zincirinin enerji sağlayan bir koenzimi olarak kullanılır , böylece ATP üretilir. Oksitlendiğinde, daha önce katabolik glikoz ve / veya yağ metabolizmasında emilen elektronları serbest bırakır ve oksijene aktarır. Bu sonuçta NAD + ve hidrojeni yaratır .
NAD + ayrıca dehidrojenazların bir koenzimidir , örn. B. Alkol dehidrojenaz (ADH), alkolü okside eder.
biyosentez
NAD + , vücutta nikotinik asit (niasin, B3 vitamini) ve nikotinamidden ve ayrıca amino asit triptofanın parçalanma ürünlerinden üretilir . Her iki başlangıç materyali de gerekli olduğundan, Pellagra gibi eksiklik semptomları mümkündür, ancak iki olası metabolik yol nedeniyle Avrupa'da oldukça nadirdir.
Her iki reaksiyon yolu ait bir düğümdür nikotinat D -ribonucleotide vasıtasıyla nikotinik asitten, doğrudan oluşturulabilir, nikotinat fosforibosil transferaz ya da ortaya çıkan triptofan parçalanma ürünü ile ilgili kuinolinik asit enzimi vasıtasıyla kinolinat fosforibosil transferaz . İkinci reaksiyon esas olarak karaciğerde gerçekleşir . Bir sonraki adımda nikotinat D-ribonükleotide adenozin fosfat eklenir. Bu reaksiyon, nikotinamid nükleotid adenilil transferaz tarafından katalize edilir ve deamido-NAD + oluşur . Bu nihayet NAD sentaz aracılığıyla NAD + 'ya aminlenir .
Başka bir sentetik yol, nikotinamid fosforibosil transferaz ile dinükleotide dönüştürülen nikotinamid ile başlar ; bu zaten bir amiddir , öyle ki sadece adenozin fosfatın yukarıdakilerle transferi. NAD + elde etmek için transferaz gereklidir .
Yüksek enerjili, indirgenmiş NADH formu, katabolizmada ( glikolizde ve sitrik asit döngüsünde ) üretilir .
Soğurma özellikleri
Nikotinamid adenin dinükleotid, hem indirgenmiş (NADH) hem de oksitlenmiş (NAD + ) formunda (cf. yapısal formül) özdeş bir adenin bölgesine sahiptir . Bu, 260 nm'lik bir dalga boyunda ışığı absorbe eder ve bu, diyagramda gösterilen 260 nm aralığında ortak absorpsiyon maksimumunu açıklar.Burada , bu aralıktaki NAD + absorpsiyonunun, aynı konsantrasyondaki NADH'den daha yüksek olduğu dikkat çekicidir. maddeler . Bunun nedeni , 260 nm'de de absorbe olan oksitlenmiş mezomerik nikotinamid halkasının absorpsiyonunun adenin absorpsiyonu üzerine bindirilmesi ve böylece 260 nm'de artan absorpsiyonu sağlamasıdır. Nikotinamid halkası azaltılırsa, 340 nm dalga boyuna sahip ışığı emen bir kinoid sistem oluşturulur . 340 nm'de NADH'nin (ve NADPH'nin) molar ekstinksiyon katsayısı ԑ ԑ = 6300 l / (mol · cm) 'dir.
UV spektrumundaki NAD + ve NADH arasındaki bu fark , bir spektrofotometrede koenzimin oksitlenmiş ve indirgenmiş formu arasındaki dönüşümü gözlemlemeyi mümkün kılar. Örneğin, kullanılan enzim substrat olarak NAD + kullanıyorsa , NADH'nin oksidasyonu veya NAD + azalması bir enzim analizinde fotometrik olarak gözlemlenebilir . Dönüştürülen substrat miktarı 340 nm'de absorpsiyondaki değişiklikle fotometrik olarak izlenebilir ; konsantrasyon daha sonra Lambert-Beer yasası yardımıyla belirlenebilir . Bu, dönüştürülen ortak substrat miktarı ile orantılı olduğundan, dönüştürülen substrat ve üretilen ürün miktarı hakkında dolaylı niceliksel ifadeler mümkündür. Öte yandan, substratın ve ürün konsantrasyonunun doğrudan izlenmesi genellikle daha zordur.
İnternet linkleri
- reactome.org: Nikotinat metabolizması
Bireysel kanıt
- ↑ üzerinde giriş nikotinamid adenin dinükleotid içinde bir Cosing veritabanı AB Komisyonu, 28 Ocak 2021 tarihinde erişti.
- ↑ a b c d Nikotinamid adenin dinükleotid girişi . İçinde: Römpp Çevrimiçi . Georg Thieme Verlag, 9 Aralık 2014'te erişildi.
- ↑ a b c Veri sayfası NAD + , Free Acid - CAS 53-84-9 - Merck'ten Calbiochem (PDF), 21 Aralık 2019'da erişildi.
- ↑ A. Harden, WJ Young: Maya suyunun alkollü fermenti. In: (a Biyolojik karakter ed olan makaleler İçeren Seri B). Londra Royal Society Proceedings , Cilt 78, No. 526, Ekim 1906, sayfa 369-375.. ( doi : 10.1098 / rspb.1906.0029 ).
- ↑ M. Nakamura, A. Bhatnagar, J. Sadoshima: Piridin nükleotidleri inceleme serisine genel bakış. İçinde: Dolaşım araştırması. Cilt 111, Sayı 5, Ağustos 2012, s. 604-610. ( doi : 10.1161 / CIRCRESAHA.111.247924 ; PMID 22904040 ; PMC 3523884 (ücretsiz tam metin)).
- ↑ C. Cantó, J. Auwerx: Metabolizmayı modüle eden bir sinyal molekülü olarak NAD +. İçinde: Nicel biyoloji üzerine Cold Spring Harbor sempozyumları. Cilt 76, 2011, s. 291-298 ( doi : 10.1101 / sqb.2012.76.010439 ; PMID 22345172 ; PMC 3616234 (ücretsiz tam metin)).
- ↑ Fukuwatari T, Morikawa Y, Hayakawa F, Sugimoto E, Shibata K: Adenin kaynaklı böbrek yetmezliğinin sıçanlarda triptofan-niasin metabolizması üzerindeki etkisi . İçinde: Biyobilim, Biyoteknoloji ve Biyokimya . 65, No. 10, Ekim 2001, sayfa 2154-2161. PMID 11758903 .
- ↑ HU Bergmeyer: Rutin laboratuvarlarda kullanılmak üzere NADH ve NADPH'nin molar yok olma katsayıları için yeni değerler . In: Journal of Clinical Chemistry and Clinical Biochemistry . bant 13 , hayır. 11 . Walter de Gruyter, Berlin Kasım 1975, s. 507-508 , PMID 3038 .





